Файл: Пояснительная записка Содержание и структура заданий.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 09.11.2023
Просмотров: 218
Скачиваний: 2
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
СОДЕРЖАНИЕ
ЕЗЕЛОЖ- без этого элемента вы не отрежете хлеб;
СЛИКОДОР- без него не проживете и 10 минут;
ЕКЛИНЬ - этот элемент помогает бороться первому элементу со вторым;
МФОЛЬВАР- из него сделана спираль лампочки накаливания;
ПРИТОНК- его можно найти в лампочках грибовидной формы;
МЕДИНЛОБ- элемент помогает лампочке держать спираль;
МНИКРЕЙ- элемент ищи среди камней;
ЛЕОДРУГ-без этого элемента нет огня;
Проверочная работа. «Относительная атомная и молекулярная масса»
| Вариант 1 Выберите правильный ответ 1.Относительная молекулярная масса Al2(SO4)3 А) 342 Б) 214 В) 278 Г) 364 2.Абсолютная масса атома марганца равна А) 86,5∙10 -27кг В) 91,3∙10 -27кг Б) 78,5∙10 -27кг Г) 61,3∙10 -27кг 3.Относительная атомная масса натрия А) 22 В) 21 Б) 23 Г) 20 4.Атомная единица массы равна: А) 1,67∙10 -27кг В) 2,99∙10 -27кг Б) 19,93∙10 -27кг Г) 1,66∙10 -27кг 5.Относительная молекулярная масса вещества – это А) сумма относительных атомных масс всех атомов, из которых состоит вещество Б) сумма абсолютных атомных масс всех атомов, из которых состоит вещество В) сумма абсолютных молекулярных масс всех атомов, из которых состоит вещество Г) сумма атомных единиц массы вещества | Вариант 2 Выберите правильный ответ 1.Относительная молекулярная масса С6Н12О6 А) 100 Б) 180 В) 150 Г) 168 2.Абсолютная масса атома золота равна А) 425,7∙10 -27кг В) 248,5∙10 -27кг Б) 327,02∙10 -27кг Г) 354,03∙10 -27кг 3.Относительная атомная масса хлора А) 35,5 В) 34 Б) 37 Г) 33 4.Абсолютная атомная масса - это А) безразмерная величина Б) отношение 1а.е.м. к массе атома углерода В) масса атома, выраженная в килограммах Г) сумма масс атомов 5. Ar (X)=ma(X)/1а.е.м. – это формула А) относительной молекулярной массы вещества Б) относительной молекулярной массы элемента В) относительной атомной массы вещества Г) относительной атомной массы элемента |
| Вариант 3 Выберите правильный ответ 1.Относительная молекулярная масса (NH4)2SO4 А) 126 В) 118 Б) 132 Г) 156 2.Абсолютная масса атома магния равна А) 55,5∙10 -27кг В) 39,84∙10 -27кг Б) 35,48∙10 -27кг Г) 40,3∙10 -27кг 3.Относительная атомная масса серы А) 36 В) 32 Б) 35 Г) 31 4.Абсолютная молекулярная масса – это А) отношение массы молекулы к 1а.е.м. Б) безразмерная величина В) сумма масс молекул Г) масса молекулы, выраженная в килограммах 5. 1а.е.м. – это А) одна атомная единица массы Б) одна абсолютная единица массы В) одна абсолютная единица молекулы Г) одна атомная единица молекулы | Вариант 4 Выберите правильный ответ 1.Относительная молекулярная масса C12H22O11 А) 342 В) 264 Б) 240 Г) 360 2.Абсолютная масса атома алюминия равна А) 45,6∙10 -27кг В) 56,91∙10 -27кг Б) 53,64∙10 -27кг Г) 44,82∙10 -27кг 3.Относительная атомная масса свинца А) 204 В) 209 Б) 207 Г) 202 4.Относительная атомная масса - это А) отношение абсолютной массы молекулы к 1/12 массы атома углерода Б) отношение относительной массы молекулы к 1/12 массы атома углерода В) отношение абсолютной массы атома к 1/12 массы атома углерода Г) отношение относительной массы атома к 1/12 массы атома углерода 5. 1/12 ma(C) – А) 1,99∙10 -27кг Б) 1,36∙10 -26кг В) 1,66∙10 -27кг Г) 1,67∙10 -26кг |
Проверочная работа. Массовая доля элемента. Молярная масса.
Задание: установите соответствие.
1. ω (в-ва) =
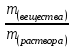
2. ω (X) =
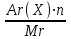 . 100%
. 100%3.
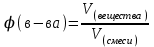
4 моль
5. массовая доля растворенного
вещества
6.
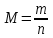
7.молярная масса
8. NA≈ 6,02. 1023моль-1
9.количество вещества
10. N = NA.n
А) формула массовой доли элемента в данном веществе
Б) физико-химическая величина, которая показывает число структурных единиц, образующих это вещество
В) формула массовой доли растворенного вещества
Г) масса одного моля вещества
Д) постоянная Авогадро
Е) формула числа молекул или атомов в определенном количестве вещества
Ё) формула молярной массы вещества
Ж) отношение массы растворенного вещества к общей массе раствора
З) формула объемной доли газообразного вещества в газовой смеси
И) количество вещества, которое содержит 6,02 . 1023 молекул этого вещества
Проверочная работа. Объёмная доля газа. Постоянная Авогадро.
| Установите соответствие: 1. ω (в-ва) = 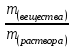 2. ω (X) = 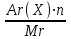 . 100% . 100%3. 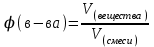 4 моль 5. массовая доля растворённого вещества 6. 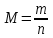 7.молярная масса 8. NA≈ 6,02. 1023моль-1 9.количество вещества 10. N = NA.n | 1 вариант А) формула массовой доли элемента в данном веществе Б) физико-химическая величина, которая показывает число структурных единиц, образующих это вещество В) формула массовой доли растворённого вещества Г) масса одного моля вещества Д) постоянная Авогадро Е) формула числа молекул или атомов в определенном количестве вещества Ё) формула молярной массы вещества Ж) отношение массы растворённого вещества к общей массе раствора З) формула объёмной доли газообразного вещества в газовой смеси И) количество вещества, которое содержит 6,02 . 1023 молекул этого вещества |
| Установите соответствие: 1. ω (в-ва) = 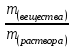 2. ω (X) = 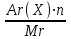 . 100% . 100%3. 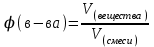 4.NA≈ 6,02. 1023моль-1 5.N = NA.n 6. 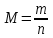 7.молярная масса 8.моль 9.количество вещества 10.массовая доля растворённого вещества | 2 вариант А) количество вещества, которое содержит 6,02 . 1023 молекул этого вещества Б) формула числа молекул или атомов в определённом количестве вещества В) формула молярной массы вещества Г) масса одного моля вещества Д) постоянная Авогадро Е) физико-химическая величина, которая показывает число структурных единиц, образующих это вещество Ё) формула массовой доли растворённого вещества Ж) отношение массы растворённого вещества к общей массе раствора З) формула объёмной доли газообразного вещества в газовой смеси И) формула массовой доли элемента в данном веществе |
Контрольная работа. Массы атомов и молекул. Массовая доля элемента.
| Вариант 1 1.Чему равна абсолютная масса атома:
2.Чему равны относительные молекулярные массы следующих веществ:
3. Чему равны массовые доли каждого элемента в следующем веществе:
4. Сколько граммов йода и спирта нужно взять для приготовления 37г 17%-го раствора йодной настойки? 5. Из 360г 23% - го раствора бромида калия (KBr) выпарили 120 мл воды. Какой стала массовая доля соли в растворе? 6.Найдите массу 15•1023 молекул кислорода О2. 7.Найдите массу 12 моль глюкозы C6H12O6. 8.Сколько молекул содержат 1,5 г водорода? 9.Какое количество вещества составляют 212 кг карбоната натрия Na2CO3? 10. В каком количестве вещества содержится 5•1023 молекул кислорода? | Вариант 2 1.Чему равна абсолютная масса атома:
2.Чему равны относительные молекулярные массы следующих веществ:
3. Чему равны массовые доли каждого элемента в следующем веществе:
4.Сколько граммов йода и спирта нужно взять для приготовления 65г 4%-го раствора йодной настойки? 5.Из 150г 17% - го раствора бромида бария (BaBr2) выпарили 10 мл воды. Какой стала массовая доля соли в растворе? 6.Найдите массу 25•1023 атомов железа Fe. 7. Найдите массу 5 моль азота N2. 8. Сколько молекул содержится в 11г углекислого газа CO2? 9.В каком количестве содержится 20 г нитрата калия KNO3? 10.Какое количество вещества составляют 35•1023 атомов золота Au? |
| Вариант 3 1.Чему равна абсолютная масса атома:
2.Чему равны относительные молекулярные массы следующих веществ:
3. Чему равны массовые доли каждого элемента в следующем веществе:
4. Сколько граммов йода и спирта нужно взять для приготовления 80г 13%-го раствора йодной настойки? 5.Из 160г 35% - го раствора хлорида бария (BaCl2) выпарили 15 мл воды. Какой стала массовая доля соли в растворе? 6.Найдите массу 9 •1023 молекул глюкозы C6H12O6. 7. Какую массу составляют 6 моль кислорода? 8.Какое число молекул содержится в 3 г кислорода? 9. Какое количество вещества составляют 5 кг глюкозы C6H12O6? 10. Какое количество вещества составляют 45•1023 молекул CO2? | Вариант 4 1.Чему равна абсолютная масса атома:
2.Чему равны относительные молекулярные массы следующих веществ:
3. Чему равны массовые доли каждого элемента в следующем веществе:
4. Сколько граммов йода и спирта нужно взять для приготовления 310г 6%-го раствора йодной настойки? 5. Из 175г 20% - го раствора сульфата калия (K2SO4) выпарили 75 мл воды. Какой стала массовая доля соли в растворе? 6.Найдите массу 50•1023 атомов меди Cu. 7.Какую массу составляют 0,8 моль железа? 8.Какое число молекул содержится в 1 г аммиака NH3? 9. В каком количестве содержится 25 г карбоната калия K2CO3? 10. Какое количество вещества составляют 15•1023 атомов серебра Ag? |
Проверочная работа. Валентность. Правило валентности.
Задание: ответьте на вопросы.
| Вариант 1 1.Чему равна валентность элемента в водородном соединении? 2.Что такое элемент с постоянной валентностью? 3.Какие элементы имеют постоянную валентность III? 4.Определите валентность элементов в следующих соединениях: N2O5, H2Te 5. Напишите формулы соединений, которые состоят из:1) алюминия и кислорода, 2) германия (IV) и кислорода. | Вариант 2 1.Чем определяется валентность? 2.Что такое элемент с переменной валентностью? 3.Какие элементы имеют постоянную валентность I? 4. Определите валентность элементов в следующих соединениях: AlCl3, Na2S 5. Напишите формулы соединений, которые состоят из:1) сурьмы (III) и кислорода, 2) фосфора (V) и кислорода. |
| Вариант 3 1.Что такое валентность? 2.Что называется бинарными соединениями? 3.Какие элементы имеют постоянную валентность II? 4. Определите валентность элементов в следующих соединениях: ZnS, Ca3N2 5.Напишите формулы соединений, которые состоят из:1) фосфора (III) и серы (II), 2) бария и кислорода. | Вариант 4 1.Как формулируется правило валентности? 2.Что такое графические формулы? 3. Какие элементы имеют постоянную валентность I? 4. Определите валентность элементов в следующих соединениях: MgBr2, Al2S3 5. Напишите формулы соединений, которые состоят из:1) натрия и кислорода, 2) марганца (VI) и кислорода. |
Проверочная работа. Степень окисления.
Задание: ответьте на вопросы.
| Вариант 1 1.Атомы каких элементов имеют отрицательные значения степени окисления? 2.Какие элементы имеют постоянную степень окисления +2? 3.Определите степень окисления каждого атома в молекулах: ZnOHNO2, Al(HSO4)3 | Вариант 2 1.Атомы каких элементов имеют положительные значения степени окисления? 2.Какие элементы имеют постоянную степень окисления -1 и -2? 3. Определите степень окисления каждого атома в молекулах: AlOH(MnO4)2, Ca(H2PO4)2 |
| Вариант 3 1.В каком состоянии атомы химических элементов могут иметь нулевое значение степени окисления? 2.Какие элементы имеют постоянную степень окисления +3? 3. Определите степень окисления каждого атома в молекулах:Ba(HCO3)2,(MgOH)2SO4 | Вариант 4 1.Что такое степень окисления? 2.Какие элементы имеют постоянную степень окисления +1? 3. Определите степень окисления каждого атома в молекулах: Sr(H2PO4)2, (ZnOH)3AsO4 |
Контрольная работа. Валентность. Степень окисления.
| 1 вариант 1.Валентность … числом … , которые …данный атом с другими атомами в молекуле. 2.Какие элементы имеют постоянную степень окисления -2? 3.Чему равна сумма степеней окисления всех атомов в веществе? 4.Напишите молекулярные формулы веществ, которые состоят из: -лития и кислорода -марганца(VI) и кислорода 5.Определите степень окисления всех атомов элементов в следующих веществах: -H2SO4 -HMnO4 6.Чему равна валентность элемента в водородном соединении? 7.Что называется валентностью? | 2 вариант 1.Степень окисления – это …… …… атомов элементов в молекуле …. вещества. 2.Какие элементы имеют постоянную валентность II? 3.Что называется графическими формулами? 4. Напишите молекулярные формулы веществ, которые состоят из: -магния и кислорода -серы(VI) и кислорода 5. Определите степень окисления всех атомов элементов в следующих веществах: -H2SO3 -H3PO4 6.Что такое элемент с постоянной валентностью? 7.С чем совпадает валентность в сложном соединении? |
| 3 вариант 1.Валентность – это…. атомов элементов, ….. определенное число химических ….. 2.Какие элементы имеют постоянную степень окисления +2? 3.Какие элементы имеют нулевое значение степени окисления? 4. Напишите молекулярные формулы веществ, которые состоят из: -алюминия и кислорода -азота(IV) и кислорода 5. Определите степень окисления всех атомов элементов в следующих веществах: -HNO3 -H2CO3 6.Как формулируется правило валентности? 7.Чем определяется валентность? | 4 вариант 1.В сложном …. степень окисления …. с…. элемента. 2.Какие элементы имеют постоянную валентность I? 3.Какие элементы имеют отрицательное значение степени окисления? 4. Напишите молекулярные формулы веществ, которые состоят из: -цинка и кислорода -хрома (VI) и кислорода 5. Определите степень окисления всех атомов элементов в следующих веществах: -HNO2 -H3PO4 6.Что такое элемент с переменной валентностью? 7.Что называется валентностью? |
Проверочная работа. Типы химических реакций.
| Вариант 1 Закончите предложения:
Ответьте на вопросы:
| Вариант 2 Закончите предложения:
Ответьте на вопросы:
|
| Вариант 3 Закончите предложения:
Ответьте на вопросы:
| Вариант 4 Закончите предложения:
Ответьте на вопросы:
|