Файл: Реферат по теме Дендримеры. Синтез и основные свойства.doc
Добавлен: 23.11.2023
Просмотров: 78
Скачиваний: 4
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Саморегуляция происходит потому, что с увеличением плотности упаковки в поверхностном слое молекулы дендримера реакционная способность концевых групп уменьшается. В то же время реакционная способность “отставших”, непрореагировавших групп в предыдущем слое остаётся высокой, в результате чего они как бы “навёрстывают упущенное”, реагируя быстрее до тех пор, пока реакционные группы на этом участке окажутся в поверхностном слое. Таким образом, стерические затруднения в поверхностном слое в случае нерегулярного роста приводят к образованию шарообразных молекул примерно одинакового размера.
Выход в зависимости от природы мономера и условий реакции составлял 80 - 90 %. Полученные продукты представляли собой вязкие жидкости с молярной массой от 6103 до 3105 в зависимости от условий реакции.
Другим примером таких систем является одностадийный синтез гиперразветвлённых полиариловых эфиров посредством термической самоконденсации 3,5-бис(триметилсилокси)бензоилхлорида (рис.7).
Выход продукта составлял 80% со средневесовой молекулярной массой от 3104 до 2105. Степень разветвления в этих системах по данным ЯМР составляла 55-60%. Полидисперсность полученных продуктов варьировалась в пределах 1.92.9 в зависимости от температуры реакции.

Рис. 4. Схема неуправляемого синтеза дендритных полиариловых эфиров.
В последних обзорах, посвящённых дендримерам, управляемый синтез стали подразделять на дивергентный и конвергентный подходы.
Описанная выше и ставшая уже классической схема синтеза дендримеров путём повторяющихся реакций наращивания слоя и снятия защиты, начинающаяся с исходного разветвляющего центра (рис. 5), получила название дивергентной. Отличительной особенностью этой схемы является быстрое увеличение числа реакционных центров, располагающихся на поверхности дендритной молекулы с возрастанием номера генерации. Это, в свою очередь, приводит к трудностям очистки конечных соединений от продуктов неполного замещения поверхностных функциональных групп, если таковые имеются в системе. Проблема очистки связана с очень малым различием молекулярных масс дендримеров с полностью прореагировавшими поверхностными группами и продуктов неполного замещения. Различие молярных масс таких соединений не превышает нескольких процентов.
Для преодоления указанного выше недостатка Фреше, а также Нинан и Миллер независимо друг от друга предложили другой подход, названный ими конвергентным методом. Если в случае дивергентного синтеза рост дендритной молекулы происходит от центра к периферии, то в данном случае, наоборот, дендример “собирается”, начиная с поверхностных групп.
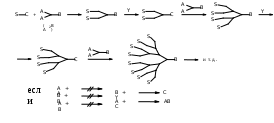
Рис. 5. Схема конвергентного синтеза дендронов.
Придерживаясь системы обозначений, введённых ранее, конвергентный рост монодендрона можно представить схемой, изображённой на рисунке 8. Стоит напомнить, что при управляемом синтезе химическая связь образуется только при взаимодействии функциональных групп А и С. Рост дендрона начинается со взаимодействия будущих поверхностных групп S с разветвлённым мономером типа А2В. Затем происходит активация образованного “димера” (перевод группы В в С) и опять взаимодействие с мономером А2В с образованием “тетрамера” и т.д. При этом, независимо от номера генерации, на каждой стадии роста дендрона количество реагирующих групп остаётся постоянным и обычно равно 2 или 3.
Таким образом получается дендрон, содержащий в своей так называемой “фокальной точке” реакционноспособную группу С или скрытую функциональность В. Для получения дендримера необходимо присоединить эти дендроны к разветвляющему центру (рис. 9).

Рис. 6. Схема получения дендримеров из моноденронов.
Следует отметить, что монодендроны можно получить и дивергентным способом, а затем их присоединить к разветвляющему центру по этой же схеме с образованием дендримера.
Как уже отмечалось выше, преимуществом конвергентного подхода является малое число реагирующих групп на каждой стадии, что, в свою очередь приводит к минимальному числу промежуточных продуктов (продуктов недозамещения). Кроме того, различия в молекулярной массе конечных, исходных и промежуточных продуктов столь велико (в 1.5 2 раза), что позволяет легко выделить целевое соединение в чистом виде.
Однако существенным недостатком данного метода являются стерические затруднения, возникающие на стадии присоединения монодендрона к разветвляющему центру. Здесь столь малое число реакционных групп (фактически единственная у монодендрона - фокальная точка) играет отрицательную роль. В реакционной системе оказывается довольно низкая концентрация реагирующих групп, активность которых ещё более снижена большим количеством “инертных” (поверхностных и др.) групп, и протекание реакции затруднено.
Учитывая рассмотренные выше преимущества и недостатки обоих подходов, следует отметить, что в последнее время наблюдается тенденция использования комбинированного подхода, заключающегося в присоединении монодендронов, полученных конвергентным методом, не к точечному разветвляющему центру, а к дендримеру генерации 2 - 3, синтезированному заранее по дивергентной схеме.
Обратимся теперь к конкретным синтетическим примерам получения регулярных дендримеров.
К настоящему времени с помощью дивергентного подхода синтезированы дендримеры на основе полиамидоаминов, полиэтилениминов, углеводородов (иптицены), полиэфиров, полиамидоспиртов (“арборолы”), полиариламинов, полисилоксанов, поликарбосиланов и многие другие.
Полисилоксановые дендримеры получают по схеме, представленной на рисунке 10. За основу здесь взята реакция взаимодействия силанолята натрия с хлорсиланом, протекающая количественно с образованием силоксановой связи. Для синтеза этих дендримеров используется трифункциональный разветвляющий центр (NC = 3) и мономеры АВ2 - типа (NB = 2). Получены регулярные структуры вплоть до генерации 8. Строение и индивидуальность конечных соединений доказаны методами ЯМР 1Н и 29Si-спектроскопии, гель-проникающей хроматографии.

Рис. 7. Схема синтеза регулярных полисилоксановых дендримеров.

Рис. 8. Схема синтеза регулярных поликарбосилановых дендримеров.
Поликарбосилановые дендримеры получают по схеме, представленной на рисунке 11. Для синтеза таких систем может быть ди-, три- или тетрафункциональный разветвляющий центр и три- или тетрафункциональные мономеры. В данном случае в качестве исходного разветвляющего центра использован тетрааллилсилан, к которому по реакции гидросилилирования присоединяют метилдихлорсилан. Хлорсилильные группы впоследствии переводят в аллильные с помощью реактива Гриньяра - аллилмагнийхлорида. Эту последовательность повторяют несколько раз до получения дендримера необходимой генерации. К настоящему времени получены поликарбосилановые дендримеры с концевыми аллильными и винильными группами вплоть до 4 генерации. Строение и индивидуальность этих соединений доказаны методами ЯМР
1Н и 29Si-спектроскопии, гель-проникающей хроматографии.
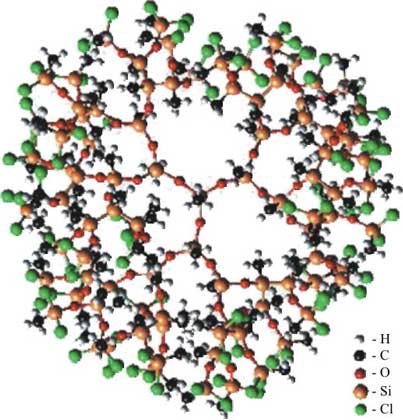
Рис.12. Дивергентная схема построения дендримера
Синтез дендримеров по этому методу был осуществлён только группами Фреше и Нинана/Миллера.
Этот подход был успешно использован для получения по крайне мере четырёх различных семейств дендримеров: полиарилэфиров, полиариленов, полиарилалкилов и поли(арил/азакраун)эфиров. Остановимся лишь на одном примере - синтезе полиарилэфирных дендримеров, предложенном Фреше.
На рисунке 13 показана схема получения тридендронов, содержащих 4, 10, 22 и 46 ароматических ядер полиариловых сложноэфирных дендримеров. Как видно из представленной схемы, выход конечного продукта с увеличением генерации с 1 по 4 падает с 98 до 25%. Это объясняется возрастанием стерических затруднений в фокальной точке монодендрона с увеличением размера макромолекулы.
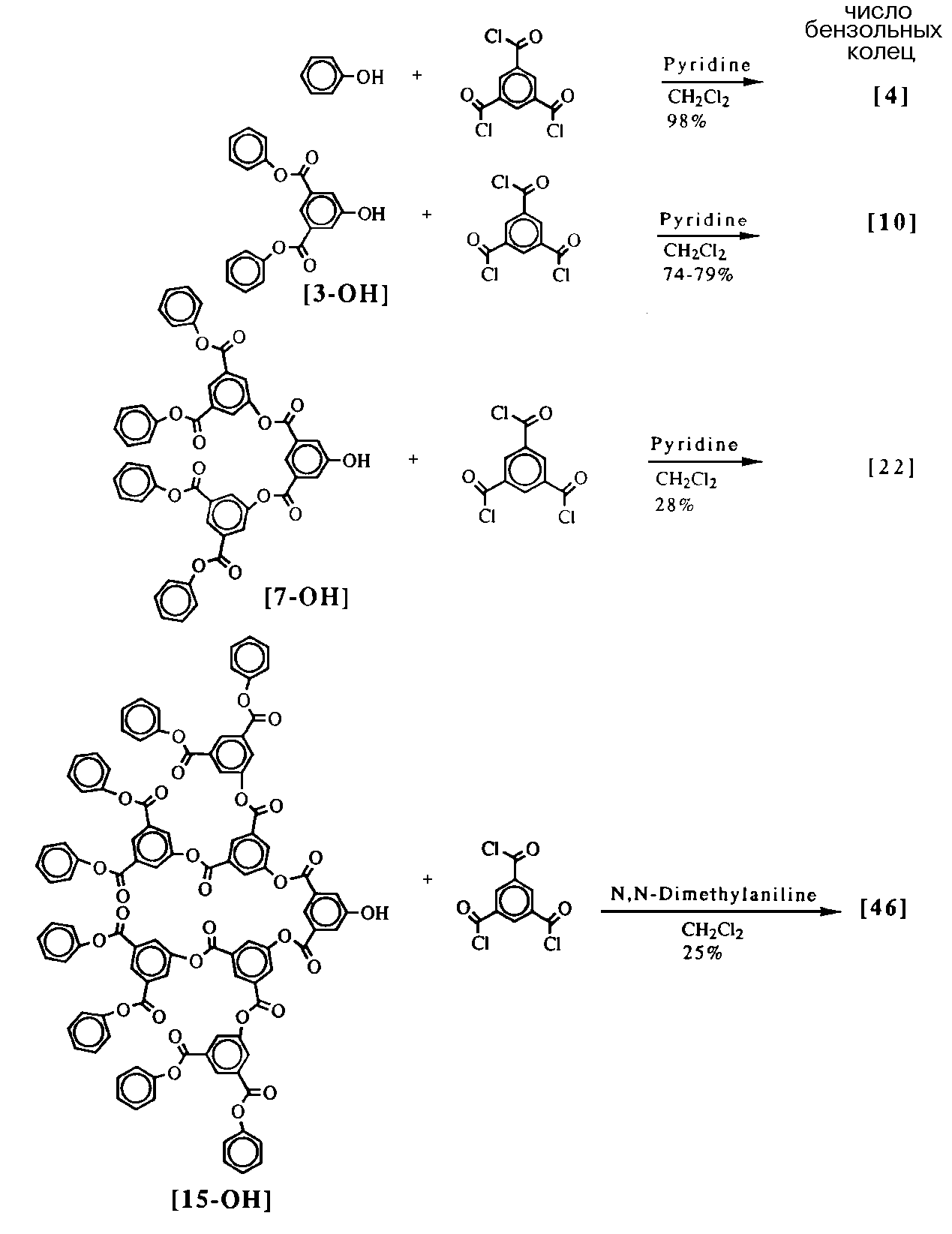
Рис. 13. Схема конвергентного синтеза полиариловых сложноэфирных дендримеров.
В работе [T.H.Morey, S.R. Turner, M. Rubinstain, J.M.J. Fréchet, C.J. Hawker, K.L.Wooley // Macromolecules, 1992, v. 25, p. 2401] Морей с соавт. изучали физические свойства полиэфирных дендримеров, полученных на основе 3,5-дигидроксибензилового спирта. Исследовались как монодендроны, так и тридендроны генераций 0 6 с молекулярной массой от 576 до 40689.
Хорошо известно, что для классических линейных полимеров, таких как, например, полистирол, с возрастанием молекулярной массы вязкость резко увеличивается в соответствии с уравнением Марка-Куна-Хаувинка []=KM, где [] - характеристическая вязкость полимера, М - средневесовая молекулярная масса, а К и - константы для данного полимера. В отличие от почти всех других макромолекул, включая даже разветвлённые и звездообразные полимеры, дендримеры не подчиняются этому соотношению после достижения определённой молекулярной массы. В случае полиэфирных дендримеров, после достижения молекулярной массы порядка пяти тысяч дальнейшее её увеличение приводит к уменьшению характеристической вязкости, как показано для полиэфирного тридендрона на рисунке 14.
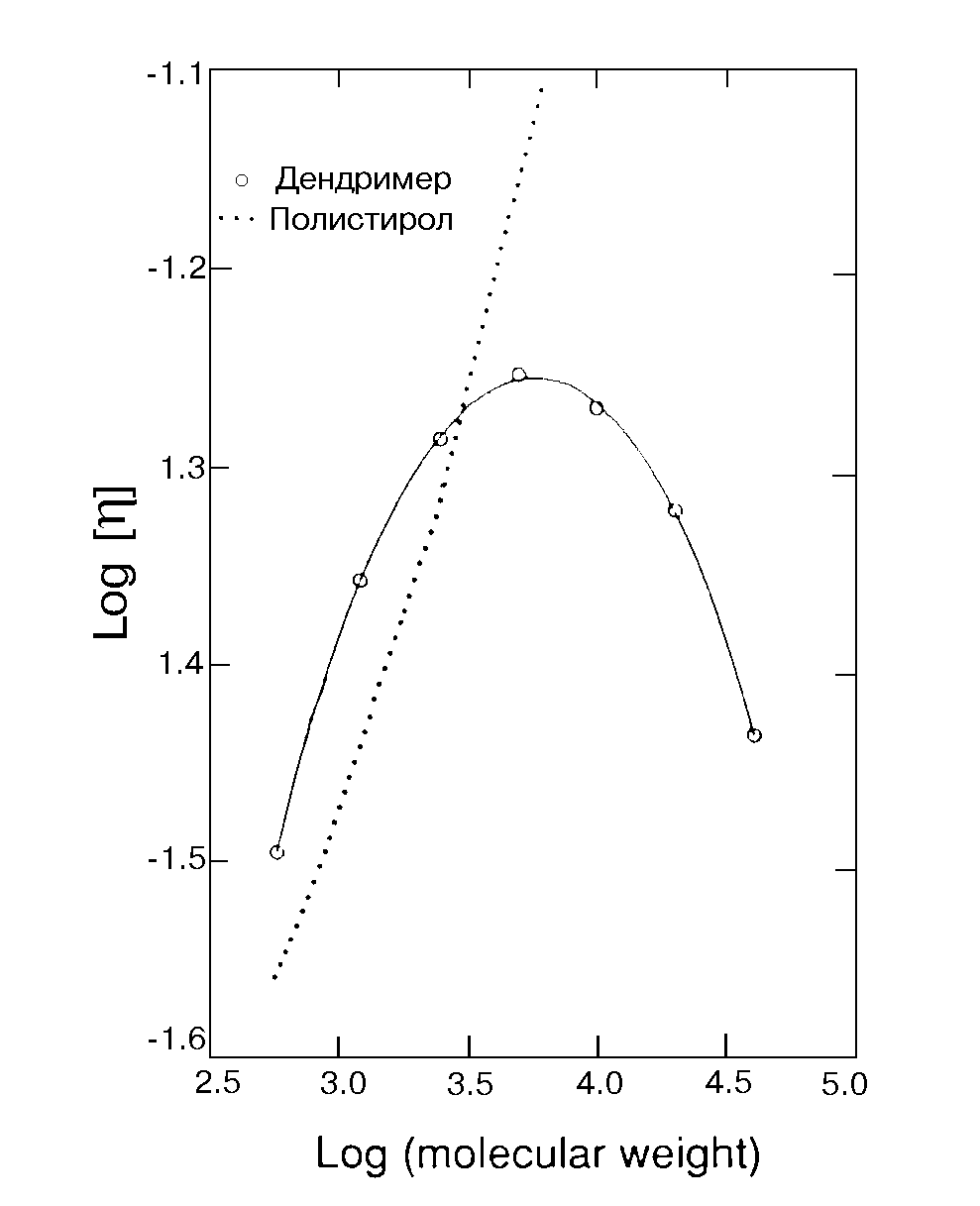
Рис. 14. Зависимость характеристической вязкости от молекулярного веса для полистирола и полиэфирных дендримеров.
Это явление можно понять, если учесть, что с ростом номера генерации объём дендритной макромолекулы увеличивается пропорционально кубу линейного размера (V=4/3 r3), в то время как её масса возрастает экспоненциально (2G-1), что не выполняется ни для каких других полимеров.
Необычные соотношения между характеристической вязкостью и молекулярным весом для дендримеров коррелирует с изменением их формы от рыхлой к глобулярной структуре с увеличением молекулярной массы . Доказательство такого изменения формы приводится в работе [C.J. Hawker, K.L.Wooley, J.M.J.Fréchet // J. Am. Chem. Soc., 1993, v. 115, p. 4375]. Здесь на примере монодендронов, к фокальной точке которых был присоединён сольватохромный зонд, изучалась зависимость максимума адсорбции max от номера генерации. При этом наблюдался излом кривой между генерациями 3 и 4, который соответствует переходу от рыхлой к глобулярной структуре. Интересно отметить, что этот переход происходит примерно при той же молекулярной массе, при которой наблюдается максимум характеристической вязкости. Такое поведение сольватохромного зонда также предполагает, что внутренняя часть дендритной макромолекулы представляет собой уникальное микроокружение. Фреше [J.M.J.Fréchet, C.J.Hawker, K.L.Wooley // J.M.S. - Pure Appl. Chem., 1994, Ser. A, v. 31, ¹ 11, pp. 1627-1645] предлагает его использовать для молекулярного катализа, систем доставки лекарств, искусственных ферментов и т.д.
Максимум имеется не только на кривой зависимости вязкости, но также и плотности и показателя преломления от номера генерации (рис. 14). Причём все эти максимумы для данных систем приходятся на одну и ту же шестую генерацию.
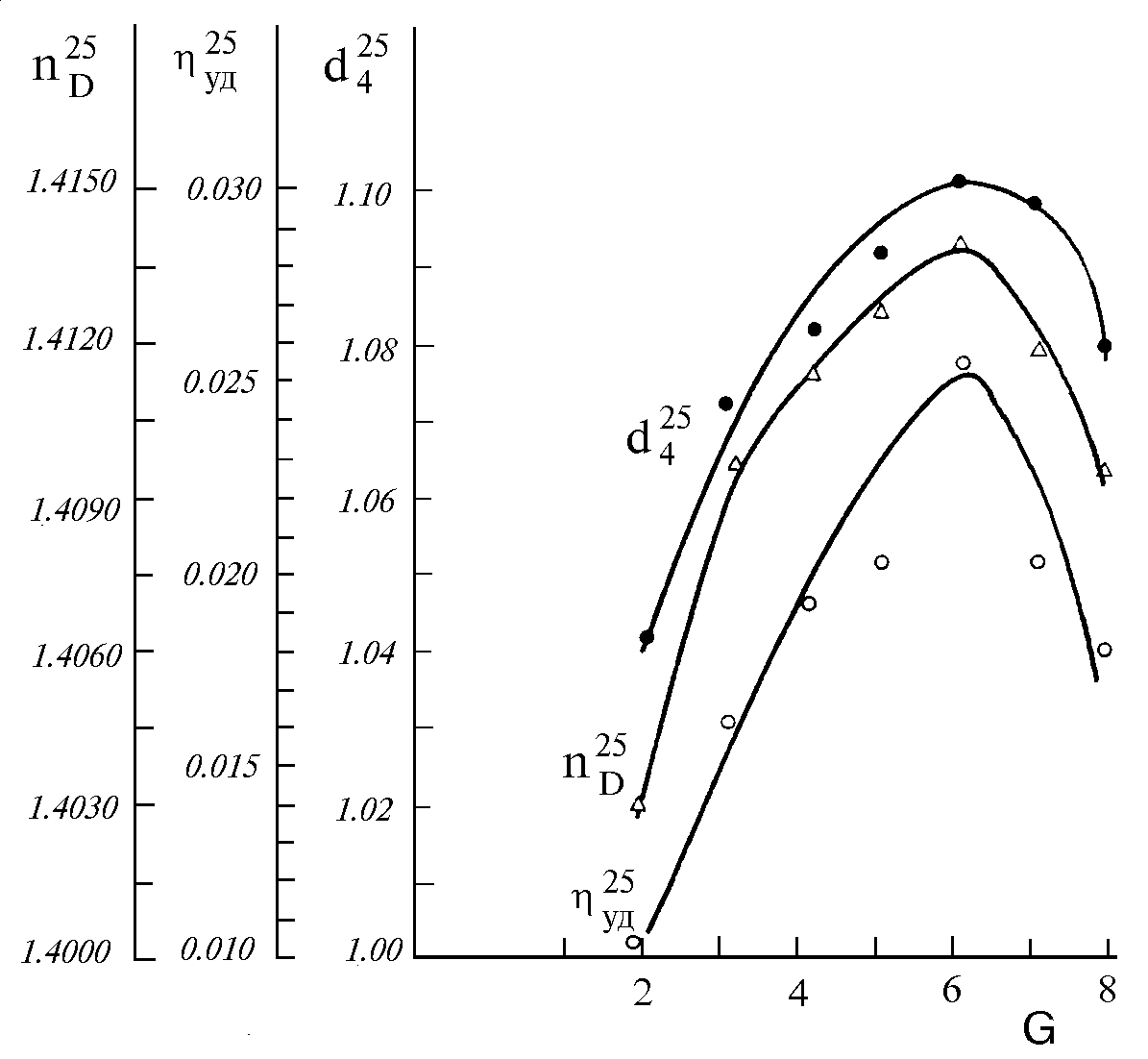
Рис. 95. Зависимость плотности (d425), удельной вязкости (уд25, 1%-ный раствор в толуоле) и показателя преломления (nD25) полиэтоксиметил-силоксановых дендримеров от номера генерации G [32].
В отличие от нетипичного поведения дендримеров, описанного выше, термические свойства дендримеров хорошо коррелируют с их линейными аналогами [J.M.J.Fréchet, C.J.Hawker, K.L.Wooley // J.M.S. - Pure Appl. Chem., 1994, Ser. A, v. 31, ¹ 11, pp. 1627-1645]. Например, изменение температуры стеклования в зависимости от молекулярного веса и количества концевых групп подчиняется модифицированной теории свободного объёма концов цепи. В работа Х. Штуца [H. Stutz // J. Polym. Sci., Part B : Polym. Phys., 1995, v. 33, p. 333-340], посвящённой температуре стеклования дендритных полимеров отмечается, что T
Выход в зависимости от природы мономера и условий реакции составлял 80 - 90 %. Полученные продукты представляли собой вязкие жидкости с молярной массой от 6103 до 3105 в зависимости от условий реакции.
Другим примером таких систем является одностадийный синтез гиперразветвлённых полиариловых эфиров посредством термической самоконденсации 3,5-бис(триметилсилокси)бензоилхлорида (рис.7).
Выход продукта составлял 80% со средневесовой молекулярной массой от 3104 до 2105. Степень разветвления в этих системах по данным ЯМР составляла 55-60%. Полидисперсность полученных продуктов варьировалась в пределах 1.92.9 в зависимости от температуры реакции.

Рис. 4. Схема неуправляемого синтеза дендритных полиариловых эфиров.
Управляемый синтез.
В последних обзорах, посвящённых дендримерам, управляемый синтез стали подразделять на дивергентный и конвергентный подходы.
Описанная выше и ставшая уже классической схема синтеза дендримеров путём повторяющихся реакций наращивания слоя и снятия защиты, начинающаяся с исходного разветвляющего центра (рис. 5), получила название дивергентной. Отличительной особенностью этой схемы является быстрое увеличение числа реакционных центров, располагающихся на поверхности дендритной молекулы с возрастанием номера генерации. Это, в свою очередь, приводит к трудностям очистки конечных соединений от продуктов неполного замещения поверхностных функциональных групп, если таковые имеются в системе. Проблема очистки связана с очень малым различием молекулярных масс дендримеров с полностью прореагировавшими поверхностными группами и продуктов неполного замещения. Различие молярных масс таких соединений не превышает нескольких процентов.
Для преодоления указанного выше недостатка Фреше, а также Нинан и Миллер независимо друг от друга предложили другой подход, названный ими конвергентным методом. Если в случае дивергентного синтеза рост дендритной молекулы происходит от центра к периферии, то в данном случае, наоборот, дендример “собирается”, начиная с поверхностных групп.

Рис. 5. Схема конвергентного синтеза дендронов.
Придерживаясь системы обозначений, введённых ранее, конвергентный рост монодендрона можно представить схемой, изображённой на рисунке 8. Стоит напомнить, что при управляемом синтезе химическая связь образуется только при взаимодействии функциональных групп А и С. Рост дендрона начинается со взаимодействия будущих поверхностных групп S с разветвлённым мономером типа А2В. Затем происходит активация образованного “димера” (перевод группы В в С) и опять взаимодействие с мономером А2В с образованием “тетрамера” и т.д. При этом, независимо от номера генерации, на каждой стадии роста дендрона количество реагирующих групп остаётся постоянным и обычно равно 2 или 3.
Таким образом получается дендрон, содержащий в своей так называемой “фокальной точке” реакционноспособную группу С или скрытую функциональность В. Для получения дендримера необходимо присоединить эти дендроны к разветвляющему центру (рис. 9).

Рис. 6. Схема получения дендримеров из моноденронов.
Следует отметить, что монодендроны можно получить и дивергентным способом, а затем их присоединить к разветвляющему центру по этой же схеме с образованием дендримера.
Как уже отмечалось выше, преимуществом конвергентного подхода является малое число реагирующих групп на каждой стадии, что, в свою очередь приводит к минимальному числу промежуточных продуктов (продуктов недозамещения). Кроме того, различия в молекулярной массе конечных, исходных и промежуточных продуктов столь велико (в 1.5 2 раза), что позволяет легко выделить целевое соединение в чистом виде.
Однако существенным недостатком данного метода являются стерические затруднения, возникающие на стадии присоединения монодендрона к разветвляющему центру. Здесь столь малое число реакционных групп (фактически единственная у монодендрона - фокальная точка) играет отрицательную роль. В реакционной системе оказывается довольно низкая концентрация реагирующих групп, активность которых ещё более снижена большим количеством “инертных” (поверхностных и др.) групп, и протекание реакции затруднено.
Учитывая рассмотренные выше преимущества и недостатки обоих подходов, следует отметить, что в последнее время наблюдается тенденция использования комбинированного подхода, заключающегося в присоединении монодендронов, полученных конвергентным методом, не к точечному разветвляющему центру, а к дендримеру генерации 2 - 3, синтезированному заранее по дивергентной схеме.
Обратимся теперь к конкретным синтетическим примерам получения регулярных дендримеров.
Дивергентный подход.
К настоящему времени с помощью дивергентного подхода синтезированы дендримеры на основе полиамидоаминов, полиэтилениминов, углеводородов (иптицены), полиэфиров, полиамидоспиртов (“арборолы”), полиариламинов, полисилоксанов, поликарбосиланов и многие другие.
Полисилоксановые дендримеры получают по схеме, представленной на рисунке 10. За основу здесь взята реакция взаимодействия силанолята натрия с хлорсиланом, протекающая количественно с образованием силоксановой связи. Для синтеза этих дендримеров используется трифункциональный разветвляющий центр (NC = 3) и мономеры АВ2 - типа (NB = 2). Получены регулярные структуры вплоть до генерации 8. Строение и индивидуальность конечных соединений доказаны методами ЯМР 1Н и 29Si-спектроскопии, гель-проникающей хроматографии.

Рис. 7. Схема синтеза регулярных полисилоксановых дендримеров.

Рис. 8. Схема синтеза регулярных поликарбосилановых дендримеров.
Поликарбосилановые дендримеры получают по схеме, представленной на рисунке 11. Для синтеза таких систем может быть ди-, три- или тетрафункциональный разветвляющий центр и три- или тетрафункциональные мономеры. В данном случае в качестве исходного разветвляющего центра использован тетрааллилсилан, к которому по реакции гидросилилирования присоединяют метилдихлорсилан. Хлорсилильные группы впоследствии переводят в аллильные с помощью реактива Гриньяра - аллилмагнийхлорида. Эту последовательность повторяют несколько раз до получения дендримера необходимой генерации. К настоящему времени получены поликарбосилановые дендримеры с концевыми аллильными и винильными группами вплоть до 4 генерации. Строение и индивидуальность этих соединений доказаны методами ЯМР
1Н и 29Si-спектроскопии, гель-проникающей хроматографии.

Рис.12. Дивергентная схема построения дендримера
Конвергентный подход.
Синтез дендримеров по этому методу был осуществлён только группами Фреше и Нинана/Миллера.
Этот подход был успешно использован для получения по крайне мере четырёх различных семейств дендримеров: полиарилэфиров, полиариленов, полиарилалкилов и поли(арил/азакраун)эфиров. Остановимся лишь на одном примере - синтезе полиарилэфирных дендримеров, предложенном Фреше.
На рисунке 13 показана схема получения тридендронов, содержащих 4, 10, 22 и 46 ароматических ядер полиариловых сложноэфирных дендримеров. Как видно из представленной схемы, выход конечного продукта с увеличением генерации с 1 по 4 падает с 98 до 25%. Это объясняется возрастанием стерических затруднений в фокальной точке монодендрона с увеличением размера макромолекулы.

Рис. 13. Схема конвергентного синтеза полиариловых сложноэфирных дендримеров.
Особенности физических свойств денримеров как следствие их необычной супрамолекулярной архитектуры
В работе [T.H.Morey, S.R. Turner, M. Rubinstain, J.M.J. Fréchet, C.J. Hawker, K.L.Wooley // Macromolecules, 1992, v. 25, p. 2401] Морей с соавт. изучали физические свойства полиэфирных дендримеров, полученных на основе 3,5-дигидроксибензилового спирта. Исследовались как монодендроны, так и тридендроны генераций 0 6 с молекулярной массой от 576 до 40689.
Хорошо известно, что для классических линейных полимеров, таких как, например, полистирол, с возрастанием молекулярной массы вязкость резко увеличивается в соответствии с уравнением Марка-Куна-Хаувинка []=KM, где [] - характеристическая вязкость полимера, М - средневесовая молекулярная масса, а К и - константы для данного полимера. В отличие от почти всех других макромолекул, включая даже разветвлённые и звездообразные полимеры, дендримеры не подчиняются этому соотношению после достижения определённой молекулярной массы. В случае полиэфирных дендримеров, после достижения молекулярной массы порядка пяти тысяч дальнейшее её увеличение приводит к уменьшению характеристической вязкости, как показано для полиэфирного тридендрона на рисунке 14.

Рис. 14. Зависимость характеристической вязкости от молекулярного веса для полистирола и полиэфирных дендримеров.
Это явление можно понять, если учесть, что с ростом номера генерации объём дендритной макромолекулы увеличивается пропорционально кубу линейного размера (V=4/3 r3), в то время как её масса возрастает экспоненциально (2G-1), что не выполняется ни для каких других полимеров.
Необычные соотношения между характеристической вязкостью и молекулярным весом для дендримеров коррелирует с изменением их формы от рыхлой к глобулярной структуре с увеличением молекулярной массы . Доказательство такого изменения формы приводится в работе [C.J. Hawker, K.L.Wooley, J.M.J.Fréchet // J. Am. Chem. Soc., 1993, v. 115, p. 4375]. Здесь на примере монодендронов, к фокальной точке которых был присоединён сольватохромный зонд, изучалась зависимость максимума адсорбции max от номера генерации. При этом наблюдался излом кривой между генерациями 3 и 4, который соответствует переходу от рыхлой к глобулярной структуре. Интересно отметить, что этот переход происходит примерно при той же молекулярной массе, при которой наблюдается максимум характеристической вязкости. Такое поведение сольватохромного зонда также предполагает, что внутренняя часть дендритной макромолекулы представляет собой уникальное микроокружение. Фреше [J.M.J.Fréchet, C.J.Hawker, K.L.Wooley // J.M.S. - Pure Appl. Chem., 1994, Ser. A, v. 31, ¹ 11, pp. 1627-1645] предлагает его использовать для молекулярного катализа, систем доставки лекарств, искусственных ферментов и т.д.
Максимум имеется не только на кривой зависимости вязкости, но также и плотности и показателя преломления от номера генерации (рис. 14). Причём все эти максимумы для данных систем приходятся на одну и ту же шестую генерацию.

Рис. 95. Зависимость плотности (d425), удельной вязкости (уд25, 1%-ный раствор в толуоле) и показателя преломления (nD25) полиэтоксиметил-силоксановых дендримеров от номера генерации G [32].
В отличие от нетипичного поведения дендримеров, описанного выше, термические свойства дендримеров хорошо коррелируют с их линейными аналогами [J.M.J.Fréchet, C.J.Hawker, K.L.Wooley // J.M.S. - Pure Appl. Chem., 1994, Ser. A, v. 31, ¹ 11, pp. 1627-1645]. Например, изменение температуры стеклования в зависимости от молекулярного веса и количества концевых групп подчиняется модифицированной теории свободного объёма концов цепи. В работа Х. Штуца [H. Stutz // J. Polym. Sci., Part B : Polym. Phys., 1995, v. 33, p. 333-340], посвящённой температуре стеклования дендритных полимеров отмечается, что T