ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 29.11.2023
Просмотров: 369
Скачиваний: 2
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
б и 163, б, где длины стрелок показывают, какая часть света рассеивается в том или ином направлении. Диффузно отражающие поверхности могут различаться также и по коэффициенту отражения, который для таких поверхностей обычно называют альбедо. Так, белая бумага для рисования имеет альбедо около 0,70—0,80. Очень высокое альбедо — около 0,95 — имеют поверхности, покрытые окисью магния (белый порошок, получающийся при сжигании металлического магния). Наоборот, очень малым альбедо обладает черный бархат — от 0,01 до 0,002.
При наблюдении земной поверхности с самолета и особенно при аэрофотосъемке большое значение имеет альбедо земных покровов и его зависимость от цвета (длины волны). Различные почвы имеют альбедо sot 0,2 до 0,4, причем большие значения соответствуют области оранжево-красного цвета; пески мало отражают (около 0,1) в фиолетовой области, особенно важной при фотосъемке, но их альбедо в красной части повышается до 0,5. Трава и листья имеют альбедо до 0,50 в желто-зеленой части (особенно к осени); очень велико альбедо снега, достигающее 0,85 для всех цветов.
64. Спектральный состав света различных источников. Спектры и спектральные закономерности.
Спектральный состав света различных источников.
Опытами Ньютона было установлено, что солнечный свет имеет сложный характер. Подобным же образом, т. е. анализируя состав света при помощи призмы, можно убедиться, что свет большинства других источников (лампа накаливания, дуговой фонарь и т. д.) имеет такой же характер. Сравнивая спектры этих светящихся тел, обнаружим, что соответственные участки спектров обладают различной яркостью, т. е. в различных спектрах энергия распределена по-разному. Еще надежнее удостовериться в этом можно, если исследовать спектры при помощи термоэлемента (см. § 149).
Для обычных источников эти различия в спектре не очень значительны, однако их можно без труда обнаружить. Наш глаз даже без помощи спектрального аппарата обнаруживает различия в качестве белого света, даваемого этими источниками. Так, свет свечи кажется желтоватым или даже красноватым по сравнению с лампой накаливания, а эта последняя заметно желтее, чем солнечный свет.
Еще значительнее различия, если источником света вместо раскаленного тела служит трубка, наполненная газом, светящимся под действием электрического разряда. Такие трубки употребляются в настоящее время для светящихся надписей или освещения улиц. Некоторые из этих
газоразрядных ламп дают ярко желтый (натриевые лампы) или красный (неоновые лампы) свет, другие светятся беловатым светом (ртутные), ясно отличным по оттенку от солнечного. Спектральные исследования света подобных источников показывают, что в их спектре имеются только отдельные более или менее узкие цветные участки.
В настоящее время научились изготовлять газоразрядные лампы, свет которых имеет спектральный состав, очень близкий к солнечному. Такие лампы получили название ламп дневного света (см. § 186).
Если исследовать свет солнца или дугового фонаря, профильтрованный через цветное стекло, то он окажется заметно отличным от первоначального. Глаз оценит этот свет как цветной, а спектральное разложение обнаружит, что в спектре его отсутствуют или очень слабы более или менее значительные участки спектра источника.
Спектральные закономерности. Линейчатый спектр атома представляет собой совокупность большого числа линий, разбросанных по всему спектру без всякого видимого порядка. Однако внимательное изучение спектров показало, что расположение линий следует определенным закономерностям. Яснее всего, конечно,
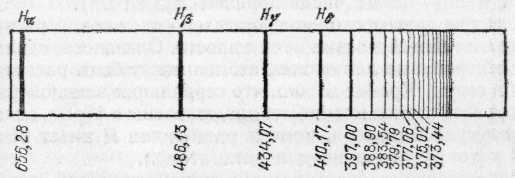
Рис. 326. Линейчатый спектр водорода (серия Бальмера, длины волн в нанометрах). H, Н, Н и H — обозначения первых четырех линий серии, лежащих в видимой области спектра
эти закономерности выступают на сравнительно простых спектрах, характерных для простых атомов. Впервые такая закономерность была установлена для спектра водорода,
изображенного на рис. 326.
В 1885 г. швейцарский физик и математик Иоганн Якоб Бальмер (1825—1898) установил, что частоты отдельных
линий водорода выражаются простой формулой:
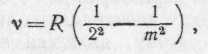
где означает частоту света, т. е. число волн, испускаемых в единицу времени, R— называемая постоянной Ридберга величина, равная 3,28984•1015 с-1, и m— целое число. Если задавать для т значения 3, 4, 5 и т. д., то получаются значения, очень хорошо совпадающие с частотами последовательных линий спектра водорода. Совокупность этих линий составляет
серию Бальмера.
В дальнейшем было обнаружено, что в спектре водорода еще имеются многочисленные спектральные линии, которые также составляют серии, подобные серии Бальмера.
Частоты этих линий могут быть представлены формулами
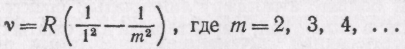 (серия Лаймана),
(серия Лаймана),
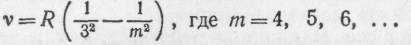 (серия Пашена),
(серия Пашена),
причем Rимеет то же самое числовое значение, что и в формуле Бальмера. Таким образом, все водородные серии можно объединить одной формулой:
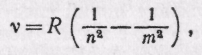
где nи m— целые числа, причем mn+1 *).
Спектры других атомов значительно сложнее, и распределение их линий в серии не так просто. Оказалось, однако, что спектральные линии всех атомов могут быть распределены в серии. Крайне важно, что сериальные закономерности для всех атомов могут быть представлены в форме, подобной формуле Бальмера, причем постоянная Rимеет почти одно и то же значение для всех атомов.
Существование спектральных закономерностей, общих для всех атомов, указывало несомненно на глубокую связь этих закономерностей с основными чертами атомной структуры. Действительно, датский физик, создатель квантовой теории атома Нильс Бор (1885—1962) в 1913 г. нашел ключ к пониманию этих закономерностей, установив в то же время основы современной теории атома (см. гл. XXII).
65. Спектральные аппараты.
Спектральные аппараты. Свечение тел тесно связано с процессами, происходящими в атомах и молекулах. Поэтому исследование свечения явилось важным средством для уяснения строения молекул и атомов.
Существенные различия в характере свечения устанавливаются при изучении спектров светящихся тел. Для получения спектров используется дифракционная решетка или
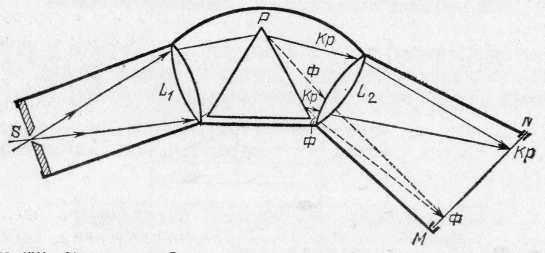
Рис.321. Схема устройства спектрографа: S — щель, L1 — объектив коллиматора, Р — призма, L2 — объектив камеры,
MN — матовое стекло или фотопластинка
чаще призма. Принцип получения спектра при помощи призмы изложен в § 160. Для того чтобы спектр был возможно более четким, т. е. чтобы различные спектральные области хорошо разделялись между собой, спектральному аппарату придается более сложное, чем указано в § 160, устройство, схематически изображенное на рис. 321.
Левая часть аппарата — коллиматор SL1 — состоит из узкой щели S, расположенной в главной фокальной плоскости объектива L1;благодаря этому свет, упавший на щель, выходит из коллиматора параллельным пучком и падает на призму. Из призмы он также выходит
406
параллельным пучком. Но так как лучи разной длины волны (разного цвета) отклоняются призмой на разные углы (дисперсия), то из призмы выходят параллельные пучки разного направления; благодаря этому свет собирается вторым объективом L2 в различных точках его фокальной плоскости MN. В этой плоскости получаются, следовательно, изображения щели S, но так, что изображения, соответствующие разным длинам волн, приходятся на разные места плоскости MN. Расположив в плоскости MNматовое стекло или фотографическую пластинку, мы получим на ней четкое изображение спектра. Если свет, падающий на щель S, представляет собой смесь нескольких монохроматических пучков, то спектр имеет вид отдельных изображений щели в разных длинах волн, т. е. имеет вид отдельных узких линий, разделенных темными промежутками. Если на щель падает белый свет, то все отдельные изображения щели сливаются в цветную полосу.
Аппараты, в которых спектр изображается на фотопластинке, носят название спектрографов. Иногда вместо камеры L2MNпомещают зрительную трубу и наблюдают спектр глазом. В этих случаях спектральный аппарат принято называть спектроскопом. Призма изготовляется из стекла, обладающего значительной дисперсией, либо из кварца, флюорита или каменной соли, если спектрограф предназначен для работы в ультрафиолетовой или инфракрасной частях спектра. Из соответствующих материалов делают и объективы.
§ 173. Типы спектров испускания. Направив на щель спектрографа свет от солнца, лампы накаливания, свечи и т. д., мы получим спектры, имеющие вид сплошной полоски, в которой представлены все длины волн, идущие непрерывной чередой. Такие спектры называются сплошными или непрерывными.
Иной вид имеет спектр, если в качестве источника света использовать светящиеся газы. Направим, например, на спектрограф свет газоразрядной лампы, в которой светится пар ртути. Наблюдаемый спектр имеет вид, изображенный на рис. 322. Он состоит из отдельных резких линий, представляющих собой изображение щели спектрографа в отдельных длинах волн. Каждая линия представляет по существу узкий спектральный интервал, охватывающий некоторый набор длин волн; но интервал этот так узок, что его можно практически считать соответст-

Рис. 322. Спектр пара ртути (длины волн — в ангстремах)

Рис. 323. Небольшой участок спектра железа (от 4143 до 4236 Å)
вующим одной определенной длине волны. Приведенный на рис. 322 в качестве примера спектр ртути характерен для свечения газов или паров. Такие спектры принято называть линейчатыми. Разнообразные пары или газы могут давать спектры, отличающиеся положением спектральных линий (т. е. их длиной волны), а также числом их и распределением по спектру. Спектр пара ртути сравнительно беден линиями; наоборот, в спектре пара железа, например, насчитывается несколько тысяч отдельных спектральных линий (рис. 323), распределенных по видимой и ультрафиолетовой областям спектра.

Рис. 324. Спектр пара иода
При изучении спектров паров или газов наблюдаются также спектры, состоящие из отдельных полос, разделенных темными промежутками. Некоторые из этих полос при более тщательном исследовании оказываются состоящими из очень большого числа отдельных линий, другие же представляют собой действительно сплошные полоски. Такого типа спектры принято называть
При наблюдении земной поверхности с самолета и особенно при аэрофотосъемке большое значение имеет альбедо земных покровов и его зависимость от цвета (длины волны). Различные почвы имеют альбедо sot 0,2 до 0,4, причем большие значения соответствуют области оранжево-красного цвета; пески мало отражают (около 0,1) в фиолетовой области, особенно важной при фотосъемке, но их альбедо в красной части повышается до 0,5. Трава и листья имеют альбедо до 0,50 в желто-зеленой части (особенно к осени); очень велико альбедо снега, достигающее 0,85 для всех цветов.
64. Спектральный состав света различных источников. Спектры и спектральные закономерности.
Спектральный состав света различных источников.
Опытами Ньютона было установлено, что солнечный свет имеет сложный характер. Подобным же образом, т. е. анализируя состав света при помощи призмы, можно убедиться, что свет большинства других источников (лампа накаливания, дуговой фонарь и т. д.) имеет такой же характер. Сравнивая спектры этих светящихся тел, обнаружим, что соответственные участки спектров обладают различной яркостью, т. е. в различных спектрах энергия распределена по-разному. Еще надежнее удостовериться в этом можно, если исследовать спектры при помощи термоэлемента (см. § 149).
Для обычных источников эти различия в спектре не очень значительны, однако их можно без труда обнаружить. Наш глаз даже без помощи спектрального аппарата обнаруживает различия в качестве белого света, даваемого этими источниками. Так, свет свечи кажется желтоватым или даже красноватым по сравнению с лампой накаливания, а эта последняя заметно желтее, чем солнечный свет.
Еще значительнее различия, если источником света вместо раскаленного тела служит трубка, наполненная газом, светящимся под действием электрического разряда. Такие трубки употребляются в настоящее время для светящихся надписей или освещения улиц. Некоторые из этих
газоразрядных ламп дают ярко желтый (натриевые лампы) или красный (неоновые лампы) свет, другие светятся беловатым светом (ртутные), ясно отличным по оттенку от солнечного. Спектральные исследования света подобных источников показывают, что в их спектре имеются только отдельные более или менее узкие цветные участки.
В настоящее время научились изготовлять газоразрядные лампы, свет которых имеет спектральный состав, очень близкий к солнечному. Такие лампы получили название ламп дневного света (см. § 186).
Если исследовать свет солнца или дугового фонаря, профильтрованный через цветное стекло, то он окажется заметно отличным от первоначального. Глаз оценит этот свет как цветной, а спектральное разложение обнаружит, что в спектре его отсутствуют или очень слабы более или менее значительные участки спектра источника.
Спектральные закономерности. Линейчатый спектр атома представляет собой совокупность большого числа линий, разбросанных по всему спектру без всякого видимого порядка. Однако внимательное изучение спектров показало, что расположение линий следует определенным закономерностям. Яснее всего, конечно,

Рис. 326. Линейчатый спектр водорода (серия Бальмера, длины волн в нанометрах). H, Н, Н и H — обозначения первых четырех линий серии, лежащих в видимой области спектра
эти закономерности выступают на сравнительно простых спектрах, характерных для простых атомов. Впервые такая закономерность была установлена для спектра водорода,
изображенного на рис. 326.
В 1885 г. швейцарский физик и математик Иоганн Якоб Бальмер (1825—1898) установил, что частоты отдельных
линий водорода выражаются простой формулой:
где означает частоту света, т. е. число волн, испускаемых в единицу времени, R— называемая постоянной Ридберга величина, равная 3,28984•1015 с-1, и m— целое число. Если задавать для т значения 3, 4, 5 и т. д., то получаются значения, очень хорошо совпадающие с частотами последовательных линий спектра водорода. Совокупность этих линий составляет
серию Бальмера.
В дальнейшем было обнаружено, что в спектре водорода еще имеются многочисленные спектральные линии, которые также составляют серии, подобные серии Бальмера.
Частоты этих линий могут быть представлены формулами
причем Rимеет то же самое числовое значение, что и в формуле Бальмера. Таким образом, все водородные серии можно объединить одной формулой:
где nи m— целые числа, причем mn+1 *).
Спектры других атомов значительно сложнее, и распределение их линий в серии не так просто. Оказалось, однако, что спектральные линии всех атомов могут быть распределены в серии. Крайне важно, что сериальные закономерности для всех атомов могут быть представлены в форме, подобной формуле Бальмера, причем постоянная Rимеет почти одно и то же значение для всех атомов.
Существование спектральных закономерностей, общих для всех атомов, указывало несомненно на глубокую связь этих закономерностей с основными чертами атомной структуры. Действительно, датский физик, создатель квантовой теории атома Нильс Бор (1885—1962) в 1913 г. нашел ключ к пониманию этих закономерностей, установив в то же время основы современной теории атома (см. гл. XXII).
65. Спектральные аппараты.
Спектральные аппараты. Свечение тел тесно связано с процессами, происходящими в атомах и молекулах. Поэтому исследование свечения явилось важным средством для уяснения строения молекул и атомов.
Существенные различия в характере свечения устанавливаются при изучении спектров светящихся тел. Для получения спектров используется дифракционная решетка или

Рис.321. Схема устройства спектрографа: S — щель, L1 — объектив коллиматора, Р — призма, L2 — объектив камеры,
MN — матовое стекло или фотопластинка
чаще призма. Принцип получения спектра при помощи призмы изложен в § 160. Для того чтобы спектр был возможно более четким, т. е. чтобы различные спектральные области хорошо разделялись между собой, спектральному аппарату придается более сложное, чем указано в § 160, устройство, схематически изображенное на рис. 321.
Левая часть аппарата — коллиматор SL1 — состоит из узкой щели S, расположенной в главной фокальной плоскости объектива L1;благодаря этому свет, упавший на щель, выходит из коллиматора параллельным пучком и падает на призму. Из призмы он также выходит
406
параллельным пучком. Но так как лучи разной длины волны (разного цвета) отклоняются призмой на разные углы (дисперсия), то из призмы выходят параллельные пучки разного направления; благодаря этому свет собирается вторым объективом L2 в различных точках его фокальной плоскости MN. В этой плоскости получаются, следовательно, изображения щели S, но так, что изображения, соответствующие разным длинам волн, приходятся на разные места плоскости MN. Расположив в плоскости MNматовое стекло или фотографическую пластинку, мы получим на ней четкое изображение спектра. Если свет, падающий на щель S, представляет собой смесь нескольких монохроматических пучков, то спектр имеет вид отдельных изображений щели в разных длинах волн, т. е. имеет вид отдельных узких линий, разделенных темными промежутками. Если на щель падает белый свет, то все отдельные изображения щели сливаются в цветную полосу.
Аппараты, в которых спектр изображается на фотопластинке, носят название спектрографов. Иногда вместо камеры L2MNпомещают зрительную трубу и наблюдают спектр глазом. В этих случаях спектральный аппарат принято называть спектроскопом. Призма изготовляется из стекла, обладающего значительной дисперсией, либо из кварца, флюорита или каменной соли, если спектрограф предназначен для работы в ультрафиолетовой или инфракрасной частях спектра. Из соответствующих материалов делают и объективы.
§ 173. Типы спектров испускания. Направив на щель спектрографа свет от солнца, лампы накаливания, свечи и т. д., мы получим спектры, имеющие вид сплошной полоски, в которой представлены все длины волн, идущие непрерывной чередой. Такие спектры называются сплошными или непрерывными.
Иной вид имеет спектр, если в качестве источника света использовать светящиеся газы. Направим, например, на спектрограф свет газоразрядной лампы, в которой светится пар ртути. Наблюдаемый спектр имеет вид, изображенный на рис. 322. Он состоит из отдельных резких линий, представляющих собой изображение щели спектрографа в отдельных длинах волн. Каждая линия представляет по существу узкий спектральный интервал, охватывающий некоторый набор длин волн; но интервал этот так узок, что его можно практически считать соответст-

Рис. 322. Спектр пара ртути (длины волн — в ангстремах)

Рис. 323. Небольшой участок спектра железа (от 4143 до 4236 Å)
вующим одной определенной длине волны. Приведенный на рис. 322 в качестве примера спектр ртути характерен для свечения газов или паров. Такие спектры принято называть линейчатыми. Разнообразные пары или газы могут давать спектры, отличающиеся положением спектральных линий (т. е. их длиной волны), а также числом их и распределением по спектру. Спектр пара ртути сравнительно беден линиями; наоборот, в спектре пара железа, например, насчитывается несколько тысяч отдельных спектральных линий (рис. 323), распределенных по видимой и ультрафиолетовой областям спектра.

Рис. 324. Спектр пара иода
При изучении спектров паров или газов наблюдаются также спектры, состоящие из отдельных полос, разделенных темными промежутками. Некоторые из этих полос при более тщательном исследовании оказываются состоящими из очень большого числа отдельных линий, другие же представляют собой действительно сплошные полоски. Такого типа спектры принято называть