Файл: Zантn 5302 Заманауи аналитикалы химияны теориялы негіздері пнінен Дрістер жинаы шымкент, 2023 растырушылар философия докторы (PhD) х.. к., Шертаева Н. Т. Заманауи аналитикалы химияны теориялы негіздері.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 30.11.2023
Просмотров: 283
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Электромагниттік сәулелену мен сәулеленуге кері электромагниттік сәулеленудің затпен жұтылуын зерттей отырып, талданатын заттың құрамы туралы қандай ақпарат алуға болады, соны толығырақ анықтап қарайық. Осы үдерістердің сандық сипаттамасы болып зерттелетін заттардың шығарылу және жұтылу спектрлері есептеледі.
Шығару спектрі — сәулешығарудың осы сауле жиілігі бойынша таралу қарқындылығы. Жұтылу спектрі — жұтылған сәуленің жиілік бойынша таралу қарқындылығы. Денелердің шығару және жұтылу спектрлерінің түрлері көптеген факторларға байланысты. Шығару спектрі сәуле түсетін заттың құрамымен, оның агрегаттық жағдайымен, температурасымен, шоғырлануымен анықталады. Жұтылу спектрі де солай зерттелетін заттың құрамына, оның агрегаттық жағдайына, температурасына, шоғырлануына, бұдан басқа, денеге түсетін сәуленің спектральді құрамына және жұтылу жүретін заттың қабатының қалыңдығына байланысты болады.
Шығару және жұтылу спектрлерін зерттеудегі тәжірибе жарқын және күтпеген заңдылықтардың ашылуына алып келді. Сөйтсе, барлық атомдық спектрлер сызықты,немесе үзік-үзік: қарқындылықтың жиілік бойынша таралуы I(v) шығару сәулесі үшін де, жұтылу сәулесі үшін де қарқындылықтың биік шыңдарының, тар сызықтарының жиынтығын құрайды екен, және олардың араларындағы қарқындылық өте аз. Қарқындылық шыңдары спектрлік сызықтар деп аталады.
«Спектрдегі сызықтардың орналасуы» термині жиі қолданылады. Ол осы спектрдегі шың сәйкес келетін жиілікпен анықталады.
Сызықты спектрлеркелесі қасиеттерге ие:
■ бір ғана химиялық элемент үшін спектрлік сызықтардың орналасуы шығару спектрі үшін де жұтылу спектрі үшін де біркелкі және температураға тәуелді емес;
■ әртүрлі сызықтардың біркелкі қарқындылығы температураға тәуелді, ал жұтылу спектрлері үшін тағы да жұтылатын сәуленің спектрлік құрамына байланысты;
■ спектрлік сызықтардың әртүрлі элементтер спектрлерінде орналасуы әрқилы;
■ спектрлік сызықтардың орналасуы атомдардың молекулаларға қосылуында өзгереді;
■ заттың қойылу-сұйылу жағдайына ауысуы сызықты спектрлердің үздіксіз спектрлерге айналуына әкеледі.
Әрбір химиялық элементтің шығару және жұтылу спектрлерінде бір қарағанда орналасуларында ешқандай тәртіп байқалмайтын, өте көп сызықтар бар. Дегенмен, көптеген зерттеушілердің бақылауларының нәтижесінде сутегі атомының барлық шығару немесе жұтылу спектрлерінің сызықтарының жиілігі қарапайым формуламен сипатталатынын анықтауға қол жеткізілді (И. Я. Бальмер, 1825—1898):
ν = RH(n1-2 – n2-2) 1
қай жерде RH — Ридберг тұрақтысы (И.Р.Ридберг, 1854— 1919); n1 = 1,2, 3, ...; n2 = n1 + 1, n1 + 2, n1 + 3, ....
n1 = 1, aл n2 = n = 2, 3, 4, ... болғанда төмендегі формула түрінде көрсетуге болады:
ν=ῡΩ =RH (1 − 1 )1
????
Екі жиіліктің айырмасы үшін
νpq =ῡp -ῡq1,
яғни, әрбір сутегі атомының спектрлі жиілігі (8.11) –ге сәйкес келетін ῡn жиынтығынан екі жиіліктің айырмасы ретінде өрнектеледі.
Одан әргі зерттеулер көрсеткендей, (8.10) ара салмағы кез келген атомдардың спектрлері үшін әділ. Кез келген атомның шығару немесе жұтылу спектрі үшін мынадай жиіліктер жиынтығын сайлауға болады ῡ1,ῡ2,..., бұл жерде әрбір спектрлі сызықтардың жиілігі жиынтықтағы екі жиіліктің айырмасы болып есептеледі. Ритцтің (В.Ритц, 1878— 1909) комбинациялық қағидасының мәні осында. ῡ1,ῡ2,... жиіліктері спектрлі термдер деп аталады.
Ритцтің қағидаларынан көретініміз, бақыланып жатқан спектрлік жиіліктердің арасындағы қарапайым байланыстар, мысалға, мыналар ν31 = ν3 – ν1 = (ν3 -ν2 ) + (ν2 – ν1) = ν32 + ν21. (8.13)
Бұл байланыстар барлық зерттелген атомдық спектрлерде бақыланған.
Ритцтің қағидаларының шығу тегі түсініксіз болды және классикалық физикамен қарама-қайшылықта болды. Бұл көзқарасқа сәйкес, ядроның айналасындағы электрондар барлық жиіліктерде сәуле түсіруі қажет, яғни электромагниттік толқындарды үзік-үзік сызықты спектрлі құраммен емес, үздіксіз спектрлі құраммен шығаруы қажет.
Ритц қағидасына 1913 ж. Н.Бор (1885—1962) электромагниттік сәулелену кванттары мен атомның энергетикалық спектрі туралы түсініктерді біріктіре отырып түсінік берді.
Физикалық жүйенің энергетикалық спектрі деп жүйеде бар барлық қуаттың ықтималды мәндерінің жиынтығын айтады. Егер спектр үзік- үзік сызықтан болса, онда қуаттың әрбір мәні энергетикалық деңгей деп аталады, немесе, жай қысқартылған түрде жүйе деңгейі деп аталады. Ең төменгі деңгей негізгі, ал басқалары – қоздырылған болып аталады.
Бор Планктың ара салмағын пайдалана отырып әрбір спектрлі терммен vn қуатты Еn1 байланыстырды:
En=hvn =ℎ/2????????n=hωn1
және атомның энергетикалық спектрі қуаттың тек осы мәндерімен сипатталады деп болжады. Басқа сөзбен айтқанда, атом тек қарғымалы түрде қозады, бұған қоса қуаттың кез келген шектеулі мәнінің қозуы атомның екі спектрлік термдерінің айырмашылығына пропорционалды Планк тұрақтысының коэффициентіне тең деп сендірілді.
Бордың идеясын қабылдаумен және Ритцтің сәулелену кванттарының өмір сүру қағидасын ескере отырып, атомдардың шығару және жұтылу спектрлері туралы тәжірибелік деректердің жинақталған тұжырымдарына қарап, қарапайым ғана қуатты сақтау заңының нәтижесі екенін ұғамыз. Умножив Л-ға көбейтіп және оны оң жаққа шығарсақ, En = Люп, онда атомның шығару және жұтылу жиілігі үшін Бордың мына формуласын аламыз:
hω = hωn2 – hωn1 = En – Em1 қай жерде n2 = n и n1 = m. Бордың формуласының мағынасы түсінікті:
Еп деңгейінен Ет < Еп деңгейіне өткенде атом ю жиілігімен сәулелену квантын шығарады. Кері ауысқанда атом электромагниттік сәулеленудің квантын жұтады.
Бордың формуласының мазмұны екі іргелі бекітуді көрсетеді:
1) атомның энергетикалық спектрі дискретті;
2) атомдық сәуле шығарудың жиілігі атомдық энергетикалық деңгейлермен байланысты.
Энергетикалық деңгейлерді көлденең сызықтармен бейнелеу мақұлданған. Кез келген сызықтардың ара қашықтығы қозу энергиясының мүмкін мәндеріне пропорционалды.
Дискретті спектр тек қана шектеулі кеңістікті жүйеде пайда болады. Мысалы, атомнан бөлініп шыққан электрон спектрі үздіксіз болады. Осы атомнан бөлінген оң зарядты ионның спектрі де өзгереді. Егер атомдар атомдар өзара әрекеттесіп және мәселен, қосатомдық молекула түзсе, онда бұл шектеулі кеңістікті жүйеде қозғалыстың екі қосымша түрі: ядролардың тербелісі және молекулалардың айналуы пайда болады.
Молекуланың электронды жағдайы сонымен қатар, оны құрайтын әрбір жеке атомның электронды жағдайымен салыстырғанда өзгереді. Мұндай молекулалы жүйенің энергиясын энергиялар сомасы түрінде елестетуге болады.
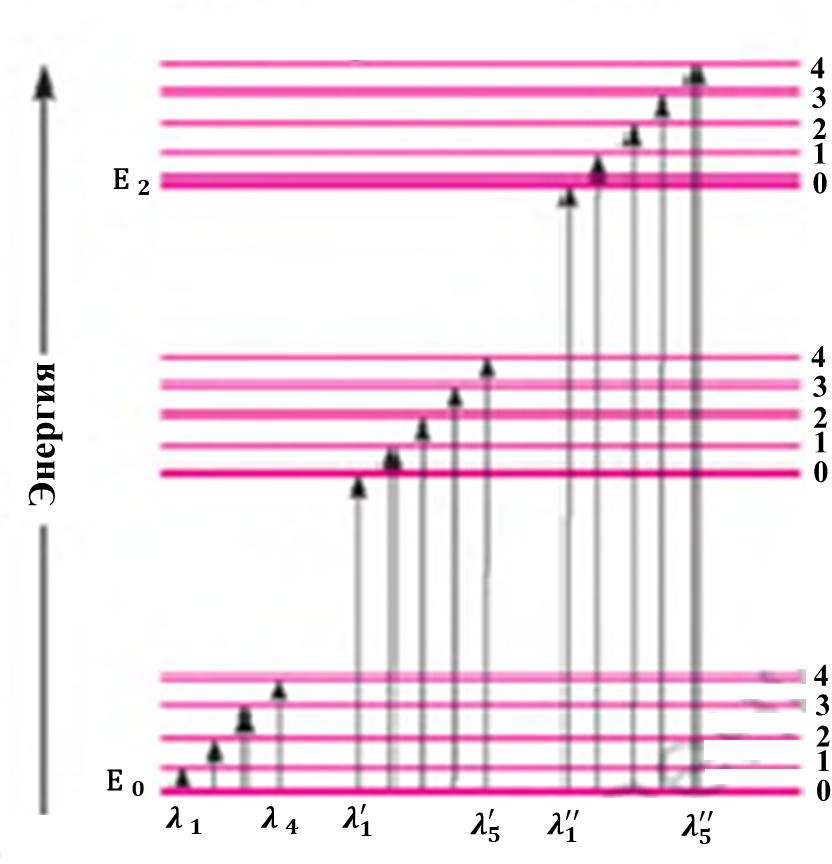
1-сурет Энергетикалық деңгейлер схемасы. Жоғарыға бағытталған нұсқарлар жүйенің қозуына сәйкес келеді; 0, 1, 2, 3, 4 — тербеліс деңгейлері
Қозғалыстың үш түрі — электронды, тербелмелі және айналмалы:
Е = Еэл + Етер + Еай.
Бұл энергияның жуықталған бөлінуі мүмкін, өйткені ЕэЛ: Екол: Еэл: Етер : Еай ≈104:102:1.
Сонымен, атоммен салыстырғанда молекулаларда екі дискретті спектрлер – тербелмелі және айналмалы спектрлер пайда болады. Молекуланың ядроларының тиімді шамадағы қозғалысымен келісілген, электронды қосалқы жүйемен құрылған тербелмелі өткелдер қуаты электронды деңгейлер арасындағы өткелдер қуатына қарағанда көп аз.
Бұл өткелдер инфрақызыл аумаққа сәйкес келеді, ал айналмалылар - қысқатолқындыға.
Мұндай молекуланың ішкі энергиясының электронды, тербелмелі, айналмалы энергияға жуықтап бөлінуі осы қосатомдық молекулалардың спектрін сипаттау үшін 1927 ж. энергияның бөлінуін енгізген зерттеушілердің атымен Борнның жуықтаулары деген атауға ие — Оппенгеймера (М.Борн, 1882—1970; Р. Оппенгеймер, 1904— 1967).
3.Спектральды талдау құралдарының компоненттері
Спектрлік аналитикалық аспаптардың көп бөлігі бес негізгі құрамдастардан тұрады (сур 2):
1) сәуле шығарудың тұрақты көзі;
2) қажетті ұзындықтағы толқынның бөліну жүйесін;
3) заттекке арнап бір немесе одан көп кювет;
4) сәуле шығару энергиясын өлшенетін белгіге айналдыратын сәуле шығару детекторы, әдетте электрлік;
5) белгіні көрсететін және (немесе) белгіні оқитын процессор, мысалға, осциллограф, сандық талдағыш немесе басқа дыбыс жазушы құрылғы.
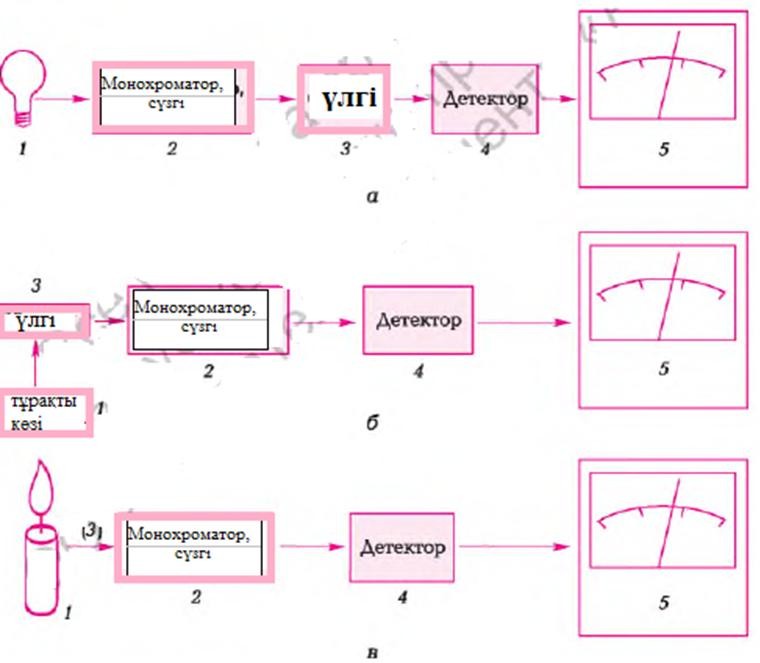
2- сурет Жұтылу (а), люминесценттік (б) және эмиссиялық (в) спектроскопияның аспаптарының негізгі блоктары
Сәулелердің жұтылу спектрін өлшеу үшін көзден тура үлгі арқылы толқын ұзындығының селекторына өтеді.
Люминесценцияның спектрін өлшеу үшін көз әдетте спектрі түскен сәуленің тік бұрышымен өлшенетін люминисценция пайда болу үшін үлгіні қоздырады.
Эмиссиялық спектрлердің пайда болуы үшін сәуле шығарудың сыртқы қоздырушы көзі қажет емес: үлгі сәуле шығару эмиттері боп саналады. Эмиссиялық спектроскопияда үлгі электрлік доғаның, ұшқынды қуатсызданудың, жоғары жиілікті индукциялы қуатсызданудың немесе жалынның әсеріне түседі, бұл үлгіні төмен температуралы плазма күйіне ауыстырады. Осылайша, бір уақытта үлгіні қамтамасыз етеді және оның сипаттамасындағы сәуле шығарушы эмиссияны қоздырады.
Оптикалық материалдардың мөлдірлігі. Кюветтер, сәуле өтетін терезелер, линзалар, жарық сүзгілері және басқа спектрлік аспаптардың оптикалық элементтері, әлбетте, қолданылатын толқындар ұзындықтарының аумағында мөлдір болуы тиіс. Бұл үшін арнайы оптикалық материалдар қолданылады. Әдеттегі силикатты шыны спектрдің көрінетін аумағында мөлдір. Дегенмен сәуленің ультракүлгін аумағын өлшеу үшін, мысалға, балқытылған кварцтан немесе литийдің фторидінен алынған оптикалық элементтер қажет. ИҚ-диапазонда жұмыс істеу үшін оптикалық элементтерді NaCl, AgCl, KBr –ден және кейбір арнайы материалдардан дайындайды.
Сәуленің шығу көздері. Ең алдымен, жеңіл детектрлеу үшін және спектрлік аналитикалық белгілерді өлшеу үшін олар айтарлықтай қуатты болуы керек. Осы мақсатта тұрақты және монохроматикалық сәуле беретін лазерлерді қолданады. Осы уақытқа дейін қолданылып келген сәуле шығарудың арзан көзі болып әртүрлі типтегі шамдар болып келеді. Кейбір көздердің сипаттамалары 1. - кестеде келтірілген.
Толқындардың қажетті ұзындығын бөлу үшін жарық сүзгілері, монохроматорлар, дифракциялық торлар қолданылады. Монохроматор мен дифракциялық торларды қолдану шамамен анықталатын спектрлік аспаптардың айыру қабілетін жақсартуға көмектеседі
R = λ/∆λ,
қай жерде λ — сыртқы сәуле шығару көзінің толқын ұзындығы; ∆λ — сызықтың жартылай ені (3 – сур.).
Радиацияның детекторлары. Қазіргі заманғы құрылғыларда фотоматтандырғыштар радиациялық детекторлар, фотодиодтар ретінде пайдаланылады кремнийлі сызғыштар, жылу детекторлары, қуат байланысымен екіөлшемдік талдауыштар - CCD (Charge Coupled Оеу1ее)-камералар қолданылады.
| 1. - кесте Молекулалық спектрлік талдауда қолданылатын сәуле шығару көздері | ||
| Көздер | ג, пм | Әдіс |
| גe-шамдар | 0,25 — 0,60 | Люминесценттік талдау |
| H, D-шамдар | 0,16 — 0,38 | УК-молекулалық абсорбция |
| W/I-шамдар | 0,24 — 2,50 | УК, көрінетін, ИҚ-молекулалық абсорб- ция |
| W-шамдар | 0,35 — 2,20 | Көрінетін және жақын ИҚ-молекулалық жұтылу аумағы |
| Ni/Cr-шамдар | 0,75 — 20,0 | MҚ-жұтылу |
| «Globar» | 1,20 — 40,0 | MҚ-жұтылу |
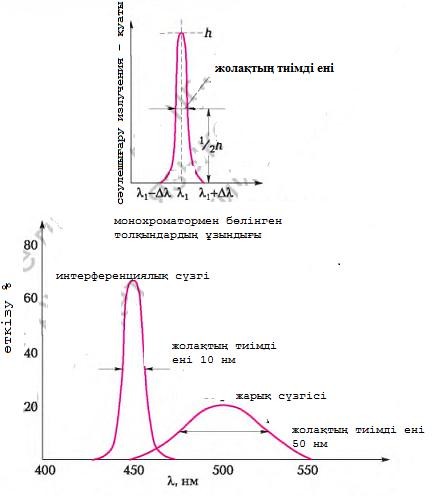
3– сур. Монохроматордан бөлінген сәуленің кіреберіс саңылауды монохроматикалық сәулемен біркелкі жарықтандырудағы толқындардың ұзындығы бойымен таралу қуаттылығы немесе қарқындылығы (аппараттық функция)
Фотокөбейткіштерді есептемегенде, әдеттегідей, бұл құрылғылар ақпарат жинау және талдау жүйесімен – көпарналы талдауыштары бар көпарналы детекторлар болып табылады. Өзімен байланысқан компьютермен пайдалы өлшем белгісі бөлінуі мүмкін (мысалға, бөтен белгілер мен шуды сүзгілеудің жақсы өңделген әдісін қолдану арқылы).