Файл: Zантn 5302 Заманауи аналитикалы химияны теориялы негіздері пнінен Дрістер жинаы шымкент, 2023 растырушылар философия докторы (PhD) х.. к., Шертаева Н. Т. Заманауи аналитикалы химияны теориялы негіздері.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 30.11.2023
Просмотров: 285
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
3. Тотығу-қалпына келтіру титрлеуі (оксидиметрия)
Осы үлгідегі титриметрлі әдістерде, электрондардың бір бөлшектен (молекулалар, иондар) екінші бөлшекке ауысуымен қатар жүретін, қышқылдану-қалпына келтіретін реакцияларды қолданады. Титранты ретінде тотықсыздандырғыш ертіндісін қолданылатын титрлеу әдісін тәжірибеде көп қолданылуда. Осындай титрдеу әдісін кейде оксидиметрия деп атайды.
Тотығу-тотықсыздандыру реакцияларын қолдану арқылы титриметриялық әдістерді есептеу үшін молярлық шоғырлану мен баламалар массын білу қажет.
Тотығу-тотықсыздандыру реакцияларындағы (молекулалар, атомдар, иондар) заттардың баламасы— бір қабылданған немесе берілген электронға келетін шартты бөлшек.
Зат баламасының молярлық массасы — осы зат баламасының бір молінің массасы.
Тотығу-тотықсыздандыру реакцияларын жүргізуге негізделген титриметриялық әдістерде, титрлеудің соуңғы нүктесін анықтау үшін әртүрлі тәсілдер қолданылады:
■ Титрлеу бояуы немесе титрленетін зат бояуының жоғылуы және пайда болуытва;
■ Ерекше және тотығу-тотықсыздану индикатор;
■ Аспаптық әдіс (мысалы, потенциометриялық титрлеу; 7- тар.қар.).
Сонымен, KMnO4 ерітіндісін титрлеу кезінде, титрлеудің аяқталуы артылған титранның тек бір артық тамшысының пайда болған кездегі қызғыл бояудың пайда болуымен анықталады.
Ерекше индикатор ретінде атап көрсетеміз, мысалы, күңгірт-көк иодты қосылыс түзетін крахмал.
Тотығу-тотықсыздандыру (редокс-) индикаторлары— негізінен, тотығу мен тотықсануға қабілетті органикалық қосылыстар. Олардың тотыққан және тотықсызданған пішіндері әртүрлі бояуда болады.
Бұл үлгідегі индикаторлар, мысалы, дифениламин, фенилантранил және салицил қышқылдар болып саналады.
-
Тұндыру титрлеуі
Тұндыру әдісімен титрлеу нашар еритін қосылыстар түзетін реакцияларға негізделген. Бұл реакциялар бөлме температурасында жеткілікті тез және іс жүзінде қайтымсыз өтеді. Тұндыру реакцияларының көптігіне қарамастан, тұндырып титрлеу кең таралмады. Тұндыру тәсілімен титрлеу әдістерінің ең кең тарағаны аргентометрия және меркуриметрия, сондай-ақ роданидометрия және цианометрияны атап көрсетуге болады. Тұндырып титрлеудің басқа әдістері сирегірек қолданылады, себебі олар үшін эквиваленнтік нүктесін белгілеп алатын сенімді индикаторлар табылған жоқ.
Тұнбалық әдісімен титрлеудің кең тараған түрі меркуриметрия. Мөлшерлік анализдің бұл әдістері сынаптың (I) галогендермен және басқа да аниондармен нашар еритін қосылыс түзу реакцияларына негізделген:
Стехиометрияны ескере отырып, сынап галогенидтерінің ерігіштігі, күміс галогенидтеріне қарағанда жоғары екендігін атап өту керек. Бұған қарамастан, меркуриметрия біртіндеп аргентометрияны ығыстырып шығаруда, себебі сынап асыл металдарға жатпайды.
Адсорбциялық индикатор ретінде 1,5-дифенилкарбозид немесе дифенилкарбазон, содай-ақ темір (III) тиоцианатты комплексі қолданылады.
Меркуриметриялық титрлеудің қисығын есептеу берілген аргентометриялық титрлеуді есептеуге ұқсас.
Темір (III) тиоцианатты комплекс бар болғанда титрлеу кезінде осы комплекстердің мына әрекеттесуге байланысты түссізденуі жүзеге асады.
Адсорбциялық индикаторлар.
Лекция 10. Талдаудың электрохимиялық әдістері
1. Талдау әдістерінің жалпы сипаттамалары және оның жіктелімі
2.Талдаудың потенциометриялық әдістері
1. Талдау әдістерінің жалпы сипаттамалары және оның жіктелімі
Электрохимиялық талдау әдістері, тағы да электроаналитикалық немесе элекрталдау деп аталатын, электродтар мен электродты кеңістік арасында болатын құбылыстарға негізделген.
Электрохмиялық әдістерде аналитикалық белгі ретінде, параметрлерді, анықталатын компоненттің концентрациясымен (белсенділігімен) байланысты көлемі қолданылады.
Мысалы, электрод, тоқ күші, электр саны, электр өткізгіштік, ом кдергісі, сыйымдылығы әлеуетінің алуан түрлігі.
Электрохимиялық талдау әдісін мына жағдайдарда кеңінен қолданалады
■органаникалық және органикалық емес заттарды алудың әртүрлі техологиялық үдерістерін аналитикалық бақылау үшін;
■экологиялық және биологиялық нысандарды талдау кезінде;
■физикалық-химиялық зерттеулерде, мысалы, органикаоық қосылыстардың құрылу реакицсяның кинетикасы, кешенді түзу үдерістері.
Заманауи электрохимиялық талдау әдістері төмендегідей сипатталады:
■100 (кулонометриядан) 10-10% (инверсиялық әдістерге дейін) зерттелетін компоненттердің анықталатын құрамының кең ауқымымен;
■Қатысты төмен құны бар аппаратура мен анықтауларды орындау қарапайымдылығымен үйлесудегі таңдаушылық және экспрестік.
■Көптеген осы әдістерді автоматтандыруға және компьютерлендіру жеңіл.
Электрохимиялық әдістердің- электрохимиялық ұяшықтың өлшенетін параметрлері бойынша анағұрлым қарапайым топтастырылуы. Белгілері бойынша мына түрлерге бөлінеді: потенциометрия, кулонометря, электрогравиметрия, вольтамперметрия, кондуктометрия және т.б. Көрсетілген әдістерді екі топқа бөлуге болады:
■ Электроды реакцияның өтуіне негізделген (потенциометрия, кулонометрия, электрогравиметрия, вольтамперометрия);
■Электродты реакцияның өтуіне байланысты емес (кондуктометрия, диэлектрометрия).
Бірінші топтың ішінде төменде аталған әдістерді бөліп көрсетуге болады:
■Өтетін электродты реакциялар ерітінді көлемінде және электродты қабатта анықталатын заттар концентрациясында мүлде өзгермейді;
■Электродты реакцияның болуы, электродты ерітінді қабаты кезінде (вольтоамперметрия) анақталатын зат концентрацияның елеулі өзгеруіне әкеліп соқтырады;
■ Электрды реакцияға ерітіндідегі заттың барлығы қатысады (кулонометрия).
Талдауды орындау жолы бойынша төменде аталған әдістер ажыратылады:
■тікелей (потенциометрия, кулонометрия, вольтамперометрия, кондуктометрия және т.б.);
■жанама (электрохимиялық немесе басқа да титрлеудің соңғы нүктесімен электрохимиялық әдістер)—потенциометрикалық, кулонометрикалық, амперометрикалық, кондуктометрикалық титрлеу.
2.Талдаудың потенциометриялық әдістері
Потенциометрикалық титрлеуді ток болмағанда (I = 0) немесе оның аз мөлшерінде (IФ 0), әртүрлі химиялық реакцияларды қолдана отырып жүргізеді: қықылды-негізгі, тұнбалы, кешен түзуші және тотығу-тотықсыздану. Бұл реакцияларға, индикатор қолданылатны титрленген әдістерде талаптар қойылады. Елеулі потенциалдың өзгеруі (ЭДС) баламалық нүкте тұсында байқалады, сонымен бірге баламалық нүктеге дейін потенциал бір индикаторлы жартылай реакциямен, ал оған жеткенде-екіншімен анықталады. Титрлеу секірісі көлеміне бір қатар факторлар әсер етеді: заттар концентрациясы, реакциялар тепе-теңдік тұрақтысы, баламалық нүктені анықтау кемшілігі және т.б.
Қышқылды-негізгі реакциялар жүргізу кезінде, инкаторлық ретінде рН-функциясы бар кез келген электрод қолданылады. Бәрінен бұрын осы мақсатта шыны электрод қолданылады. Индикаторлық электрод тотығу-тотықсыздандыру реакцияларны қолдану кезінде,
платина электроды беріледі. Галогенді-иондарды анықтау кезінде тұнбалы титрлеуде күміс электродты қолданады.
Егер электрод анықталатын иондар немесе титрант иондарына сезімтал болса, ион іріктемелі электродтарды титрлеу үшін индикаторлық ретінде қолдануға болады. Потенциометриялық титрлеуде титрлеудің соңғы нүктесін (ТСН) әртүрлі тәсілдермен табады. ТСН сызба түрінде табу үшін интегралды түрде немесе бірінші немесе екінші туынды түрінде қисық сызықты титрлеуді қолданады ( 1-сурет). Қисық сызықты титрлеу, екі реакцияда да электрондар саны тепе-тең болған кезде, баламалық нүктесіне қатысты симметриялы (тотығу және тотықсыздандыру).
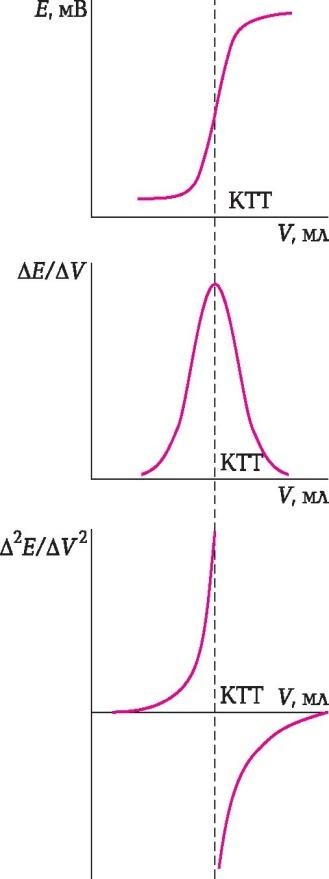
1-сурет. Титрлеудің соңғы нүктесін табудың сызбалық тәсілдері
ТСН табудың басқа да тәсілдері –берілген потенциалға дейін титрлеу қолданылады.
Сонымен бірге, алдын ала қисық сызықты титрлеудің соңғы нүктесінде потенциалды бағалавйды. Көбінесе бұл титрлеу нұсқасын автоматты потенциалды титраторларда қолданады.
Ток болмағанда, (I = 0) қайтарымды редокс-жұптармен жұмыс кезіндегі потенциометрлік титрлеу жұмыс электродының тұрақсыз потенциалының салдарынан қиындатылады. Бұл жағдайда, титрлеуді аз токта (I Ф 0) жүргізеді. Бұл үдерісті жеделдетуге және ДЕ потенциалдарының өлшенетін айырмасының тұрақиы көлемін алуға мүмкіндік береді. Бір индикаторлы электрод (салыстырмалы электродпен бірге) немесе екі полярланған электрод (электросыз