Файл: Методические рекомендации по применению практикума по биологии.docx
Добавлен: 09.01.2024
Просмотров: 352
Скачиваний: 3
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Приложение. Модификации образуют вариационный ряд изменчивости признака в пределах нормы реакции от наименьшей до наибольшей величины. Причина вариаций связана с воздействием различных условий на развитие признака.
Для определения предела изменчивости признака рассчитывают частоту встречаемости каждой варианты и строят вариационную кривую - графическое выражение характера изменчивости признака. Средние члены вариационного ряда встречаются чаще, что соответствует среднему значению признака.
Средняя величина выраженности признака высчитывается по формуле:
-
сумма
М = (P×V)P – частота встречаемости
nV - варианта
n – общее число особей; M – среднее значение модификации
Приложения
Приложение 1 (к практической работе №1)
Десять крупнейших достижений десятилетия в биологии и медицине Версия независимого эксперта
Новые высокопроизводительные методы секвенирования ДНК – «цена» генома падает
Синтетическая биология и синтетическая геномика – как просто стать Богом
Лекарства от старения – путь к «химическому» бессмертию?
Использование стволовых клеток в медицине – ждем революцию
Древняя ДНК – от неандертальца до чумной бактерии
Нейропротезирование – человек или киборг?
Нелинейная оптика в микроскопии – увидеть невидимое
Дизайнерские белки – эволюция в пробирке
Персонализированная медицина – получаем генные паспорта
МикроРНК – о чем молчал геном
Новые высокопроизводительные методы секвенирования ДНК – «цена» генома падает
Один из основателей знаменитой фирмы «Intel» Г. Мур в свое время сформулировал эмпирический закон, который до сих пор выполняется: производительность компьютеров будет удваиваться каждые два года. Производительность секвенаторов ДНК, с помощью которых проводят расшифровку нуклеотидных последовательностей ДНК и РНК, растет даже быстрее чем по «закону Мура». Соответственно, падает стоимость чтения геномов.
Так, затраты на проведение работ по проекту «Геном человека», который завершился в 2000 г., составили 13 млрд долларов. Появившиеся позднее новые массовые технологии секвенирования были основаны на параллельном анализе множества фрагментов ДНК (сначала – в микролунках, а сейчас – в миллионах микроскопических капель). В результате, например, расшифровка генома знаменитого биолога Д. Уотсона, одного из авторов открытия структуры ДНК, которая в 2007 г. обошлась в 2 млн долларов, всего через два года «стоила» уже 100 тыс. долларов.
В 2011 г. фирма «Ion torrent», предложившая новый метод секвенирования на основе измерения концентрации ионов водорода, выделяющихся при работе ферментов ДНК-полимераз, прочитала геном самого Мура. И хотя стоимость этой работы не оглашалась, создатели новой технологии обещают, что чтение любого генома человека не должно в будущем превышать 1 тыс. долларов. А их конкуренты – создатели еще одной новой технологии, секвенирования ДНК в нанопорах, уже в нынешнем году представили прототип устройства, на котором, потратив несколько тысяч долларов, можно секвенировать геном человека за 15 минут.
Синтетическая биология и синтетическая геномика – как просто стать Богом
Информация, накопленная за полвека развития молекулярной биологии, сегодня позволяет ученым создавать живые системы, никогда не существовавшие в природе. Как оказалось, сделать это совсем нетрудно, особенно если начать с чего-то уже известного и ограничить свои притязания такими несложными организмами, как бактерии.

Фраза «Hello, world!», изображенная на этой чашке Петри, получена с помощью «колироида» – ранее не существовавшей в природе генетически усовершенствованной модификации кишечной палочки. Фото UT/UCSF
В наши дни в США даже проводится специальный конкурс iGEM (International Genetically Engineered Machine), в котором студенческие команды соревнуются в том, кто сможет придумать наиболее интересную модификацию обычных бактериальных штаммов, используя набор стандартных генов. Например, пересадив в широко известную кишечную палочку (
Escherichia coli) набор из одиннадцати определенных генов, можно заставить колонии этих бактерий, растущие ровным слоем на чашке Петри, стабильно менять цвет там, где на них падает освещение. В результате можно получить их своеобразные «фотографии» с разрешением, равным размеру бактерии, т. е. около 1 мкм. Создатели этой системы дали ей имя «Колироид», скрестив видовое имя бактерии и название знаменитой фирмы «Поляроид».
В этой области есть и свои мегапроекты. Так, в фирме одного из отцов геномики К. Вентера был синтезирован из отдельных нуклеотидов геном бактерии-микоплазмы, который не похож ни на один из существующих микоплазменных геномов. Эту ДНК заключили в «готовую» бактериальную оболочку убитой микоплазмы и получили работающий, т.е. живой организм с полностью синтетическим геномом.
Лекарства от старения – путь к «химическому» бессмертию?
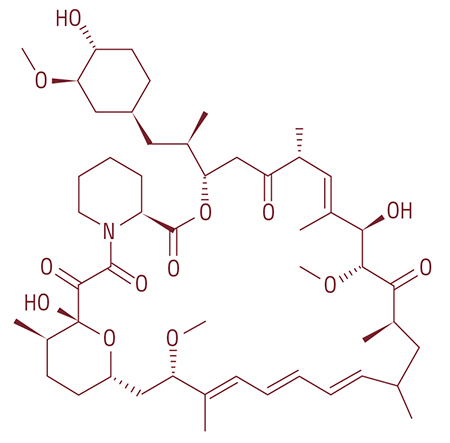
Почва под знаменитыми статуями с о. Пасхи послужила источником для антибиотика рапамицина – потенциального «лекарства против старости»
Сколько ни пытались за тысячи лет создать панацею от старения, легендарное средство Макропулоса так и осталось недосягаемым. Но и в этом, казалось бы, фантастическом направлении появляются подвижки.
Так, в начале прошедшего десятилетия большой бум в обществе произвел ресвератрол – вещество, выделенное из кожуры ягод красного винограда. Сначала с его помощью удалось значительно продлить жизнь клеткам дрожжей, а потом – и многоклеточным животным, микроскопическим червям-нематодам, плодовым мушкам-дрозофилам и даже аквариумным рыбкам. Потом внимание специалистов привлек рапамицин – антибиотик, впервые выделенный из почвенных бактерий-стрептомицетов с о. Пасхи. С его помощью удалось продлить жизнь не только клеткам дрожжей, но даже лабораторным мышам, которые жили на 10—15 % дольше.
Сами по себе эти препараты вряд ли будут широко применять для продления жизни: тот же рапамицин, к примеру, подавляет иммунную систему и повышает риск инфекционных заболеваний. Однако сейчас ведутся активные исследования механизмов действия этих и подобных веществ. И если это удастся, то мечта о безопасных лекарственных средствах для продления жизни вполне может стать явью.
Использование стволовых клеток в медицине – ждем революцию
Сегодня в базе данных клинических испытаний Национальных институтов здоровья США перечислено почти полтысячи работ с использованием стволовых клеток, находящихся на разных стадиях исследования
Однако настораживает тот факт, что первое из них, касающееся использования клеток нервной системы (олигодендроцитов) для лечения травм спинного мозга, было прервано в ноябре 2011 г. по неизвестной причине. После этого американская компания «Geron Corporation» – один из пионеров в области «стволовой» биологии, которая проводила это исследование, объявила о полном сворачивании своих работ в этой области.
Тем не менее, хочется верить, что медицинское применение стволовых клеток со всеми их волшебными возможностями не за горами.
Древняя ДНК – от неандертальца до чумной бактерии

Возраст знаменитых наскальных изображений в пещере Шове (Франция) составляет около 30 тыс. лет. Проанализировав ДНК из найденных там лошадиных волос, генетики смогли определить масть древних животных, которые были гнедыми, вороными и чубарыми
В 1993 г. вышел фильм «Парк Юрского периода», в котором на экране гуляли монстры, воссозданные из остатков ДНК из крови динозавров, сохранившейся в желудке замурованного в янтаре комара. В тот же год один из крупнейших авторитетов в области палеогенетики, английский биохимик Т. Линдал заявил, что даже при самых благоприятных условиях из ископаемых остатков нельзя извлечь ДНК старше 1 млн лет. Скептик оказался прав – ДНК динозавров так и осталась недоступной, однако успехи в техническом совершенствовании методов извлечения, амплификации и секвенирования более молодой ДНК, достигнутые за последнее десятилетие, впечатляют.
На сегодня полностью или частично прочитаны геномы неандертальца, недавно открытого денисовца и множества ископаемых останков Homo sapiens, а также мамонта, мастодонта, пещерного медведя… Что касается более далекого прошлого, то была изучена ДНК из хлоропластов растений, чей возраст датируется 300—400 тыс. лет, и ДНК бактерий возрастом 400—600 тыс. лет.
Из исследований более «молодой» ДНК стоит отметить расшифровку генома штамма вируса гриппа, вызвавшего 1918 г. эпидемию знаменитой «испанки», и генома штамма чумной бактерии, опустошившей Европу в XIV в.; в обоих случаях материалы для анализа были выделены из захороненных останков умерших от болезни.
Нейропротезирование – человек или киборг?
Эти достижения принадлежат скорее к инженерной, а не биологической мысли, но от этого они не смотрятся менее фантастическими.
Вообще простейший тип нейропротеза – электронный слуховой аппарат – был изобретен еще более полувека назад. Микрофон этого устройства улавливает звук и передает электрические импульсы непосредственно на слуховой нерв или в ствол головного мозга – таким образом можно вернуть слух даже пациентам с полностью разрушенными структурами среднего и внутреннего уха.
Взрывообразное развитие микроэлектроники за последний десяток лет позволило создать такие виды нейропротезов, что впору говорить о возможности скорого превращения человека в киборга. Это и искусственный глаз, действующий по тому же принципу, что и слуховой прибор; и электронные подавители проведения болевых импульсов через спинной мозг; и автоматические искусственные конечности, способные не только воспринимать управляющие импульсы мозга и выполнять действия, но и передавать ощущения обратно в мозг; и электромагнитные стимуляторы зон мозга, пораженных при болезни Паркинсона.
Сегодня уже ведутся исследования, касающиеся возможности интеграции разных отделов мозга с компьютерными микросхемами для улучшения умственных способностей. И хотя до полной реализации этой идеи далеко, но видеоклипы, показывающие людей с искусственными руками, уверенно пользующихся ножом и вилкой и играющими в настольный футбол, поражают воображение.
Нелинейная оптика в микроскопии – увидеть невидимое
Из курса физики студенты твердо усваивают понятие дифракционного предела: в самый лучший оптический микроскоп невозможно увидеть объект, размеры которого меньше половины длины волны, разделенной на показатель преломления среды. При длине волны 400 нм (фиолетовая область видимого спектра) и показателе преломления около единицы (как у воздуха) объекты мельче 200 нм неразличимы. А именно в этот размерный диапазон попадают, например, вирусы и множество интереснейших внутриклеточных структур.
Поэтому в последние годы широкое развитие в биологической микроскопии получили методы нелинейной и флуоресцентной оптики, для которых понятие дифракционного предела неприменимо. Сейчас такими методами удается в деталях исследовать внутреннее строение клеток.