Файл: Реферат Давление газа с точки зрения молекулярнокинетической теории. Уравнение состояния идеального газа..docx
Добавлен: 12.01.2024
Просмотров: 133
Скачиваний: 5
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Министерство сельского хозяйства Российской федерации
Федеральное государственное бюджетное образовательное учреждение высшего образования
Государственный университет по землеустройству
Кафедра Высшей математики и физики
Реферат
«Давление газа с точки зрения молекулярно-кинетической теории. Уравнение состояния идеального газа.»
Выполнил студент очной формы обучения
Направление подготовки Городской кадастр
1 курса группы 11 ГК Данилова Анастасия Дмитриевна
Преподаватель: Климов Александр Петрович
Москва
2022
Оглавление
Молекулярно-кинетическая теория 3
Дискретное строение вещества 5
Тепловое движение частиц вещества 6
Давление газа с точки зрения молекулярно-кинетической теории 7
Уравнение состояния идеального газа 12
Ссылки на источники 14
Молекулярно-кинетическая теория
Молекулярно-кинетическая теория (MKT) - теория, объясняющая свойства макроскопических тел и тепловые процессы в этих телах на основе представлений о веществе как о системе атомов и молекул, беспрерывно и хаотически движущихся и взаимодействующих друг с другом.
Основные положения молекулярно-кинетической теории. В основе MKT лежат три положения:
I положение: все вещества состоят из частичек — атомов и молекул. Существование атомов и молекул было предсказано еще древними философами. Однако ясную количественную теорию этого факта впервые предложил английский ученый-химик Джон Далтон (1766-1844). Составив таблицу относительных атомных масс ряда элементов, он заложил основу теории атомного строения вещества. В наше время, используя способность электронного микроскопа увеличивать в миллионы раз размеры объекта, можно увидеть и сфотографировать достаточно большие молекулы.
II положение: частицы, из которых состоит вещество, находятся в непрерывного и беспорядочного (хаотического) движения.
Верность этого положения была установлена на основе открытия, сделанного в 1827 году английским ботаником Робертом Броуном, наблюдавшим в микроскоп за движением цветочной пыльцы в воде. Он обнаружил, что пыльца совершает хаотическое движение и изменяет свое положение по сложной траектории
(с).
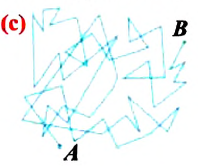
Беспорядочное движение частиц, называемое "броуновским движением", теоретически было объяснено А.Эйнштейном в 1905 году, а опытным путем было подтверждено в 1909-1911 годах французским физиком Яном Батистом Перреном (1870— 1942). Он подтвердил предположение Эйнштейна, что причиной хаотического движения частичек краски в воде является тепловое движение молекул воды. Перрен определил, что интенсивность броуновского движения частиц зависит не от их химической природы, а от температуры: с увеличением температуры интенсивность броуновского движения также увеличивается. Таким образом:
Броуновским движением называется беспорядочное движение частиц, взвешенных в жидкости (или газе).
Другим явлением, подтверждающим второе положение MKT, является диффузия.
Диффузией называется процесс самопроизвольного взаимного проникновения атомов или молекул одного вещества в межатомные или межмолекулярные промежутки другого вещества.
Первое количественнное описание процесса диффузии дал в 1855 году немецкий физик и физиолог Адольф Фик (1829-1901) в законе, названном "законом диффузии Фика ".
III положение: частицы вещества взаимодействуют друг с другом, то есть между ними существуют силы взаимного притяжения и отталкивания.
Подтверждением этого положения является возникновение силы упругости во время деформации тела. Эти силы имеют характер близкодействия, электромагнитную природу и в значительной степени зависят от расстояния между частицами. Например, было определено, что силы притяжения между молекулами уменьшаются по закону
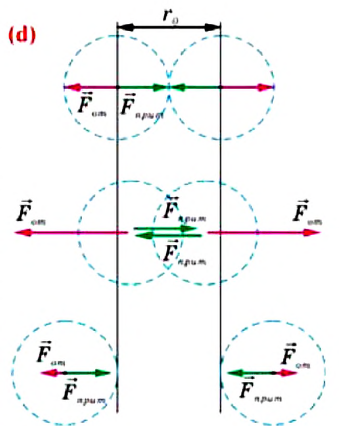
В основе молекулярно-кинетической теории лежат три положения:
-
Вещество имеет дискретное строение, т. е. состоит из микроскопических частиц. -
Частицы вещества хаотически движутся. -
Частицы вещества взаимодействуют между собой.
Дискретное строение вещества
Согласно первому положению молекулярно-кинетической теории вещество имеет дискретное строение, т. е. состоит из отдельных частиц (молекул, атомов, ионов). При изучении физики в 6 и 8 классах вы узнали, что реальное существование молекул подтверждают экспериментальные факты. Такими фактами, в частности, являются растворение веществ в воде и в других растворителях, сжатие и расширение любых тел и особенно газов, механическое дробление вещества, диффузия, броуновское движение и многое другое.
Глаз может различить две точки, если расстояние между ними не менее 0,1 мм. Современные оптические микроскопы позволяют различать структуры с расстоянием между элементами порядка двухсот нанометров и более (

фотография молекулы нуклеиновой кислоты нитевидной формы, общая длина которой 34 мкм.
Переход от световых волн в оптических микроскопах к ускоренным пучкам электронов, управляемым электрическими и магнитными полями, в электронных микроскопах улучшил пределы разрешения до десятых долей нанометра. Использование электронных микроскопов позволило наблюдать и фотографировать атомарные структуры.
4 марта 1981 г. немецкий учёный Герд Бинниг и швейцарский учёный Генрих Рорер впервые в мире наблюдали отдельные атомы на поверхности кремния (рис. 3). На рисунке 4, а, б изображены электронный и туннельный микроскопы. За создание первого электронного микроскопа немецкому учёному Эрнсту Руске и за изобретение сканирующего туннельного микроскопа Г. Биннигу и Г. Рореру была присуждена Нобелевская премия по физике за 1986 год.

Тепловое движение частиц вещества
Согласно второму положению молекулярно-кинетической теории частицы, составляющие вещество, находятся в непрерывном хаотическом движении, которое называют тепловым.
Наиболее ярким экспериментальным подтверждением теплового движения частиц вещества (молекул, атомов и ионов) является броуновское движение, т. е. движение «взвешенных» в жидкости или газе мельчайших нерастворимых твёрдых частиц размерами примерно 1 мкм и меньше. «Взвешенные» частицы — это частицы, плотность вещества которых близка к плотности окружающей их среды (жидкости или газа). Они распределяются по всему объёму среды, не оседая на дно сосуда и не поднимаясь на её поверхность (рис. 5).

Давление газа с точки зрения молекулярно-кинетической теории
С точки зрения молекулярно-кинетической теории давление газа возникает в результате ударов молекул, образующих газ, по телу, соприкасающемуся с ним. При ударе
импульс молекулы газа изменяется:
средней силе
продолжительностью
. Используя второй закон Ньютона для описания удара молекулы
При нормальных условиях и макроскопических размерах сосуда число ударов молекул газа о плоскую поверхность площадью 1
Пусть в сосуде, имеющем форму куба с ребром длиной l (рис. 12), находится идеальный газ, состоящий из одинаковых молекул массой
Для описания удара молекулы газа о стенку ABCD (см. рис. 12) запишем соотношение (3.1) в проекциях на координатные оси: