Добавлен: 14.02.2019
Просмотров: 109510
Скачиваний: 5703
Chapter 7. Neuroendocrine Syndromes
278
Общие сведения (general information)
Гипоталамический синдром возникает вследствие ацирхорального ритма
выработки ГнРГ, вторично проявляясь нарушением регулярности менстру-
ального цикла, поликистозными яичниками (англ. — polycystic ovaries) и про-
явлениями гиперандрогении.
Синонимы (convertible terms)
В литературе эта форма может обозначаться как «поликистозные яични-
ки центрального генеза».
Этиология (etiology)
Начало заболевания обычно связано со стрессовыми факторами:
тяжелые инфекционные процессы в препубертатном или пубертатном
•
периоде — ангины, аденовирусные инфекции и пр.;
интоксикации;
•
эмоционально-психические травмы;
•
начало половой жизни;
•
роды, самопроизвольные или артифициальные аборты.
•
NB!
NB!
Для гипоталамического синдрома характерна четкая времен-
ная граница начала заболевания.
Патогенез (pathogenesis)
Вследствие воздействия стрессового фактора происходит нарушение
образования и выделения дофамина и эндогенных опиоидных пептидов
в надгипоталамических и/или медиобазальных структурах гипоталамуса.
Это изменяет цирхоральный ритм выброса ГнРГ, следовательно, нарушает
и выделение гонадотропинов (особенно ЛГ) гипофизом. В ответ на измене-
ние выработки гонадотропинов нарушается процесс фолликулогенеза, раз-
вивается ановуляторная дисфункция яичников. С каждой несостоявшейся
овуляцией происходит кистозная атрезия все новых фолликулов, в яични-
ках возникает множество мелких кист (рис. 7.1).
NB!
NB!
Симптом поликистозного изменения яичников универсален
для нескольких синдромов, при которых по разным причи-
нам нарушается фолликулогенез.
К ним относится метаболический синдром, болезнь поликистозных
яичников (БПКЯ; первичная ароматазная недостаточность яичников), адре-
ногенитальный синдром (врожденная дисфункция коры надпочечников),
может быть проявлением гиперпролактинемии, андрогенпродуцирующих
опухолей надпочечников или яичников.
Отсутствие нормального фолликулогенеза, сопровождающее все эти
синдромы, потенцирует увеличение синтеза андрогенов, закрепляет нару-
шение выработки ЛГ и ФСГ, формируя порочный круг патогенеза и усугу-
бление клинических проявлений (см. раздел 7.5.1).
279
Глава 7. Нейроэндокринные синдромы в гинекологии
Клиническая картина
(clinical presentation)
Гипоталамический синдром обя-
зательно проявляется диэнцефаль-
ными (гипоталамическими) нару-
шениями: вегетативно-сосудистой
астенией (обычно по гипертони-
ческому типу), нарушением сна
и бодрствования, эмоциональными
нарушениями (раздражительность,
плаксивость). Механизм развития
синдрома обусловливает и возник-
новение ряда других симптомов:
повышение аппетита и жажду
•
(проявления нарушения толе-
рантности к глюкозе);
ожирение (нарушение липид-
•
ного обмена);
гипертрихоз (вторичная яич-
•
никовая гиперандрогения);
нарушение менструа льной
•
функции (ановуляция, олиго-
менорея);
бесплодие (ановуляция);
•
гиперпластические процессы
•
эндометрия (относительная
гиперэстрогения).
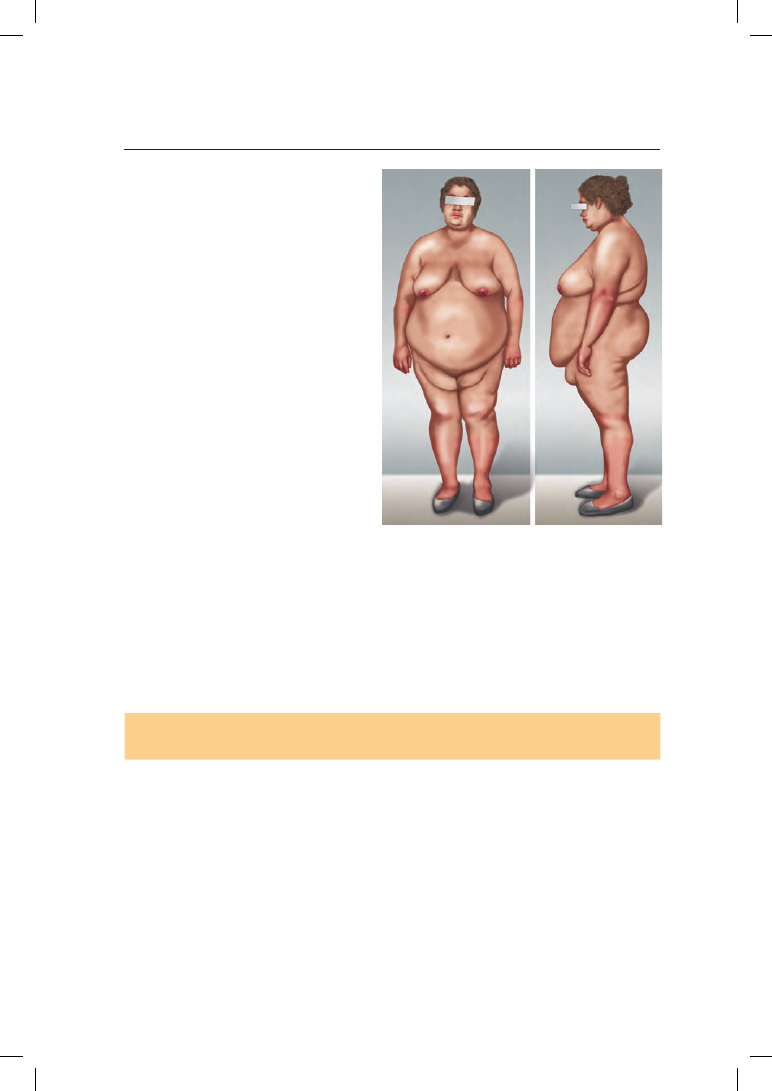
Ожирение у пациенток с гипоталамическим синдромом имеет специ-
фический характер: жировая ткань локализуется в верхней трети плеча
и в нижней половине живота («фартук»), характерен «климактерический
горбик» — скопление жира в области VII шейного позвонка. Молочные
железы даже у молодых нерожавших женщин отвислые за счет большого
содержания жировой ткани (рис. 7.2). На животе и молочных железах могут
появляться стрии. На фоне олигоменореи со временем развивается вторич-
ная ароматазная недостаточность яичников и гиперандрогения, проявляю-
щаяся гипертрихозом.
Менархе у больных гипоталамическим синдромом наступает раньше,
чем в популяции (9–12 лет). Это обусловлено ранней активацией гипота-
ламических структур. В пубертатном периоде менструальный цикл имеет
неустойчивый характер, интервалы между менструациями составляют
21–70 дней; летом интервалы увеличиваются. Ановуляция формируется
через стадию недостаточности желтого тела, постепенно развивается оли-
гоменорея и ановуляторное бесплодие.
Возникает риск гиперпластических процессов эндометрия и молочных
желез. Он обусловлен увеличением внегонадного синтеза эстрогенов в жиро-
вой ткани (поддерживается ожирением, нарушением стероидогенеза в яич-
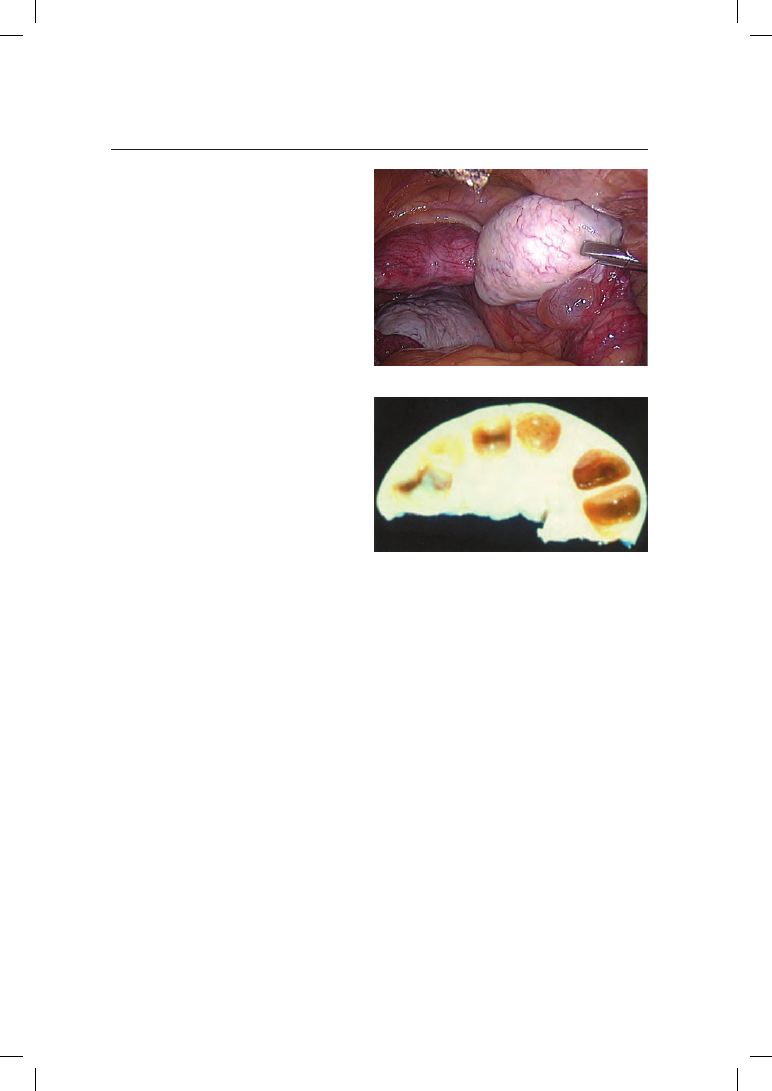
а
б
Рис. 7.1. Макроскопическая картина поли-
кистозных яичников: а — внешний вид; б —
в разрезе
Chapter 7. Neuroendocrine Syndromes
280
никах, дополнительной ароматиза-
цией надпочечниковых андрогенов
в жировой ткани) и длительным воз-
действием этих эстрогенов на эндо-
метрий и ткань молочной железы
при пролонгированном цикле.
Иногда гипота лами ческ ий
синдром обозначают как «мета-
болический», но это некорректно.
Действительно, гипоталамические
расстройства могут проявляться
нарушением метаболизма липидов
и глюкозы, но это происходит вто-
рично и не всегда.
Метаболический синдром имеет
первичные нарушения метаболизма,
проявляющиеся обязательным уве-
личением объема талии более 80 см
и сочетанием 2 критериев и более:
повышение уровня триглице-
•
ридов более 1,7 мМ/л;
снижение содержания липопро-
•
теидов высокой плотности менее
1,29 мМ/л;
повышение АД выше 130/85 мм рт.ст.;
•
увеличение содержания глюкозы более 5,6 мМ/л;
•
нарушение толерантности к глюкозе.
•
Метаболический синдром также может приводить к расстройствам функции
гипоталамо-гипофизарной системы, поликистозным яичникам, нарушениям
менструального цикла и гиперандрогении, но это происходит вторично.
NB!
NB!
Проявления гипоталамического и метаболического синдромов
могут быть сходными, но патогенез этих синдромов различен.
Диагностика (diagnosis)
Патогномоничные признаки СПКЯ гипоталамического генеза выяв-
ляют уже при сборе жалоб и анамнеза: жалобы имеют четкую времен-
ную границу — после психического стресса, нейроинфекции, интоксика-
ции, осложненной беременности или родов. Нарушения менструального
цикла возникают первично (при стрессовом факторе в период препубертата
или пубертата) или вторично после менархе, усугубляются от ациклических
кровотечений до аменореи, часто сопровождаются бесплодием.
Синдром включает множественные вегетативно-сосудистые, обменно-
эндокринные нарушения, подтверждаемые изменениями электроэнцефа-
лограммы и исследованием гормонального профиля.
Рис. 7.2. Внешний вид больной гипотала-
мическим синдромом
281
Глава 7. Нейроэндокринные синдромы в гинекологии
Нарушения метаболизма глюкозы и липидов, в том числе ожирение — необя-
зательный признак. При возникновении ожирения подкожная жировая клетчатка
распределяется преимущественно на плечевом поясе и внизу живота. Возможны
гипертрихоз, гирсутизм, акне, стрии на коже живота и молочных желез.
При гинекологическом осмотре отклонений от нормы не обнаруживают.
УЗИ выявляет увеличение объема яичников и не менее 8–10 перифери-
ческих гипоэхогенных структур — фолликулов диаметром 6–10 мм, доми-
нантный фолликул обычно отсутствует (см. раздел 7.5.1, рис. 7.11). Следует
помнить, что подобная картина при УЗИ визуализируется у 25% фертиль-
ных женщин без жалоб и клинических симптомов, имеющих нормальные
овуляторные менструальные циклы.
NB!
NB!
Диагноз поликистозных яичников не может быть поставлен
только по результатам УЗИ.
Диагноз любого из синдромов, сопровождающихся поликистозными
изменениями яичников, должен быть обязательно подтвержден рядом дру-
гих специфических признаков. Анализ этих признаков устанавливает нали-
чие нейроэндокринного синдрома. Верификация любого из нейроэндо-
кринных синдромов означает определение первичного уровня поражения
регуляции репродуктивной системой.
Лечение (treatment)
Лечение гипоталамического синдрома следует начинать с коррекции
метаболических нарушений, снижения массы тела. После снижения массы
тела на 12–15% у женщин восстанавливается регулярный менструальный
цикл, причем у 2/3 из них — овуляторный. После коррекции инсулинорези-
стентности для лечения гипертрихоза назначают микродозированные КОК
с гестагеном, имеющим антиандрогенное действие (ципротерона ацетат,
диеногест, дроспиренон, хлормадинона ацетат). При противопоказаниях
к КОК назначают монотерапию верошпироном, имеющим антиандрогенное
действие.
При рецидивирующих гиперпластических процессах эндометрия пока-
зана клиновидная резекция яичников.
7.4. ГИПОФИЗАРНЫЕ РАССТРОЙСТВА
DYSFUNCTION OF HYPOPHYSIS
7.4.1. Послеродовой гипопитуитаризм
(синдром Симмондса–Шихена)
Symmonds–Sheehan's Syndrome
Код по МКБ-10 (International Classification of Diseases, ICD)
E23.0. Гипопитуитаризм (англ. — hypopituitarism).
Chapter 7. Neuroendocrine Syndromes
282
Общие сведения (general information)
Сведения о гипопитуитаризме известны с конца XIX в., но только
в 1937 г. H. Sheehan (в русскоязычной литературе встречаются варианты
транскрипции фамилии — Шихен, Шихан, Шиен) научно обосновал связь
массивного кровотечения во время родов с последующей гипофункцией
передней доли гипофиза. М. Симмондс (M. Simmonds) в 1914 г. описал точно
такой же синдром, но в связи с септическим шоком
1
.
Синонимы (convertible terms)
Синдром Шихена, синдром Шихана, синдром Шиена, синдром
Симмондса–Шихена.
NB!
NB!
Синдром Симмондса–Шихена — это гипофункция передней
доли гипофиза, возникающая после родов или аборта, ослож-
ненных массивным кровотечением или септическим шоком.
Эпидемиология (epidemiology)
Частота возникновения синдрома Шиxена после массивной кровопотери
в родах или в результате осложнения аборта достигает 40%. Заболевание
развивается у 25% женщин, перенесших во время родов кровопотерю 700–
800 мл, у 50% — после кровопотери 800–900 мл и у 75–80% женщин с мас-
сивной кровопотерей до 4000 мл.
В последние десятилетия риск развития некроза гипофиза, обусловлен-
ного септическим шоком, значительно уменьшился. Это связано в первую
очередь со снижением септических осложнений после родов и успешной
борьбой с послеродовой инфекцией. Тем не менее акушерский сепсис все
еще остается причиной материнской смертности и заболеваемости в эконо-
мически слабо развитых странах.
Патогенез (pathogenesis)
Гипофиз имеет анатомические особенности кровоснабжения. В его кро-
вотоке отсутствуют коллатерали и какой-либо альтернативный кровоток,
т. е. механизмов защиты тканей от ишемии нет.
Массивное кровотечение или септический шок, сопровождающие роды
или аборт, могут привести к стойкому спазму или тромбозу в сосудах
передней доли гипофиза. Вледствие нарушения трофики аденогипофиза
возникают его ишемия и некроз. Риск таких тяжелых последствий для аде-
ногипофиза особенно высок во время беременности, поскольку появляется
гестационная компенсаторная гиперплазия клеток передней доли гипофиза,
масса которого увеличивается в 2 раза. Кроме того, после родов происходит
физиологический выброс АКТГ, что также способствует ишемии.
Риск некроза аденогипофиза дополнительно увеличивается у женщин:
1
Simmonds M. Über Hypophysisschwund mit tödlichem Ausgang // Deutsche medicinische
Wochenschrift. — 1914. — Vol. 40. — P. 322–323;
Sheehan H. L. Postpartum necrosis of anterior pituitary // J. of Pathology and Bacteriology. — 1937. —
Vol. 45. — P. 189–214.