Файл: Расчет ректификационной колонны по дисциплине Процессы и аппараты химической технологии.docx
Добавлен: 11.01.2024
Просмотров: 265
Скачиваний: 2
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
СОДЕРЖАНИЕ
2.2 Построение х-у диаграммы, кривых изобар пара и жидкости
2.4 Расчет однократного испарения бинарной смеси
2.5 Расчет материального баланса ректификационной колонны
2.7 Расчет числа тарелок на комбинированной и x-y-диаграмме
2.8 Расчет профиля концентраций и нагрузок по высоте колонны
2.9 Расчет фактического числа тарелок
2.10 Расчет диаметра ректификационной колонны
2.11 Расчет высоты ректификационной колонны
Министерство науки и высшего образования Российской Федерации
Федеральное государственное бюджетное образовательное учреждение
высшего образования
«Уфимский государственный нефтяной технический университет»
Кафедра нефтехимии и химической технологии
| РГР принят с оценкой | |
| За соблюдение календарного графика | |
| За оформление | |
| За защиту | |
| Итоговая | |
Руководитель: доцент каф. НХТ
_______________ С.П.Ломакин
РАСЧЁТНО-ГРАФИЧЕСКАЯ РАБОТА
на тему
РАСЧЕТ РЕКТИФИКАЦИОННОЙ КОЛОННЫ
по дисциплине «Процессы и аппараты химической технологии»
направление подготовки Химическая технология
профиль «Химическая технология органических веществ»
Студент гр. БТБ-20-01 А.Х. Хамматова
Уфа 2022
СОДЕРЖАНИЕ
ВВЕДЕНИЕ 2
1 Теоретическая часть 3
2 Расчетная часть 5
2.1 Построение зависимости давления насыщенных паров от температуры 5
2.2 Построение х-у диаграммы, кривых изобар пара и жидкости 9
2.3 Построение энтальпийной диаграммы 12
2.4 Расчет однократного испарения бинарной смеси 17
2.4.1 Расчет x*F и y*F 17
2.4.2. Расчет равновесной температуры 19
2.4.3 Проверка значения мольной доли отгона 19
2.5 Расчет материального баланса ректификационной колонны 20
2.5.1 Определение молекулярной массы сырья, дистиллята и остатка 20
2.5.2 Покомпонентный расчет материального баланса РК
22
2.5.3 Проверка материального баланса 24
2.5.4 Расчет теплового баланса ректификационной колонны 25
2.6 Расчет режима полного орошения Error: Reference source not found
2.7 Расчет числа тарелок на комбинированной и x-y-диаграмме 29
2.7.1 Расчет числа теоретических тарелок на xʹ-yʹ диаграмме 29
2.7.2. Расчёт числа теоретических тарелок на комбинированной диаграмме 32
2.8 Расчет профиля концентраций и нагрузок по высоте колонны 33
2.8.1 Расчет профиля концентраций и температуры по высоте колонны 33
2.8.2 Расчет флегмового и парового числа колонны 37
2.9 Расчет фактического числа тарелок 46
2.10 Расчет диаметра ректификационной колонны 48
2.11 Расчет высоты ректификационной колонны 54
2.12 Расчет конденсатора-холодильника 55
2.13 Расчет кипятильника 53
2.14 Расчет диаметра штуцеров Error: Reference source not found
ЗАКЛЮЧЕНИЕ 60
Список использованной литературы 62
ВВЕДЕНИЕ
Для получения продуктов с любой желаемой концентрацией компонентов и с высокими выходами служит процесс ректификации, заключающийся в многократно повторяющемся контактировании неравновесных паровой и жидкой фаз.
Образованные в результате контакта паровая и жидкая фазы будут отличаться по составу от вступивших в контакт встречных неравновесных потоков паровой и жидкой фаз. В итоге такого контакта пар обогатится низкокипящим компонентом, а жидкость – высококипящим. Если исходные пары и жидкость находились при одинаковом давлении, то для обеспечения этих условий требуется, чтобы температура вступающей в контакт жидкости была ниже температуры паров. После контактирования температуры пара и жидкости выравниваются, так как система стремится к состоянию равновесия.
Производя многократное контактирование неравновесных потоков паровой и жидкой фаз, направляя после каждой ступени пары на смешение с жидкостью
, а жидкость на контакт с парами, более бедными НКК, можно изменить составы фаз желаемым образом. Подобное контактирование фаз по схеме противотока в целом по аппарату осуществляется в специальных аппаратах – ректификационных колоннах, заполненных различными контактными устройствами: тарелками, насадками и т.д.
Таким образом, процесс ректификации есть диффузионный процесс разделения жидких смесей, компоненты которых различаются по температурам кипения, осуществляемый путем противоточного контактирования неравновесных паров и жидкости.
Расчет ректификационной колонны сводится к определению ее основных геометрических размеров – диаметра и высоты. Оба параметра определяются гидродинамическим режимом работы колонны, который, в свою очередь, зависит от скоростей и физических свойств взаимодействующих фаз, а также от типа контактного устройства.
2.2 Построение х-у диаграммы, кривых изобар пара и жидкости
Для построения необходимо определить мольные доли НКК в жидкой фазе и равновесной паровой фазе. Для этого воспользуемся:
- законом Дальтона, который гласит: парциальные давление компонента газовой смеси
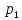 равно произведению давления в системе
равно произведению давления в системе 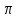 на мольную долю компонента
на мольную долю компонента 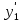 в газовой смеси, т.е.
в газовой смеси, т.е. 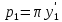 (4)
(4)- законом Рауля, согласно которому парциальные давление
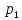 компонента идеального жидкого раствора равно произведению давления насыщенных парой
компонента идеального жидкого раствора равно произведению давления насыщенных парой 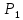 компонента при данной температура на мольную долю компонента
компонента при данной температура на мольную долю компонента 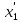 в жидкой фазе, т.е.
в жидкой фазе, т.е.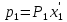 (5)
(5)Совместным решением Дальтона и Рауля получим следующее уравнение равновесия:
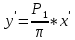 (6)
(6)Согласно закону Рауля, парциальные давления компонентов определяются следующим образом:
-для НКК:
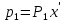 (7)
(7)-для ВКК:
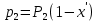 (8)
(8)Давление насыщенных паров смеси этих компонентов
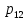 равно сумме парциальных давлений; так как в рассматриваемой системе жидкость находится в равновесии с соответствующим насыщенным паром, то
равно сумме парциальных давлений; так как в рассматриваемой системе жидкость находится в равновесии с соответствующим насыщенным паром, то 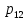 равно внешнему давлению
равно внешнему давлению 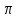 :
: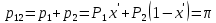 (9)
(9)Из уравнения следует, что при известном внешнем давлении
 и температуре системы t можно однозначно определить состав жидкой фазы:
и температуре системы t можно однозначно определить состав жидкой фазы: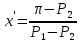 (10)
(10)Используя формулы (6) и (10) определим мольные доли НКК в жидкой фазе и равновесной паровой фазе
При температуре t1 = 93,862 °С:
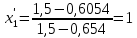 ,
,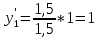 .
.При температуре t2 = 99,1415 °С:
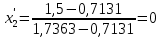 ,7691,
,7691,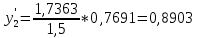 .
.При температуре t3 = 104,421°С:
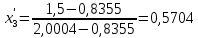 ,
,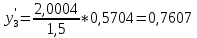 .
.При температуре t4 = 109,7005 °С:
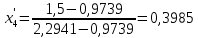 ,
,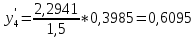 .
.При температуре t5 = 114,98°С:
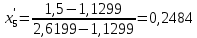 ,
,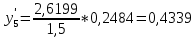 .
.При температуре t6 = 120,2595 °С:
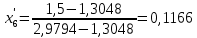 ,
,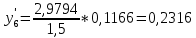 .
.При температуре t7= 125,539 °С:
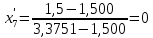 ,
,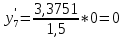 .
.Полученные результаты приведены в таблице 4.
Таблица 4 – Результаты расчета равновесных концентраций
| t, ˚C | PБ, атм | PТ, атм | x’ | y’ |
| 93,862 | 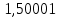 | 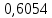 | 1,0000 | 1,0000 |
| 99,1415 | 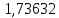 | 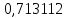 | 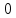 ,7691 ,7691 | 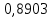 |
| 104,421 | 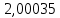 | 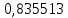 | 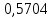 | 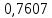 |
| 109,7005 | 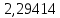 | 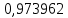 | 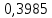 | 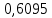 |
| 114,98 | 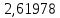 | 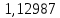 | 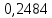 | 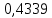 |
| 120,2595 | 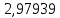 | 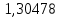 | 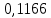 | 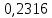 |
| 125,539 | 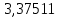 | 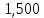 | 0,0000 | 0,0000 |