Файл: Пояснительная записка Содержание и структура заданий.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 09.11.2023
Просмотров: 216
Скачиваний: 2
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
СОДЕРЖАНИЕ
ЕЗЕЛОЖ- без этого элемента вы не отрежете хлеб;
СЛИКОДОР- без него не проживете и 10 минут;
ЕКЛИНЬ - этот элемент помогает бороться первому элементу со вторым;
МФОЛЬВАР- из него сделана спираль лампочки накаливания;
ПРИТОНК- его можно найти в лампочках грибовидной формы;
МЕДИНЛОБ- элемент помогает лампочке держать спираль;
МНИКРЕЙ- элемент ищи среди камней;
ЛЕОДРУГ-без этого элемента нет огня;
= FeCl3 + K3PO4 =
Na2O + N2 O5 = Cu(NO3)2 + NaOH =
Fe Cl3 + K3PO4 = Zn + CuSO4 =
Оксид натрия + серная кислота = оксид лития + серная кислота =
Оксид серы IV + гидроксид калия = оксид железа III + серная кислота =
Оксид фосфора V + гидроксид натрия = оксид алюминия + серная кислота =
1) H2CO3, HNO3, HMnO4, H2SiO3 2) H4P2O7, H3PO4, H2SO4, H3AsO4, HClO
оксидом кислотой
основанием солью
солеобразующим оксидом несолеобразующим оксидом
основным оксидом кислотным оксидом
бескислородной кислотой кислородсодержащей кислотой
щёлочью нормальной солью
кислой солью основной солью

Проверочная работа. Соли
Вариант 1
SO3; CuOH; H2S; CuSO4; Ni(NO2)2; NaHCO3; K2O; NaHSO3; (CuOH)2CO3;
HNO3; Fe(OH)3; Na2Cr2O7; Fe(H2PO4)2;

Проверочная работа. Соли
Вариант 2
CO; Cu(OH)2; HCl; CuCO3; Fe2(SO4)3; NaHSO3; Li2O; NaH2PO4;
(CaOH)2SO4; HClO4; Al(OH)3; Cr2(SO4)3; Ca(HSO4)2
Проверочная работа. Номенклатура кислот.
Задание: заполните колонки таблицы.

Самостоятельная работа. Классы неорганических веществ
1 вариант
ZnO + HNO3 =
Al + H2SO4 =
P2O5 + KOH =
Fe(OH)2 + HNO3 =
Fe2O3 + H2O =
BaO + HNO3 =
SO2, K2O, N2O5, Mg(OH)2, LiOH, Ba(OH)2, H3PO4, HClO, H2SO3.
атомов кислорода:
H2SiO3, HNO3, H2S, H3PO4, HMnO4, HCN, HF.

Самостоятельная работа. Классы неорганических веществ
2 вариант
1. Закончите уравнения химических реакций, напишите тип реакции:
HNO3 + CuSO4=
HCl + FeS =
CO2 + Ca(OH)2 =
Ba(OH)2 + Fe(NO3 )3 =
Na2O + N2O5 =
N2O + NaOH =
2. Напишите названия веществ:
Al2O3, Cl2O7, Ag2O, Hg(OH)2, KOH, Pt(OH)2, HClO3, H2CO3, H2CrO4.
3.Классифицируйте следующие основания по кислотности и по растворимости
в воде:
NaOH, Cr(OH)3, Ba(OH)2, CuOH, Mg(OH)2, Al(OH)3.

Самостоятельная работа. 3 вариант
1. Закончите уравнения химических реакций, напишите тип реакции:
NaCl + HNO3 =
Ca + H2SO4 =
KOH + NaNO3 =
C uOHtº
uOHtº
N2O + NaOH =
CO2 + Ca(OH)2 =
2. Напишите названия веществ:
MnO2, Ag2O, PbO2, Sr(OH)2, KOH, Co(OH)3, H2MnO4, HNO3, H2SiO3.
3. Классифицируйте следующие оксиды:
BaO, CrO3, Cu2O, SnO, ZnO, Cl2O7.
Контрольная работа. Электролитическая диссоциация. Вариант 1
Контрольная работа. Электролитическая диссоциация. Вариант 2
Контрольная работа. Электролитическая диссоциация. Вариант 3
Na2O + N2 O5 = Cu(NO3)2 + NaOH =
Fe Cl3 + K3PO4 = Zn + CuSO4 =
Оксид натрия + серная кислота = оксид лития + серная кислота =
Оксид серы IV + гидроксид калия = оксид железа III + серная кислота =
Оксид фосфора V + гидроксид натрия = оксид алюминия + серная кислота =
-
Определите валентность кислотного остатка и кислотообразующего элемента.
1) H2CO3, HNO3, HMnO4, H2SiO3 2) H4P2O7, H3PO4, H2SO4, H3AsO4, HClO
-
Что называется:
оксидом кислотой
основанием солью
солеобразующим оксидом несолеобразующим оксидом
основным оксидом кислотным оксидом
бескислородной кислотой кислородсодержащей кислотой
щёлочью нормальной солью
кислой солью основной солью

Проверочная работа. Соли
Вариант 1
-
Напишите класс и название вещества:
SO3; CuOH; H2S; CuSO4; Ni(NO2)2; NaHCO3; K2O; NaHSO3; (CuOH)2CO3;
HNO3; Fe(OH)3; Na2Cr2O7; Fe(H2PO4)2;
-
Напишите формулы веществ:
-
Гидроксид стронция -
Дигидрофосфат кальция -
Оксид железа (II) -
Нитрат серебра -
Фтороводородная кислота -
Карбонат кальция

Проверочная работа. Соли
Вариант 2
-
Напишите класс и название вещества:
CO; Cu(OH)2; HCl; CuCO3; Fe2(SO4)3; NaHSO3; Li2O; NaH2PO4;
(CaOH)2SO4; HClO4; Al(OH)3; Cr2(SO4)3; Ca(HSO4)2
-
Напишите формулы веществ:
-
Гидроксид алюминия -
Дигидрофосфат меди -
Оксид серы (II) -
Нитрат ртути -
Бромоводородная кислота -
Карбонат натрия
Проверочная работа. Номенклатура кислот.
Задание: заполните колонки таблицы.
| 1 вариант | 2 вариант | ||||
| Формула кислоты | Название кислоты | Название Кислотного ост. | Формула кислоты | Название кислоты | Название Кислотного ост. |
| H2SO4 | | | H2SO3 | | |
| H3PO3 | | | H3PO4 | | |
| H2SiO3 | | | H2CO3 | | |
| HNO3 | | | HNO2 | | |
| HMnO4 | | | H2MnO4 | | |
| | Хлорная к-та | | | Марганцовая к-та | |
| | Марганцовистая к-та | | | Хлористая к-та | |
| | Хромовая к-та | | | Дихромовая к-та | |
| | Хлорноватистая к-та | | | Хлорноватая к-та | |
| | Фосфорная к-та | | | Фосфористая к-та | |

Самостоятельная работа. Классы неорганических веществ
1 вариант
-
Закончите уравнения химических реакций, напишите тип реакции:
ZnO + HNO3 =
Al + H2SO4 =
P2O5 + KOH =
Fe(OH)2 + HNO3 =
Fe2O3 + H2O =
BaO + HNO3 =
-
Напишите названия веществ:
SO2, K2O, N2O5, Mg(OH)2, LiOH, Ba(OH)2, H3PO4, HClO, H2SO3.
-
Классифицируйте следующие кислоты по основности и по содержанию
атомов кислорода:
H2SiO3, HNO3, H2S, H3PO4, HMnO4, HCN, HF.

Самостоятельная работа. Классы неорганических веществ
2 вариант
1. Закончите уравнения химических реакций, напишите тип реакции:
HNO3 + CuSO4=
HCl + FeS =
CO2 + Ca(OH)2 =
Ba(OH)2 + Fe(NO3 )3 =
Na2O + N2O5 =
N2O + NaOH =
2. Напишите названия веществ:
Al2O3, Cl2O7, Ag2O, Hg(OH)2, KOH, Pt(OH)2, HClO3, H2CO3, H2CrO4.
3.Классифицируйте следующие основания по кислотности и по растворимости
в воде:
NaOH, Cr(OH)3, Ba(OH)2, CuOH, Mg(OH)2, Al(OH)3.

Самостоятельная работа. 3 вариант
1. Закончите уравнения химических реакций, напишите тип реакции:
NaCl + HNO3 =
Ca + H2SO4 =
KOH + NaNO3 =
C
 uOHtº
uOHtºN2O + NaOH =
CO2 + Ca(OH)2 =
2. Напишите названия веществ:
MnO2, Ag2O, PbO2, Sr(OH)2, KOH, Co(OH)3, H2MnO4, HNO3, H2SiO3.
3. Классифицируйте следующие оксиды:
BaO, CrO3, Cu2O, SnO, ZnO, Cl2O7.
Контрольная работа. Электролитическая диссоциация. Вариант 1
| 1.Электролиты – это… | А) вещества, которые растворяются в воде Б) вещества, которые не растворяются в воде В) вещества, которые могут проводить электрический ток Г) вещества, которые не могут проводить электрический ток |
| 2.Электролитами являются… | А) сахароза, бензин, азот Б)гидроксид калия, натрий, серная кислота В) сера, углекислый газ, азотная кислота Г) калий, фруктоза, спирт |
| 3.Реакции, протекающие в растворах между электролитами, называются… | А) реакциями замещения Б) реакциями ионного обмена В) реакциями соединения Г) реакциями молекулярного обмена |
| 4.Реакции ионного обмена протекают до конца, если… | А) появляется свет Б) изменяется цвет В) образуется вода Г) образуется соль |
| 5. Выберите уравнение реакции фосфорной кислотыc нитратом серебра в ионной форме. | А) 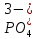 + 3Ag+ = Ag3PO4↓ + 3Ag+ = Ag3PO4↓Б) 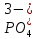 + Ag+ = AgPO4↓ + Ag+ = AgPO4↓В) 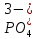 + 3Ag+ = Ag3PO4↑ + 3Ag+ = Ag3PO4↑Г) 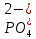 + 3Ag3+ = Ag3PO4↓ + 3Ag3+ = Ag3PO4↓ |
| 6. К раствору хлорида алюминия добавили раствор сульфата натрия. Выберите уравнение реакции. | А) 3AlCl3 + NaSO4 = 2NaCl +3 Al2(SO4)3 Б) 3AlCl3 + 3Na2SO4 = 3NaCl + Al3(SO4)2 В) 2AlCl3 + NaSO4 = 2NaCl + Al2(SO4)3 Г) 2AlCl3 + 3Na2SO4 = 6NaCl + Al2(SO4)3 |
| 7.Сокращенному ионному уравнению реакции Fe+2+2OH-→Fe(OH)2 соответствует молекулярное уравнение реакции: | А)2Fe+ 2H2O+ O2= 2Fe(OH)2 Б) FeCl3+3 NaOH= Fe(OH)3+3NaCl В) FeSO4+ 2KOH= Fe(OH)2+ K2SO4 Г) FeO+ H2O= Fe(OH)2 |
| 8. Фосфорная кислота диссоциирует на… | А) 2 катиона водорода и 1 -анион Б) катион водорода и 2 фосфат - аниона В) на 2 катиона водорода и фосфат - анион Г) на 3 катиона водорода и фосфат- анион |
| 9. Катионами называются... | А) отрицательно заряженные ионы Б) положительно заряженные ионы В) положительно и отрицательно заряженные ионы Г) вещества |
Контрольная работа. Электролитическая диссоциация. Вариант 2
| 1.Электролитическая диссоциация – это… | А) процесс распада неэлектролита с образованием воды и соли Б) процесс распада электролита с образованием воды и соли В) процесс распада неэлектролита с образованием ионов Г) процесс распада электролита с образованием ионов |
| 2.Неэлектролитами являются… | А) сахароза, сера, азот Б) спирт, магний, азотная кислота В) бензин, натрий, серная кислота Г) фруктоза, калий, сернистая кислота |
| 3.Электролиты, которые диссоциируют на катионы металла и гидроксил-анион, называются… | А) солями Б) кислотами В) оксидами Г) основаниями |
| 4.Реакции ионного обмена протекают до конца, если… | А) выделяется газ Б) изменяется цвет В) появляется свет Г) образуется кислота |
| 5. Выберите уравнение реакции серной кислоты с хлоридом бария в ионной форме. | А) 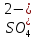 + Ba2+ = BaSO4↑ + Ba2+ = BaSO4↑Б) 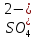 + Ba2+ = BaSO4↓ + Ba2+ = BaSO4↓В) 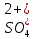 + Ba2- = BaSO4↓ + Ba2- = BaSO4↓Г) 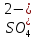 + 2Ba2+ = Ba2SO4↓ + 2Ba2+ = Ba2SO4↓ |
| 6. К раствору сульфата железа II добавили раствор сульфида калия. Выберите уравнение реакции. | А) FeSO4 + K2S = FeS + K2SO4 Б) FeSO4 + KS = FeS + KSO4 В) FeSO3 + K2S = FeS + K2SO3 Г) FeSO4 + K2S = FeS + 2KSO4 |
| 7.Сокращенному ионному уравнению реакции H+ + ОН- = H2O соответствует молекулярное уравнение реакции: | А) ZnCl2 + 2NaOH = Zn(OH)2 + 2NaCl Б) H2SO4 + Cu(OH)2 = CuSO4 + 2H2O В) NaOH + HNO3 = NaNO3 + H2O Г) H2SO4 + Ba(OH)2 = BaSO4 + 2H2O |
| 8.Гидроксид бария диссоциируетна… | А) 1 катион бария и 1 гидроксил – анион Б)1 катион бария и 2 гидроксил-аниона В)2 катиона бария и 1 гидроксил- анион Г) 2 катиона бария и 2 гидроксил- аниона |
| 9. Анионами называются… | А) отрицательно заряженные ионы Б) положительно заряженные ионы В) положительно и отрицательно заряженные ионы Г) вещества |
Контрольная работа. Электролитическая диссоциация. Вариант 3
| 1.Неэлектролиты – это… | А) вещества, которые обладают ионной проводимостью Б) вещества, которые не обладают ионной проводимостью В) вещества, которые могут растворяться в воде Г) вещества, которые не могут растворяться в воде |
| 2.Сильными электролитами являются… | А) H2S, Cu(OH)2, FeS Б) H2CO3, NH4OH В) CH3COOH, вода Г)HBr, KOH, Na2S |
| 3.Электролиты, которые диссоциируют на катионы металла и анионы кислотного остатка, называются… | А) оксидами Б) основаниями В) солями Г) кислотами |
| 4.Реакции между ионами, которые образуются в результате диссоциации электролитов, называются… | А) реакциями замещения Б) реакциями ионного обмена В) реакциями молекулярного обмена Г) реакциями соединения |
| 5. Выберите уравнение реакции угольной кислоты с сульфатом магния в ионной форме. | А) 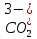 + Mg1+ = MgCO3↓ + Mg1+ = MgCO3↓Б) 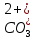 + Mg2- = MgCO3↓ + Mg2- = MgCO3↓В) 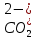 + Mg2+ = MgCO3↑ + Mg2+ = MgCO3↑Г) 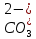 + Mg2+ = MgCO3↓ + Mg2+ = MgCO3↓ |
| 6. К раствору нитрата бария добавили раствор сульфита натрия. Выберите уравнение реакции. | А) BaNO3 + Na2SO3 = BaSO3 + NaNO3 Б) Ba(NO3)2 + Na2SO4 = BaSO4 + 2NaNO3 В)Ba(NO3)2 + Na2SO3 = BaSO3 + 2NaNO3 Г) Ba(NO2)2 + Na2SO3 = BaSO3 + 2NaNO2 |
| 7.Молекулярному уравнению реакции Cu(OH)2 +2HNO3 → Cu(NO3)2 + 2H2O соответствует сокращенное ионное уравнение: | А)Cu(OH)2 +2HNO3 →Cu2+ +2NO3- +2H2O Б) Cu(OH)2 + 2H+ +2NO3- →Cu2+ +2NO3- + +2H2O В) Cu(OH)2 + 2H+ → Cu2+ + 2H2O Г) O2- + 2H+ → H2O |
| 8. Фосфат калия диссоциируетна… | А) катион калия и фосфат-анион Б)2 катиона калия и 3 фосфат – аниона В)3 катиона калия и фосфат-анион Г) катион калия и 4 фосфат - аниона |
| 9. Под действием электрического тока катионы движутся к… | А)катоду Б) аноду В)соединяются с водой Г)остаются на месте |