Файл: Белоусова Юлия Александровна ( фио обучающегося ) выпускная квалификационная работа магистерская диссертация.docx
Добавлен: 23.11.2023
Просмотров: 285
Скачиваний: 3
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Данные таблицы 16 представлены на рисунке 3. На рисунке отслеживаются пики концентрации загрязняющих веществ в виде ХПК и ВВ. Явно прослеживается не стабильность сброса СВ в течение суток, что подтверждает на примере конкретного исследования информацию, изложенную в разделе 3.3 о неравномерности сброса СВ молокоперерабатывающего предприятия.
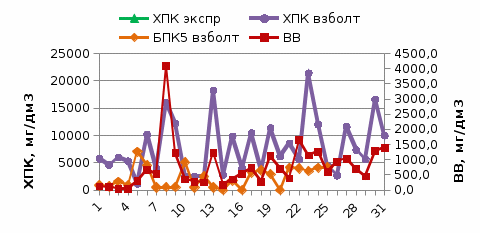
Рисунок 3 Характеристика СВ
Для выбора технологии и определения нагрузки на очистные сооружения необходимо знать основные показатели качества СВ. Показатели, определенные в среднесуточной пробе, представлены в таблице 17.
Таблица 17 Характеристика среднесуточной пробы СВ при сбросе сыворотки в общую канализацию
| Параметры | Концентрация загрязнений, мг/дм3 |
| ХПК взб. экспресс-метод | 3040 |
| ХПК фил. экспресс-метод | 1520 |
| ХПК взб. арбитраж | 10440 |
| ХПК фил. арбитраж | 3740 |
| ВВ | 3212 |
| БПК5 | 3895 |
| Азот аммонийный | 10,3 |
| Фосфор фосфатный | 19,84 |
| Азот нитритный | 5,07 |
| Азот нитратный | 119 |
3.6 Отработка физико-химических методов очистки СВ в лабораторных условиях
3.6.1 Отработка метода коагуляции
Метод коагуляции играет важную роль в процессе очистки СВ и предназначен для удаления взвешенных коллоидных частиц, способных придавать воде мутность. Для коагуляции используют специальные химические реагенты – коагулянты, которые в определенных дозах добавляют в неочищенную воду. В качестве коагулянта будем использовать сульфат алюминия. Дозу коагулянта, а так же выбор флокулянта и его дозу, будем устанавливать экспериментально.
К числу факторов, оказывающих влияние на процесс коагуляции, относятся выбор коагулянтов и флокулянтов, их дозы, значения рН воды до и после введения реагентов, ее температура и др.
В качестве исследуемой воды использовали сточную воду молокоперерабатывающего предприятия. Эксперимент проводили при комнатной температуре, обеспечивающей достаточно высокую скорость физико-химической и биологической очистки СВ. .
Исследование процесса флокуляции проводили на СВ с концентрацией ХПК 1616 мг/дм3. Концентрация коагулянта сернокислого алюимния – глинозема, составила 7 % по Al2O3, концентрация флокулянтов – 1 г/дм3 или 0,1 %.
3.6.1.1 Тестирование флокулянтов
На первом этапе опыты проводили без подщелачивания реакционной смеси (вода–коагулянт–флокулянт). Номера и серии флокулянтов зашифрованы, так как представляют коммерческую тайну. Раствор флокулянта готовили следующим образом. Перемешивание проводили на магнитной мешалке. В емкости (стаканчик) вместимостью 100 см3 взвешивали 0,1 г порошкообразного флокулянта; добавляли этиловый спирт 96 % для смачивания порошка и приливали 100 см3 водопроводной воды. Растворение происходило при постоянном перемешивании около 700 об/мин. в течение 40-60 минут до полного растворения продукта. При перемешивании не допустимо вовлечение воздуха в раствор флокулянта.
При исследовании анионного флокулянта А1 в 4-е мерных цилиндра емкостью 100 см3 наливали исследуемую воду до 100 мл, затем в цилиндры добавляли последовательно 2, 3, 4, 5 см3 раствора сульфата алюминия концентрацией 7,0 %.
Содержимое во всех цилиндрах смешивали медленным перемешиванием палочкой в течение 15-20 секунддля инициирования коагуляции. В период разделения реакционной смеси каждые 3-5 минут пробу медленно перемешивали той же палочкой. Затем в каждый цилиндр добавляли флокулянт по 1 см
3 в каждый цилиндр, и тоже перемешивали медленно палочкой в течение 3-5 минут и оставляем для завершения процесса коагуляции. Сразу после добавления реагентов и после 30 минут отстаивания не наблюдалось никаких видимых изменений.
Затем довели дозу коагулянта в каждом цилиндре до 15 см3, а довели дозу флокулянта в каждом цилиндре до 3 см3. Результат наблюдений не изменился.
При исследовании анионного флокулянта А2 в 9 мерных цилиндров емкостью 100 см3 наливали исследуемую воду до метки, затем в цилиндры добавляем различное количество миллилитров раствора сульфата алюминия из расчета получения различных его доз в диапазоне, охватывающем предполагаемую оптимальную дозу.
Содержимое во всех цилиндрах перемешивали быстрым вращением палочки в течение 15-20 секунд, не разбивая хлопок. Затем в течение 3-5 минут пробу медленно перемешивали также палочкой. Затем в каждый цилиндр добавляли исследуемый флокулянт из расчета получения различных его доз, проводили туже процедуру перемешивания, наблюдая за процессами образования хлопьев и их осаждением. Через 30 минут из каждого цилиндра отбирали из верхнего слоя пробу воды, фильтровали через обеззоленный фильтр «синяя лента» и определяли содержание в фильтрованной пробе концентрацию ХПК и рН. Результаты исследования эффективности работы анианных флокулянтов представлены в таблице 18.
Входе эксперимента было показано: при введении в сточную воду флокулянтов помимо коагулянтов улучшается процесс осаждения взвеси.
В данном исследовании изменяли дозировку и соотношение коагулянт – флокулянт. при увеличении расхода коагулянт-флокулянт эффективность коагуляции увеличивается. Но максимальная эффективность 33,9 % получена на минимальной дозировке обоих раегентов, поэтому следующие серии проводили в сторону снижения расхода коагулянта и флокулянта.
Наблюдая за процессами образования хлопьев и осаждения при введении различных флокулянтов, выбираем для дальнейшего исследования флокулянт А2, так как при его использовании образуются крупные быстрооседающие хлопья и он проявил более высокую эффективность даже без корректировки рН при подщелачивании.
Таблица 18 – Тестирование коагулянта и флокулянта А2
| № опыта | Дозировка коагулянта, см3/100см3 | Дозировка флокулянта, см3/100см3 | ХПК,мгО/дм3 | Эффективность удаления ХПК, % | рН |
| 1 | 5 | 1 | 1068 | 33,9 | 4 |
| 2 | 10 | 1 | 1224 | 24,3 | 4 |
| 3 | 15 | 1 | 1421 | 12,1 | 4 |
| 4 | 5 | 2 | 1258 | 22,2 | 4 |
| 5 | 10 | 2 | 1168 | 27,7 | 4 |
| 6 | 15 | 2 | 1184 | 26,7 | 4 |
| 7 | 10 | 4 | 1108 | 31,4 | 4 |
| 8 | 15 | 4 | 1070 | 33,8 | 4 |
| 9 | 20 | 4 | 1142 | 29,3 | 4 |
Таким же образом испытывали серию катионных флокулянтов, но уже с подщелачиванием. Выбрали наиболее активный, который проявил эффективность уже на низких значениях рН.
3.6.1.2 Подбор дозировки флокулянта
Дозировку реагентов проводили по схеме, представленной в таблице 19.
Таблица 19 План эксперимента по изучению процесса коагуляции-флокуляции СВ
| № опыта | Коагулянт | Флокулянт | |||
| 1 | + | 5 см3 | – | 0,5 см3 | |
| 2 | – | 2 см3 | + | 1,0 см3 | |
| 3 | + | 5 см3 | – | 0,5 см3 | |
| 4 | – | 2 см3 | + | 1,0 см3 | |
Для исследования в 8 мерных цилиндров емкостью 100 см3 наливали исследуемую воду до метки, затем в цилиндры добавляли различное количество миллилитров раствора сульфата алюминия: максимальное 5 см3 и минимальное 2 см3 в соответствие с планом. Содержимое всех цилиндров смешиваем палочкой в течение 3 минут. Затем в первые 4 цилиндра добавляем катионный флокулянт К1 с дозировками: минимальная 0,5 см3 и максимальная 1 см3 в соответствие с планом эксперимента. В оставшиеся 4 цилиндра добавляем анионный флокулянт А2 с дозировками: минимальная 0,5 см3 и максимальная 1 см3. Содержимое всех цилиндров медленно перемешивали палочкой в течение 3-5 минут и наблюдали за процессами образования хлопьев.
Хлопьеобразование было слабым. при введении в воду сульфата алюминия щелочность воды в пробе снижалось, то есть требовалось подщелачивание. Поэтому для обеспечения удовлетворительного уровня щелочности добавляли в исследуемую воду 5 капель индикатора – фенолфталеина и подщелачиваем воду 33% раствором NaOH до появления розовой окраски.
После подщелачивания хлопьеобразование сразу стало интенсивным, стали образовываться крупные, быстро оседающие хлопья, надосадочная жидкость стала прозрачней. В цилиндрах, где была максимальная дозировка коагулянта хлопья оседали быстрее. Надосадочная жидкость прозрачней в цилиндрах, где минимальная доза коагулянта. Если сравнивать флокулянты, то надосадочная жидкость прозрачнее в цилиндрах с добавлением флокулянта А2, но осаждение происходило быстрее при введении катионного флокулянта..

Рисунок 4 – Флокулянт К1 после первого подщелачивания

Рисунок 5 – Флокулянт А2 после первого подщелачивания
Определив рН полученных растворов с помощью индикаторной бумаги, взяли пробу воды для определения концентрации ХПК – определения эффективности коагуляции.
Затем в каждый цилиндр добавили еще 33% раствора NaOH по 2 см3 и снова осторожно смешали палочкой. Оставили на 30 минут для отстаивания.
Затем определяли рН растворов с помощью индикаторной бумаги и отбирали пробу воды для определения концентрации ХПК.
Подщелачивание усилило эффективность осветления воды в цилиндрах с минимальной дозой коагулянта: прозрачность надосадочной жидкости улучшилась.
3.6.1.3 Исследование биокоагуляции СВ
На заключительной стадии эксперимента после проведения процесса химической коагуляции–флокуляции добавляли в каждый цилиндр по 10 см3 активного ила, осторожно перемешав палочкой. Оставляли на 30 минут для отстаивания, после чего определяем рН растворов с помощью индикаторной бумаги. Отбирали пробу воды для определения концентрации ХПК.
Результаты представлены в таблицах 20 и 21.

Рисунок 6 – Флокулянт К1 после второго подщелачивания
Таблица 20 Изменение ХПК при испытании флокулянта К1
| № Опыта | Дозировка | ХПК после подщелачивания, мгО/дм3 | рН после подщелачивания | ХПК после введения ила, мгО/дм3 | рН после введения ила |
| Исходная | | 1616 | | 1616 | |
| 1 | «+ +» | 1672 | 5 | 1308 | 5 |
| 2 | «– –» | 1492 | 9 | 1484 | 9 |
| 3 | «+ –» | 1518 | 5 | 1408 | 5 |
| 4 | «– +» | 1488 | 8 | 1446 | 9 |