Файл: Zантn 5302 Заманауи аналитикалы химияны теориялы негіздері пнінен Дрістер жинаы шымкент, 2023 растырушылар философия докторы (PhD) х.. к., Шертаева Н. Т. Заманауи аналитикалы химияны теориялы негіздері.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 30.11.2023
Просмотров: 288
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Қолдану тәсілі бойынша индикаторлар ішкі және сыртқы болып екіге бөлінеді. Үздіксіз талданатын ерітінді құрамына тікелей кіретін индикаторлар, ішкі деп аталады. Кейбір жағдайларда, индикаторды талданатын ерітіндіге қосуға болмайды. Онда осы ерітіндінің бір-екі тамшысын іріктеп алып, сосын индикатормен қанықтырылған арнайы қағазға салады, немесе индикатордың ерітіндісімен ақ фарфор пластинкада немесе әдеттегі сүзгі қағазда араластырады. Қолданылған индикатор талданатын ерітіндіге қатысты сыртқы болып табылады.
Бақыланатын әсердегі табиғатына сәйкес түсі- түрлі-түсті; жарқылдау — хемилюминесцентті және флуоресцентті индикаторларды; гетерофазаны құрушы индикаторларды (жеке жағдайларда — шөгінді) айырады және оның қасиеттерінің өзгеруі — шөгінді түзуші, лайлану, абсорбциялық.
Лекция 9. Сандық химиялық талдау
1.Тотығу-негізгі титрлеу (протолитометрия)
2.Кешіндінометриялық титрлеу
3. Тотығу-қалпына келтіру титрлеуі (оксидиметрия)
4. Тұндыру титрлеуі
1.Тотығу-негізгі титрлеу (протолитометрия)
Қышқылдық-негіздік титрлеу әдістері қышқылдардың және негіздердің өзара реакцияласын пайдалануға негізделген. Жалпы түрде бұл реакцияны келесі түрде жазуға болады:
Н3О+ + В → ВН+ + Н2О; немесе Н3О+ + ОН- → 2Н2О;
Қолданылатын титрантқа байланысты ацидиметриялық және алкалиметриялық титрлеу түрлері болады. Ацидиметриялық титрлеу әдісінде (acidum - қышқыл) титрант ретінде НСІ-ның және Н2SО4-ның 0,1 және 0,01 н ерітінділері қолданылады. Алкалиметриялық титрлеуде (alkalis - сілті) – NаОН-нің және Ва(ОН)2-нің 0,1 және 0,01 н ерітінділері қолданылады.
Индикаторлар – реакция жүріп жатқан ортаның қасиетінің өзгеруіне байланысты өзінің құрылысын және сондықтан өзінің физикалық қасиеттерін өзгертетін заттар. Көп жағдайда индикатордың түсі өзгереді, кейде люминисценция люминесценция байқалады. Қышқылдық-негіздік титрлеудің индикаторлары ортаның рН-нің мәні өзгергенде құрылымдарын және қасиеттерін өзгертеді. Оларды осыңан сәйкес қышқылдық-негіздік индикаторлар деп атайды. Протолиттік теория тұрғысынан қарастырғанда олардың қышқылдық НJnd және негіздік Jnd типтес индикаторлары болады. Ерітінділерде индикаторлар иондалған және иондалмаған күйде болады. Олар өз-ара тепе-теңдікте болады. Бұл тепе-теңдіктің ығысуы ортаның рН-нің мәніне тәуелді және константамен сипатталады.
Титрлеуді жүргізу барысында келесі сұрақтар туындайды:
1.Затты анықтау үшін титриметриялық әдісті қолдануға болады ма ?
2.Егер мүмкін болса, онда қандай индикаторды қолданған дұрыс ?
Бұл сұрақтарға жауап беру үшін қышқылдық-негіздік титрлеудің қисықтарын тұрғызу және оны талдау керек. Бұл қисықтар титранттың көлемінің және ортаның рН-нің мәнінің өзара тәуелділігі болып табылады. Титрлеудің қисықтарын тұрғызу үшін титрленетін ерітіндінің орасының рН-нің мәнін есептейді. рН-нің есептеу барысында титриметриялық қоспаның құрамын, қышқылдардың және негіздердің константаларын және титрленген заттың бөлігін ескереді.
Титрлеудің қисықтары титрлеудің барысында қоспадағы болып жатқан үрдістер туралы мағлұмат алуға мүмкіндік береді. Сондықтан қышқылдық-негіздік титрлеудің әдісін және осыған сәйкес индикатордың белгілі бір түрін қолдану мүмкіндігін анықтайды. Титрлеудің келесі түрлері болады: күшті қышқылдарды күшті негіздермен титрлеу қисықтары; әлсіз қышқылдарды және негіздерді титрлеу; полипротондық қышқылдарды және негіздерді, қышқылдардың және енгіздердің қоспаларын титрлеу;
2.Кешіндінометриялық титрлеу
Комплексон деп аталатын кейбір органикалық реактивтермен комплекстік қосылыстар түзетін иондарды анықтау реакцияларына комплексонометрия негізделген. Мұнда өте берік, суда жақсы еритін комплекстік қосылыстар түзіледі. Әдіс тездігімен және жоғарғы дәлдігімен ерекшеленеді.
Комплексондар аминополикарбон қышқылдарының туындысы болып табылады.
Комплексонометриялық титрлеу ертеректен белгілі. Алғашқы жұмыстар иодид иондарын анықтауға жатады.
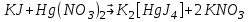
1851 жылы Либих цианидтерді күміс нитраты ерітіндісімен комплексонометриялық анықталу туралы жазды:
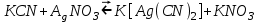
Бейорганикалық титранттар қазіргі уақытта шектеулі қолданылады. Оларды ең кең тарағаны хлоридтерді, бромидтерді, роданидтерді, цианидтерді және тиомочевинаны меркуриметриялық титрлеу әдісі.
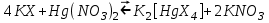
Органикалық тиранттар айтарлықтай көп таралған. Соңғы уақытта тиолдар, купферон, дитизон және басқалар қолданылып жүр.
Олардың комплекстерге қарағанда артықшылығы арнайылығында. Органикалық комплекс түзушілерді қолданылатын титриметриялық әдістерде эквиваленттік нүктесін металлохромдық индикатормен анықтайды.
Комплексонометрия реакцияларына қойылатын жалпы талаптар барлық титриметриялық әдістегілерге ұқсас: - олар тез, соңына дейін, қосымша процестерсіз және т.с.с. өтуі керек.
Комплесонометриялық әдістің сұрыпталуы әдетте үлкен емес және қандай донорлық атомдар катионмен әректесуде қатысатынына байланысты. Иодидтер кейбір элементтермен ғана
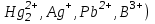 тұнба және комплекстер түзетін болғандықтан, калий иодидімен титрлеу жоғарғы сұрыпталуға алып келеді. Аммиак және полиаминдердің де, әсіресе, комплексондарға қарағанда сұрыпталуы бойынша ерекшелігі үлкен, себебі ол элементтердің аз санымен тұрақты комплестер түзеді.
тұнба және комплекстер түзетін болғандықтан, калий иодидімен титрлеу жоғарғы сұрыпталуға алып келеді. Аммиак және полиаминдердің де, әсіресе, комплексондарға қарағанда сұрыпталуы бойынша ерекшелігі үлкен, себебі ол элементтердің аз санымен тұрақты комплестер түзеді.ЭДТА қолданған алғашқы титриметриялық методикаларда кәдімгі қышқылды-негіздік индикаторлар пайдаланылған, себебі ЭДТА-ның артық мөлшері металл тұзының бейтарап ерітіндісіне қосылады да реакция нәтижесінде тиісті мөлшерде бөлініп шыққан сутек иондары титрленген. Бұл әдіс кейбір жағдайларда қазір де қолданылады.
Комплексонометрияның қарқынды дамуы металлохромды индикаторлардың ашылуымен байланысты. Бұл заттар металл иондарымен әрекеттескенде боялған қосылыстар түзеді, бірақ комплексонаттарға қарағанда беріктігі нашарлау. Металл иондармен комплекс түзетін индикаторларды бос иондардан немесе индикатор молекуларынан түсі бойынша ажыратады.
Бұл индикатордың алғашқылары мурексид (МУР) болды – пурпур қышқылының аммоний тұзы. Оның қолданылуы Шверценбахтың лабораториядағы кездейсоқ зерттеуіне негізделген.
Кальций тұздарымен сарғыш-қызыл түсті кальций пурпуреаты түзіледі. Пурпур қышқылы үш негізді. Оның константалары: рK=0; pK2=9,2 және pK3=10,9. 0,1 M пурпуреат аммонийдің сулы ерітінділері 12-15 күнде ыдырайды. Индикатордың ерітінділерін анализдің алдында ғана даярлайды. Мурексид өлшендісін өлшеу ыңғайлы болу үшін оны натрий хлоридімен араластырады, анализденетін ерітіндіде оның концентрацисы жоғары болмау қажет, себебі бұл жағдайда индикатордың өту интервалының анықтығы нашарлайды. Мурексид ерітіндісіндегі тепе-теңдікті сызба нұсқада жазамыз.
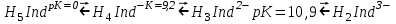
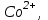
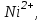
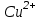 сары түсті комплекстер түзеді және оларды индикатор түсі сарыдан көгілдір күлгінге өткенше аммиакты ортада комплексонмен титрлейді. Реакцияны жылдамдату үшін титрлеуді жоғары температурада жүргізеді. Мурексидпен комплекстердің құрамы ерітіндінің рН-ына байланысты. Мурексидпен комплекстердің құрамы ерітіндінің рН-ына байланысты. Мысалы, мырыш әлсіз сілтілік ортада 1:1 комплексін, ал сілтілік ортада 1:2 түзеді.
сары түсті комплекстер түзеді және оларды индикатор түсі сарыдан көгілдір күлгінге өткенше аммиакты ортада комплексонмен титрлейді. Реакцияны жылдамдату үшін титрлеуді жоғары температурада жүргізеді. Мурексидпен комплекстердің құрамы ерітіндінің рН-ына байланысты. Мурексидпен комплекстердің құрамы ерітіндінің рН-ына байланысты. Мысалы, мырыш әлсіз сілтілік ортада 1:1 комплексін, ал сілтілік ортада 1:2 түзеді.
Комплексонометрияда эриохром қара Т-ны кеңінен қолданады, бұл азобояғыш және оның молекуласында хелат түзуші топтар бар:
Сульфаттың протоны ерітіндіде толық диссоциацияланады, ОН—тобынан протондардың әрі қарай үзілуі, индикатор түсінің өзгеруіне алып келеді, ол ерітіндінің рН-на тәуелді:
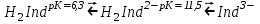
Аммиакты ерітіндіде басым анион металл иондарымен әрекеттеседі де қызыл немесе күлгін түсті бояулы қосылыс түзеді.
Комплексонометриялық титрлеу үшін қышқыл хром көк Т индикаторы ұсынылған. Олар кальций, мырыш, қорғасын, марганец және магний иондарымен қызыл түсті комплекс ішілік қосылыстар түзеді және оларды титриметриялық анықтау үшін 1 -дық спирттік ерітінді түрінде қолданады (рН 12). Қышқыл ортада олар сарғыш қызыл.
Комплексонометриялық титрлеудің соңғы нүктесін индикатордың жалпы түрі төмендегідей өрнектелетін тиісті комплекс түзуші константасы бар комплекс түзеді:
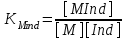
Түсінің өзгеруі шамамен [MInd]=[Ind] болады да, ал өту нүктесі рМТ мына арақатынаспен анықталады:
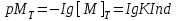
Көп сатылы комплекс түзілуі процесі үшін шартты константаны а-ның комплекстенген функциясы арқылы шығаруға болады:
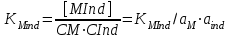
Онда
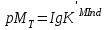
Индикатордың металмен комплекстерінің беріктігі ерітіндінің рН-на тәуелді. Титрлеу процесінде металдың индикатормен комплексі бұзылып, титрантпенен беріктеу комплекс түзіледі, титрлеудің соңғы нүктесіне ерітінді түсі өзгереді.
Қателіктер өте аз болуы үшін, төмендегі талаптар орындалуы қажет: металдың индикатормен комплексінің шарты тұрақтылық комплексінің мәні
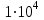 көп болуы қажет; КМҮ және КMind тұрақтылық константалары бірнеше ретке ерекшеленуі керек; индикаторды ион концентрациясын 1 %-тен артық емес мөлшерде қосқанда ерітіндінің бояуының қанықтығын қамтамасыз етілуі керек; титрленгенде ерітіндіні сұйылту тек қана рМТ>рМэкв мақсатқа сай орындалуы керек.
көп болуы қажет; КМҮ және КMind тұрақтылық константалары бірнеше ретке ерекшеленуі керек; индикаторды ион концентрациясын 1 %-тен артық емес мөлшерде қосқанда ерітіндінің бояуының қанықтығын қамтамасыз етілуі керек; титрленгенде ерітіндіні сұйылту тек қана рМТ>рМэкв мақсатқа сай орындалуы керек.Комплексонометрияны қолдану. Судың жалпы кермектігін анықтау. Комплексонометрияда қолданылатын ерітінділер – ЭДТА-ның 0,1 М; 0,05 М; 0,01 М ерітінділері; магнийдің сульфатының 0,1 М; 0,05 М; 0,01 М ерітінділері; мырыштың сульфатының 0,1 М; 0,05 М; 0,01 М ерітінділері. ЭДТА ерітіндісін «Трилон Б» химиялық таза ұнтағынан нақты салмақ бойынша дистилденген суда дайындайды. Дистилденген судың құрамында кальцийдің және магнийдің тұздарының қсопалары болмауы керек. Еріткіш ретінде дистилденген судың жарамдылығын қышқылдық хромдық қара арнайы индикатордың көмегімен анықтайды. Ол үшін 100 см
3 суға 5 см3 аммиактық буферлік ерітінді және 0,1 г индикаторлық қоспаны қосады. Индикаторлық қоспаның құрамы индикатор:натрийдің хлориді – 1:500. Ерітіндінің түсі күлгін, 0,05 М ЭДТА ерітіндісінен 1-2 тамшы қосқанда көк түске өтеді. Ал 0,1 н. мырыштың сульфатының ерітіндісінен 1-2 тамшы қосқанда қайтадан күлгін түске өтеді. Егер осы сынаққа су жауап берсе, онда ол жарамды болып саналады. Басқа жағдайда жарамсыз болып табылған дистилденген суды КУ-2 катиониті бар бағаналардан өткізіп тазалайды.
ЭДТА-ның титрін өлшенген салмақ бойынша немесе стандарттар – мырыштың сульфаты, магнийдің сульфаты, кальцийдің карбонаты бойынша белгілейді.
Титрлеуді тікелей, кері және ығыстыру тәсілдері бойынша орындауға болады.
Техникалық, агрохимиялық анализ тәжірибесінде, тамақ өнеркәсібінде және халық шаруашылығының басқа салаларына су кермектігін комплексонометриялық анықтауды жиі қолданады, оны 1 л судағы қальций және магнийдің мг-эвиваленттерінің қосындысы санымен сипаттайды.
Анализді жасау үшін зерттелетін суды аммоний буферлік қоспамен рН-10 болғанша сілтілендіреміз. Индикатор ретінде арнайы хромоген қара ЕТ-00 ерітіндісін пайдаланады, ол Са2+ және Мg2+ иондарымен шарап қызыл түсті ерімтал комплекстер түзеді:
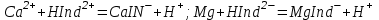
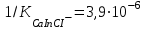
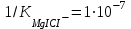
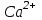 және
және 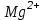 ЭДТА-мен тұрақсыздық константалары едәуір кіші
ЭДТА-мен тұрақсыздық константалары едәуір кіші 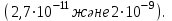 Сондықтан ЭДТА ерітіндісімен титрленгенде, ол тиісті комплекстерден индикаторды ысырып шығарып, одан да берік комплекстер түзеді. Реакция өтеді, босап шыққан индикатордың түсі көк.
Сондықтан ЭДТА ерітіндісімен титрленгенде, ол тиісті комплекстерден индикаторды ысырып шығарып, одан да берік комплекстер түзеді. Реакция өтеді, босап шыққан индикатордың түсі көк. 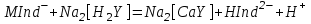
Сонымен эквиваленттік нүктесінде ерітіндінің шарап қызыл түсі көкке ауысады.
Табиғи суда титрлеу үшін, әдетте, 0,05 н ЭДТА жұмысшы ерітіндісін пайдаланады.
Ерітіндінің жалпы кермектігін мына формула бойынша есептейді:
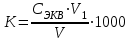
Мұндағы
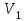 және
және 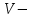 титрлеуге кеткен комплексон көлемі және анықтауға алынған су көлемі, мл.
титрлеуге кеткен комплексон көлемі және анықтауға алынған су көлемі, мл.