ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 03.12.2023
Просмотров: 189
Скачиваний: 10
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Вопросы и задания для самоконтроля
-
В чём заключается сущность явления фотоэффекта? -
Объясните принцип работы фотоэлемента с внешним фотоэффектом. -
Что такое «красная граница» фотоэффекта? Чем обусловлено её наличие и положение на шкале длин волн? -
Объясните причину различия вольтамперных характеристик в прямом направлении для разных световых потоков.
-
При каких условиях возникает ток насыщения? Изобразите вольтамперную характеристику фотоэлемента, включенного в обратном направлении. Объясните ее.
ЛАБОРАТОРНАЯ РАБОТА № 4
ИЗУЧЕНИЕ СПЕКТРА АТОМА ВОДОРОДА
И ОПРЕДЕЛЕНИЕ ПОСТОЯННОЙ РИДБЕРГА
ЦЕЛЬ РАБОТЫ:
Провести калибровку спектрометра; исследовать спектр атомарного водорода и неона; вычислить постоянную Ридберга.
КРАТКАЯ ТЕОРИЯ
Оптические свойства атомов определяются состоянием валентных электронов. Согласно современным представлениям, электроны в атомах могут находиться лишь в неких стационарных состояниях, которым соответствуют строго определенные дискретные значения энергии, называемые энергетическими уровнями. В простейшем случае, в атоме водорода имеется единственный электрон, который является валентным электроном.
Состояние атома в квантовой механике описывается волновой функцией φn, его энергия Еn. В случае простейшего атома – атома водорода, состоящего из протона и электрона, квантовая механика позволяет получить точные решения уравнения Шредингера
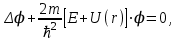 , , | | (4.1) |
где m – масса электрона, Е – полная энергия,
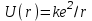 - энергия взаимодействия электрона с ядром, е – заряд электрона,
- энергия взаимодействия электрона с ядром, е – заряд электрона, 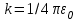 ,
, 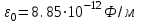 - электрическая постоянная. Решения уравнения (4.1) для атома водорода являются набором дискретных уровней энергии. Для связанных состояний (Еn<0):
- электрическая постоянная. Решения уравнения (4.1) для атома водорода являются набором дискретных уровней энергии. Для связанных состояний (Еn<0): 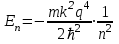 , , | | (4.2) |
где
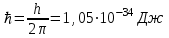
, n =1,2,3,…- главное квантовое число.
С ростом числа n уровни энергии атома сближаются, в пределе при
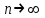 дискретный спектр приближается к непрерывному, а квантовая система к классической. Это и есть принцип соответствия Бора, который позволяет выразить энергию электронов в атоме через фундаментальные постоянные. Для простоты Бор принял, что в атоме водорода электроны вращаются вокруг протона по окружности радиусом r с циклической частотой ω:
дискретный спектр приближается к непрерывному, а квантовая система к классической. Это и есть принцип соответствия Бора, который позволяет выразить энергию электронов в атоме через фундаментальные постоянные. Для простоты Бор принял, что в атоме водорода электроны вращаются вокруг протона по окружности радиусом r с циклической частотой ω: 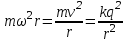 . . | | (4.3) |
Согласно правилу квантования момента импульса электрона в атоме:
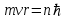 . . | | (4.4) |
Решение уравнений (4.3) и (4.4) дает выражение для радиусов круговых орбит электронов в атоме водорода:
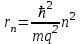 . . | | (4.5) |
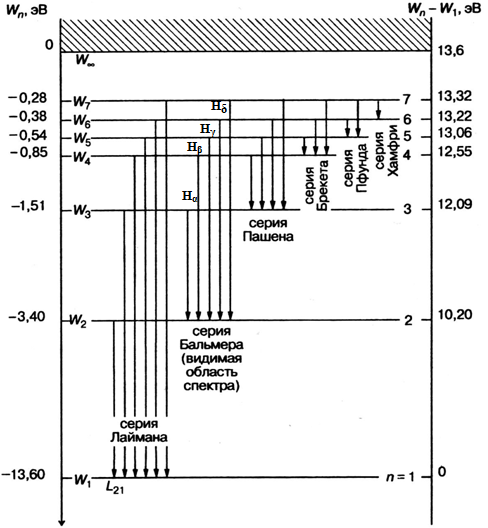
Рис.4.1. Энергетическая диаграмма атома водорода
Таким образом, при переходе атома водорода из состояния n2 c энергией Е2 в состояние n1 с энергией Е1 действует правило частот Бора:
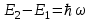 , , | | (4.6) |
то есть испускается фотон с частотой ω и длиной волны λ
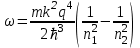 , , | | (4.7) |
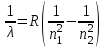 . . | | (4.8) |
Здесь введено обозначение
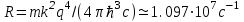 - постоянная Ридберга. Формула (4.8) называется формулой Бальмера-Ритца. В этой формуле с увеличением n2 и n1 разность между волновыми числами
- постоянная Ридберга. Формула (4.8) называется формулой Бальмера-Ритца. В этой формуле с увеличением n2 и n1 разность между волновыми числами
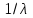 уменьшается, стремясь при
уменьшается, стремясь при 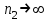 к предельному значению 0. При этом линии сближаются, и уменьшается их интенсивность.
к предельному значению 0. При этом линии сближаются, и уменьшается их интенсивность. Совокупность длин волн (или частот), излучаемых телом, называют спектром излучения этого тела. Как мы видим, вследствие квантования энергетических уровней электронов в атомах атомарные спектры излучения состоят из дискретного набора длин волн (частот). Такие спектры называются линейчатыми. Совокупность спектральных линий, т.е. длин волн или частот, соответствующих переходам на один и тот же энергетический уровень n1 образует серию линий:
- совокупность переходов в основное состояние (n1 =1) образует серию Лаймана;
- переходы в состояние с n1 =2 образуют серию Бальмера;
- переходы в состояние с n1 =3 образуют серию Пашена.
Визуально мы можем наблюдать только серию Бальмера: для водорода – n1 = 2, n2 = 3,4,5…(рис.4.1).
Выполнение работы:
Внешний вид установки для определения спектральных характеристик атомов показан на рис. 4.2. На оптической скамье 1 соосно установлены источник света (поочередно ртутная, неоновая и водородная лампы) и приемник-анализатор 3 с микрометрическим винтом 4, задающим исследуемую длину волны, и окуляром для наблюдения 5.
Измерения с помощью микрометрического винта
Микрометрический винт имеет два отсчетных устройства. Первое отсчетное устройство состоит из шкалы с ценой деления 0,500 мм, нанесенной на стебле 1 , как показано на рис.4.3, и указателя, которым является торец барабана 2. Второе отсчетное устройство состоит из шкалы, с ценой деления 0,010 мм, нанесенной на конусной поверхности барабана 2, и указателя в виде продольного штриха, нанесенного на стебле 1. Шаг микровинта S = 0,500 мм, следовательно, одному обороту микровинта и жестко скрепленного с ним барабана соответствует линейное перемещение торца барабана на одно деление, равное 0,500 мм. Круговая шкала барабана имеет число делений n=50 и следовательно, поворот барабана с микровинтом на одно деление относительно продольного штриха стебля 1 рис.2 будет соответствовать величине 0.500/50 10 мкм. Это цена деления прибора. Для проведения измерений производят отсчеты по двум отсчетным устройствам и суммируют их. Примеры отсчета показаны на рис.4.3.

Рис.4.2. Вид установки для измерения постоянной Ридберга
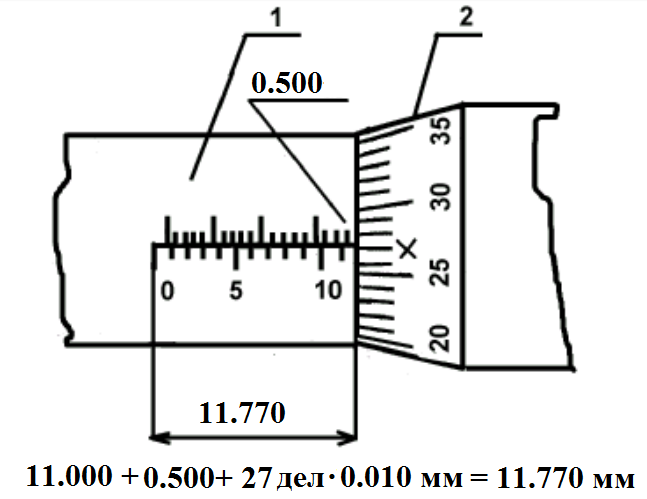 | 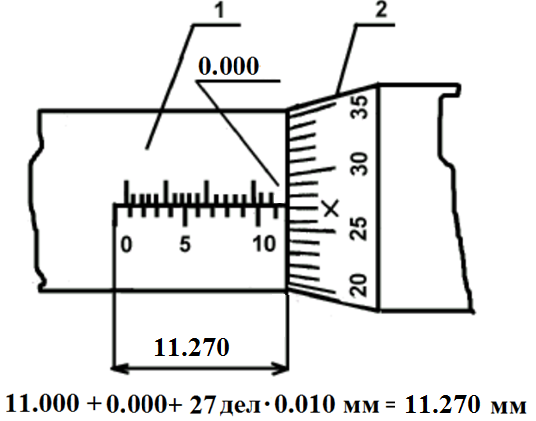 |
| Рис.4.3.Измерение с помощью микрометрического винта | |
Для проведения измерений необходимо провести калибровку спектрометра по известному спектру ртутной лампы.
-
Установить на оптической скамье ртутную лампу в качестве источника излучения. С помощью регулировочных винтов добиться одинакового уровня источника излучения и бленды фотоприемника. Установить головку микрометрического винта в ближайшее к корпусу положение (УФ область спектра). -
Осторожно вращая головку винта и наблюдая в окуляр, найти максимум крайней фиолетовой линии спектра, отвечающий 404.7 нм. Записать положение винта в таблицу 4.1.
Таблица 4.1. Градуировка спектрометра
№ | Цвет линии | Длины волн линий спектра ртути λ, нм | Положение микрометрического винта d, мкм |
| 1 | Фиолетовый | 404.7 | |
| 2 | Фиолетовый | 407.8 | |
| 3 | Сине-фиолетовый | 435.8 | |
| 4 | Голубой | 491,6 | |
| 5 | Зеленый | 546.0 | |
| 6 | Желтый | 576.9 | |
| 7 | Желтый | 579.0 | |
| 8 | Оранжевый | 623.4 | |
| 9 | Красный | 671.0 | |
| 10 | красный | 690.7 | |
-
Повторить измерения для указанных в таблице линий спектра. -
Считая калибровочную зависимость λ(d) линейной функцией, определить ее угловой коэффициент и свободный член с помощью метода наименьших квадратов. Выбрав достаточно крупный масштаб, построить зависимость λ(d) на миллиметровой бумаге формата А4.
Наблюдение спектра неоновой лампы