Файл: Научноисследовательская работа студентки 4 курса Направления подготовки 06. 03. 01 Биология Профиль Биохимия.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 04.12.2023
Просмотров: 198
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
СОДЕРЖАНИЕ
Уравнения кривой оксигенации гемоглобина
Определение параметров взаимодействия гемоглобина с протонами водорода (эффект Бора)
Определение начальных условий для распределения кислорода в гемоглобине
ГЛАВА 2 МЕХАНИЗМЫ РЕГУЛЯЦИИ СВЯЗЫВАНИЯ ГЕМОГЛОБИНА С КИСЛОРОДОМ
2.1. Модельные представления, используемые для описания взаимодействия гемоглобина с кислородом
2.2. Свободная энергия системы гемоглобин – лиганды
2.3. Описание неравновесных процессов взаимодействия гемоглобина с кислородом
Определение начальных условий для распределения кислорода в гемоглобине
Согласно обзору данных, мембрана эритроцита вопреки известным предположениям не является причиной замедления диффузии кислорода. Измерение коэффициента диффузии кислорода через мембрану эритроцитов дало цифру 0.7-КГ см1 І с, что примерно в 5 раз меньше чем для воды. Чтобы объяснить фактическое замедление диффузии, коэффициент должен быть примерно в 100 раз меньше, чем у воды, т. е. порядка 1.2-10"7 елі2 /с. Как отмечает Мелдон, распространено мнение, что диффузию кислорода в эритроцит замедляет неподвижный слой молекул плазмы, прилегающий к мембране эритроцита снаружи и достигающий толщины 5 мкм. В работе [10], показано, что слой жидкости между стенкой легочного капилляра и эритроцитом не превышает в среднем 0.15 мкм. Кроме того, при прохождении через капилляр эритроцит постоянно вращается в силу чисто физических причин. Поэтому слой жидкости как препятствие диффузии кислорода можно рассматривать лишь для экспериментальных условий в искусственной среде. Препятствием диффузии может служить сама «толща» гемоглобина. Кроме того, по мнению [2] важное значение имеет различие кислородсвязывающих свойств гемоглобина в эритроците и растворе. Высокая концентрация гемоглобина в эритроците (около 33%), наличие солей, ДФГ и других веществ уменьшают его сродство к кислороду и замедляют соответствующую реакцию. В растворе все вышеперечисленные факторы не действуют.
Модельные кривые хорошо описывают экспериментальными данными. В данном случае значение параметра а для процесса оксигенации составило: а = 0.9 10э м% /(с моль).
Здесь также наблюдается хорошее сравнение с экспериментом. Символы -экспериментальные данные для различного начального заполнения. Кривые моделирование. В данном случае значение параметра а для процесса диссоциации составило: а = 1.3 103 м3 /(с моль).
ГЛАВА 2 МЕХАНИЗМЫ РЕГУЛЯЦИИ СВЯЗЫВАНИЯ ГЕМОГЛОБИНА С КИСЛОРОДОМ
Наш организм потребляет в сутки примерно 400–600 л кислорода [1]; такое же его количество содержится в 100 тоннах воды. Если бы
наше сердце вместо крови перекачивало жидкость с таким же содержанием кислорода, то за каждое сокращение нужно было бы прокачивать 15 л этой жидкости. Представляете себе такой насос? Реальный сердечный выброс в 100 раз меньше. Такая фантастическая экономия возникает благодаря тому, что в нашей крови может раствориться в 100 раз больше кислорода, чем в воде. Для этой цели в организме имеются специальные клетки – эритроциты. В этом обзоре мы расскажем, как устроен эритроцит, обеспечивающий необыкновенно высокую эффективность транспорта кислорода.
Гемоглобин
Эритроциты занимают 40% объема нашей крови. Эти клетки в норме представляют собой двояковогнутые диски, на 98% заполненные красным белком– гемоглобином, связывающим кислород (рис. 1) [2]. Гемоглобин – относительно небольшой интенсивно окрашенный белок с молекулярной массой 66 000– 68 000 Дальтон [2–5]. Гемоглобина в крови так много, что он определяет ее цвет. Молекула белка состоит из четырех похожих субъединиц, каждая из которых способна обратимо связывать кислород [2, 3]. Для этого связывания не требуется энергия. Таким образом, каждая молекула гемоглобина способна связать от одной до 4 молекул кислорода.
Рисунок 8 – Электронная микрофотография эритроцитов [2]
Связывание кислорода с гемоглобином происходит в активном центре – геме (рис. 9). Гем – это изящная химическая конструкция, состоящая из четырех пятичленных гетероциклов, лежащих в одной плоскости. Четыре атома азота в этой плоской конструкции образуют в центре зону, которая хорошо связывает атом железа – главный элемент гемоглобина, который в свою очередь непосредственно связывает кислород. Химические связи железа с атомами азота не ковалентные, а координационные – более слабые. Это нужно для того, чтобы железо могло связывать кислород обратимо [2]. Электроны железа не должны перейти на кислород, иначе произойдет окислительно-восстановительная реакция между железом и кислородом. В результате мы потеряем кислород: он превратится в один из сильнейших окислителей на Земле – супероксид-радикал, способный натворить много бед. Координационные связи в силу своей слабости достаточно хорошо удерживают кислород в геме, но не отдают ему свои электроны.
Еще одна важная особенность гема состоит в том, что одинарные и двойные связи в нем чередуются. В результате возникает система делокализованных электронов. Множество электронов, образующих
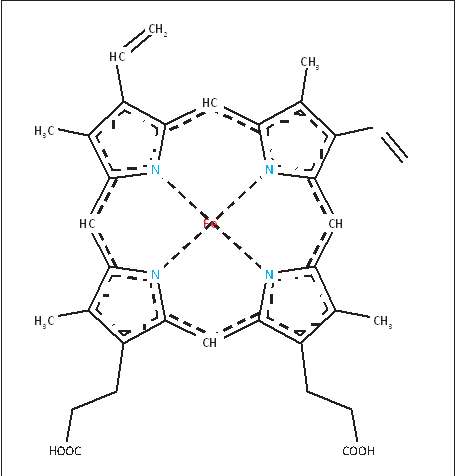
Рисунок 9 – Структура молекулы гема; пунктиром показаны связи, образующие делокализованную систему электронов [2]
химические связи между атомами гема, оказываются принадлежащими всему кольцу – это создает уникальную возможность легко менять электронные свойства всей молекулы в целом и в первую очередь атома железа за счет слабых влияний соседних химических групп [2]. Возможность управлять электронным состоянием железа позволяет изменять способность железа связываться с кислородом.
Атом железа может образовать 6 координационных связей; в геме четыре из них лежат в плоскости кольца и связывают железо с азотами; две другие перпендикулярны плоскости кольца (рис. 3). Одна из этих связей используется для связывания кислорода (рис. 3 Б), а противоположная ей – связь железа с азотом гистидина, занимающего 93-е положение в последовательности аминокислотных остатков глобина (так называется белковая часть молекулы гемоглобина), – как раз и позволяет управлять связыванием железа-скислородом [2, 4]. Посколькугистидин 93 является частью глобина, конформационные изменения этой молекулы могут изменять положение гистидина относительно плоскости кольца гема. В отсутствие кислорода конформация глобина такова, что гистидин 93 несколько вытягивает железо из плоскости кольца на себя (рис. 3 А). В этом состоянии гем хуже связывает кислород, чем в ситуации, когда железо находится в плоскости кольца. Таким образом, конформация белковой молекулы влияет на силу связывания кислорода.
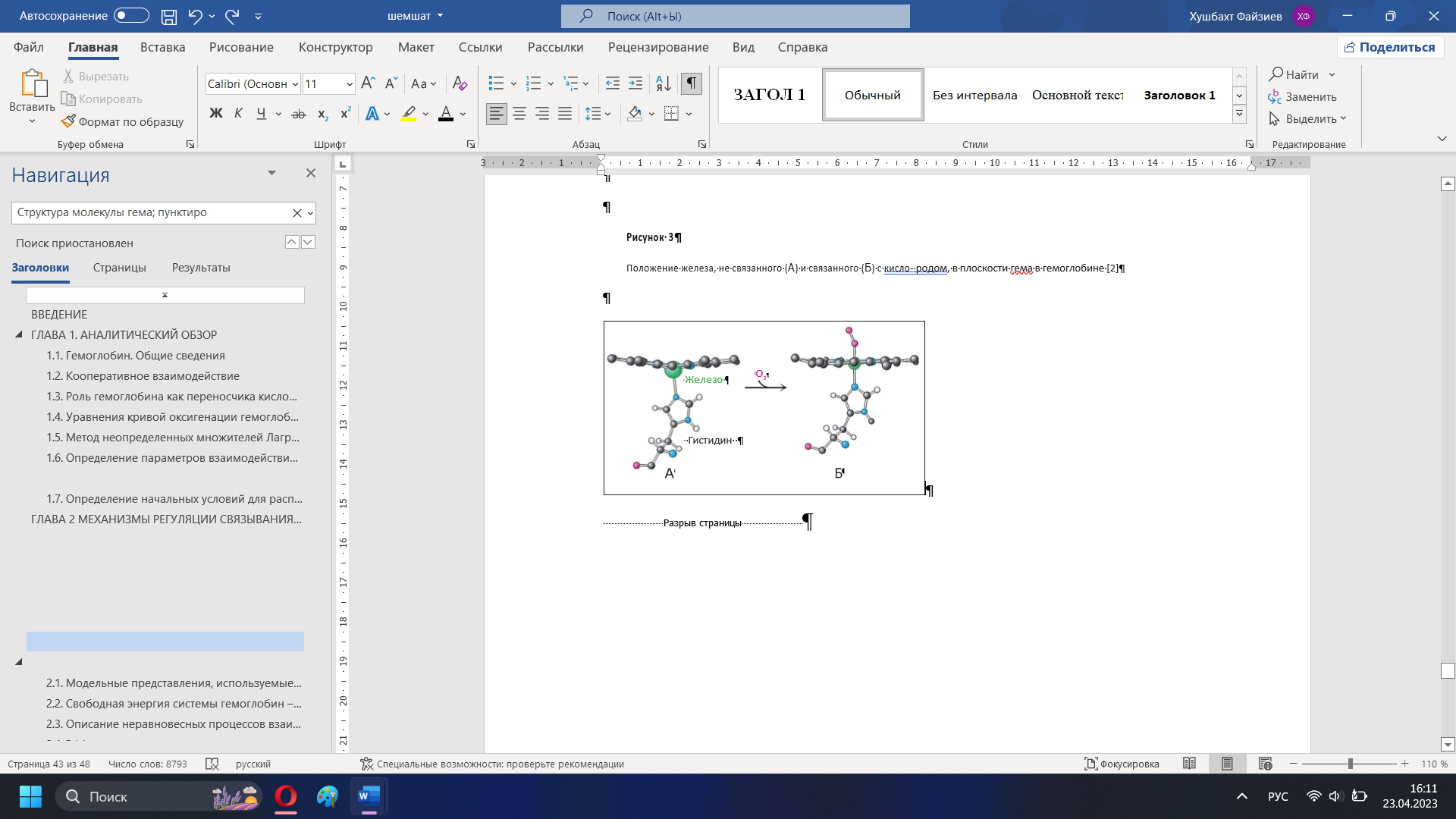
Рисунок 3 – Положение железа, не связанного (А) и связанного (Б) с кислородом, в плоскости гема в гемоглобине [2]
Эта сила важна, так как организм может использовать только свободный, не связанный с гемоглобином кислород. Поэтому важно не только то, сколько кислорода есть в крови в целом и как гемоглобин его связывает, но и как он кислород отдает. Поскольку в легких растворимого кислорода больше всего, там доминирует связывание. По мере того, как кровь из легких поступает в другие органы и по капиллярам расходится по разным тканям, растворенный в крови кислород потребляется клетками, уходит из крови внутрь клеток, концентрация его уменьшается. Равновесие гемоглобина с кислородом сдвигается в сторону отдачи кислорода. Кислород освобождается и выходит в кровь [1, 6]. Молекулярная регуляция, определяющая конформацию гемоглобина и его способность связывать и отдавать кислород, позволяет более эффективно регулировать процесс переноса кислорода из легких в ткани.
Рассмотрим, как это происходит (рис. 4). Кислород связывается с гемоглобином обратимо, поэтому доля гемоглобина, связанного с кислородом, зависит от давления кислорода в крови (его концентрации). Это давление в легких (100 мм рт. ст., или 100 torr) гораздо выше, чем аналогичное давление в тканях в покое (20–30 torr) [1, 2]. Организму нужен такой гемоглобин, который будет максимально связывать кислород в легких и отдавать большую его часть в тканях, ибо та часть гемоглобина, которая связала кислород и не отдала его в тканях, представляет собой балласт – мы зря гоняем груженые вагоны из легких в ткани и обратно. Закономерности этого обмена определяются двумя основными параметрами кривой связывания гемоглобина с кислородом. Эта кривая имеет S-образную форму и описана уравнением Хилла (1) [4, 7]:
HbО2/Hb0 = [P]n/([P]n+[P50]n) (2),
где HbO2 – концентрация гемоглобина, связанного с кислородом; Hb0 – полная концентрация гемоглобина; Р – давление кислорода в крови (величина, пропорциональная концентрации кислорода); Р50 – давление кислорода, при котором гемоглобин насыщен кислородом наполовину; n – коэффициент в формуле Хилла (1).
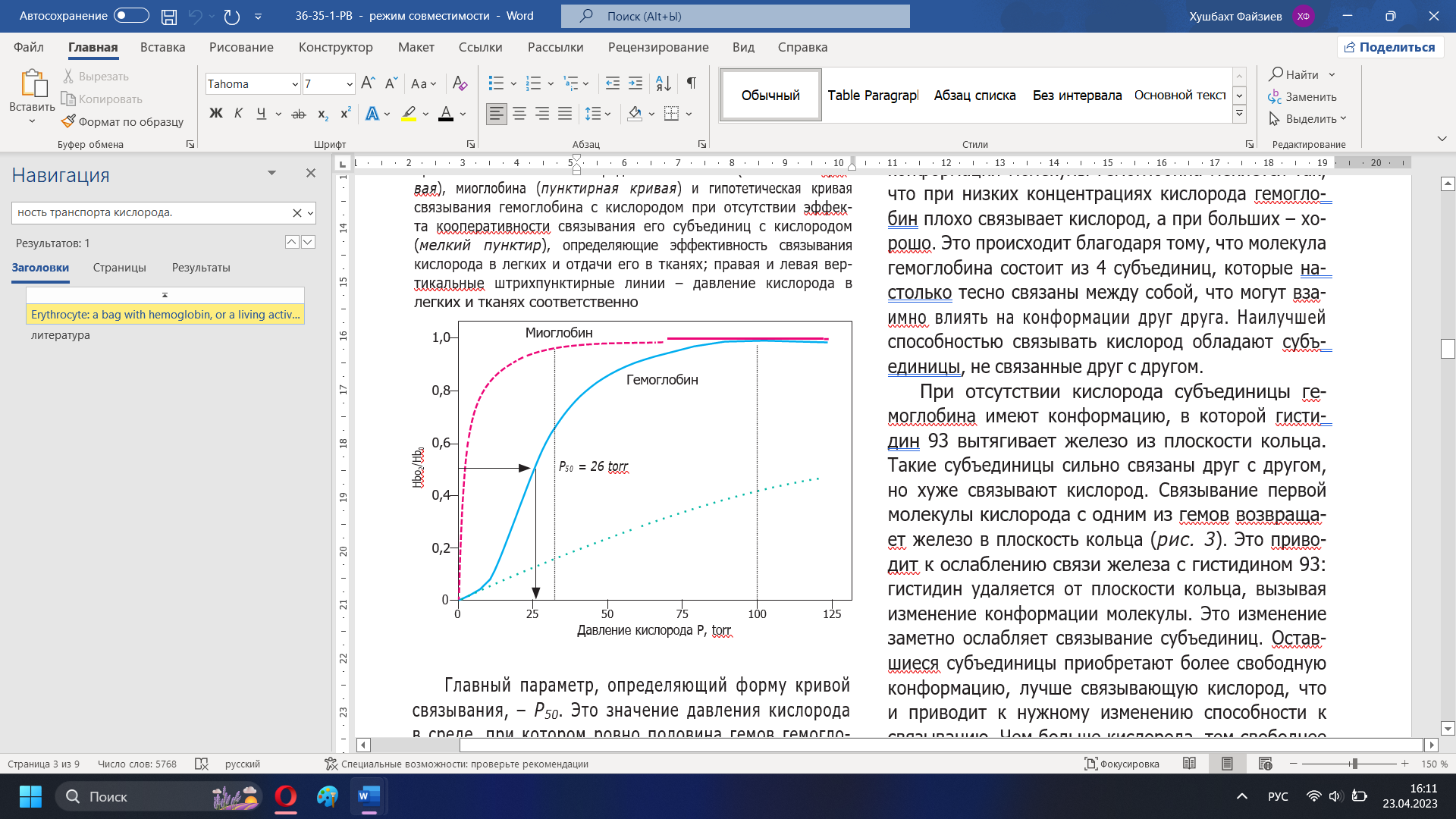
Рисунок 11 – Кривые связывания с кислородом гемоглобина (сплошная кривая), миоглобина (пунктирная кривая) и гипотетическая кривая связывания гемоглобина с кислородом при отсутствии эффекта кооперативности связывания его субъединиц с кислородом (мелкий пунктир), определяющие эффективность связывания кислорода в легких и отдачи его в тканях; правая и левая вертикальные штрихпунктирные линии – давление кислорода в легких и тканях соответственно
Главный параметр, определяющий форму кривой связывания, – Р50. Это значение давления кислорода в среде, при котором ровно половина гемов гемоглобина насыщена кислородом. На рисунке 9 показано, как определяется эта величина.
Второй важный параметр этой кривой – коэффициент Хилла, или коэффициент кооперативности.
Как уже было сказано, кривая связывания гемоглобина с кислородом имеет S-образный характер (сплошная линия на рис. 4) и не похожа на кривую обычного химического связывания (пунктир на рис. 4). Связывание, характерное для гемоглобина, называют кооперативным. При низких концентрациях кислорода кривая с увеличением его концентрации растет медленно – гемоглобин плохо связывает кислород. Постепенно, при увеличении концентраций кислорода, кривая становится все круче. В области концентраций кислорода, близких к Р50, гемоглобин значительно эффективнее (резче) связывает или отдает кислород по сравнению с некооперативным сорбентом. S-образность характеристики помогает гемоглобину сильнее связывать кислород в легких и больше отдавать его в тканях, чем это могло бы быть при отсутствии кооперативности. Если бы S-образность была более выраженной, эффективность переноса была бы еще больше. Неполная отдача кислорода, видимо, физиологически обоснована – это запас для быстрого увеличения его потребления. Увеличение физиологической нагрузки, сопряженное с увеличенным потреблением кислорода
, снизит концентрацию кислорода в тканях, что позволит отнять у гемоглобина больше кислорода.
На молекулярном уровне S-образность кривой связывания гемоглобина с кислородом означает, что конформация молекулы гемоглобина меняется так, что при низких концентрациях кислорода гемоглобин плохо связывает кислород, а при больших – хорошо. Это происходит благодаря тому, что молекула гемоглобина состоит из 4 субъединиц, которые настолько тесно связаны между собой, что могут взаимно влиять на конформации друг друга. Наилучшей способностью связывать кислород обладают субъединицы, не связанные друг с другом.
При отсутствии кислорода субъединицы гемоглобина имеют конформацию, в которой гистидин 93 вытягивает железо из плоскости кольца. Такие субъединицы сильно связаны друг с другом, но хуже связывают кислород. Связывание первой молекулы кислорода с одним из гемов возвращает железо в плоскость кольца (рис. 3). Это приводит к ослаблению связи железа с гистидином 93: гистидин удаляется от плоскости кольца, вызывая изменение конформации молекулы. Это изменение заметно ослабляет связывание субъединиц. Оставшиеся субъединицы приобретают более свободную конформацию, лучше связывающую кислород, что и приводит к нужному изменению способности к связыванию. Чем больше кислорода, тем свободнее субъединицы и тем лучше связывание [4]. Таким образом, субъединицы гемоглобина кооперируют в связывании кислорода – это и называют эффектом кооперативности [8, 9].
S-образность кривой связывания теряется при отсутствии эффекта кооперативности (на рис. 4 крупным пунктиром показана кривая связывания некооперативного белка миоглобина с кислородом). Миоглобин – мышечный белок, близкий родственник гемоглобина, который по структуре и способности связывать кислород очень похож на одну субъединицу гемоглобина [10]. Похожую зависимость имеет аналогичная кривая для мономеров гемоглобина. Гипотетическая кривая связывания гемоглобина с кислородом, рассчитанная при условии отсутствия эффекта кооперативности, показана мелким пунктиром на рисунке 4. Если можно было бы зафиксировать гемоглобин в этом состоянии, то кривая связывания с кислородом проходила бы очень полого.
Гемоглобин умеет связывать не только кислород, но и многие другие молекулы, похожие на кислород. C этим cвязаны некоторые медицинские эффекты радикального нарушения газотранспорта. Так, место кислорода может занимать молекула оксида углерода (СО), в быту она известна как угарный газ. Эта молекула очень похожа на кислород. Она связывается с гемоглобином сильнее кислорода и очень плохо диссоциирует из образовавшегося комплекса, освобождая гемоглобин [4]. Таким образом, если во вдыхаемом нами газе появляется угарный газ, то происходит отравление: СО вытесняет кислород из молекулы гемоглобина, который оказывается загружен прочно связанным балластом и не может выполнять свою функцию, несмотря на то, что он функционально совершенно нормален. Наступает удушье. Человек,