ВУЗ: Казахский национальный медицинский университет им. С.Д. Асфендиярова
Категория: Шпаргалка
Дисциплина: Химия
Добавлен: 05.02.2019
Просмотров: 12596
Скачиваний: 45
именьшими цифрами (направление нумерации не
имеет значения), для дизамещенных соединений ис
пользуют следующие обозначения: 1,2 орто (о),
1,3 мета (м), 1,4 пара (п) положение.
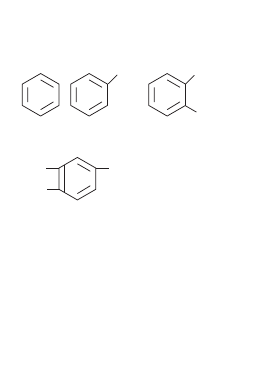
бензол
толуол
ксилол
СН
3
СН
3
СН
3
Н
3
C
Н
3
C
C
3
Н
3
1
2
3
4
5
6
1,2 диметил4этилбензол
52. стрОение бензОла.
физические свОйства aренОв
Бензол содержит шесть атомов углерода и шесть
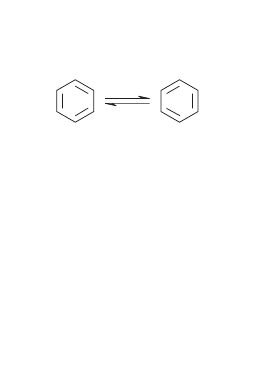
водорода. Ф. Кекуле выдвинул гипотезу (1865), что
бензол является равновесным гибридом двух альтер
нативных структур гексатриена1,3,5:
противоречия гипотезы кекуле:
•
Согласно формуле Кекуле, для бензола, содержа
щего три двойные связи, должны быть характерны
реакции присоединения. Но бензол не обесцвечи
вал бромную воду и разбавленный щелочной вод
ный раствор перманганата калия.
•
Формула Кекуле предполагает существование
двух изомеров для 1,2дизамещенных бензолов,
содержащих заместители у соседних атомов угле
рода в кольце.
современная теория строения бензола:
•
все атомы углерода и водорода в молекуле бензола
лежат в одной плоскости;
•
C—C связи кольца имеют одинаковую длину
0,139 нм;
•
углы между связями С—С и С—Н равны 120°.
В бензоле каждый атом углерода связан с тремя
другими (с двумя атомами углерода и атомом водо
рода), следовательно, находится в состоянии sp
2
ги
бридизации. Все эти связи являются у-связями. Пос
ле образования связей с двумя атомами углерода и
одним атомом водорода у каждого атома углерода

остается по электрону на негибридизованной р-ор
битали, состоящей из двух одинаковых частей, рас
положенных над и под плоскостью кольца. Негибри
дизованная р-орбиталь каждого атома углерода пе
рекрывается с р-орбиталями двух coседних атомов
углерода. В результате образуется единое электрон
ное облако, плотность которого равномерно распре
делена по всему бензольному кольцу (делокализа-
ция электронов).
правило Xюккеля: к ароматическим системам от
носят моноциклические карбоциклы, имеющие плос
кое строение и содержащие в замкнутой системе со
пряжения (4n + 2) электронов. Так, для бензола n = 1,
и он содержит шесть р-электронов, которые называ
ют ароматическим секстетом.
физические свойства.
Ароматические углеводороды — жидкие или твер
дые вещества, плотность которых меньше плотности
воды, нерастворимы в воде, сами являются хороши
ми растворителями для многих органических соеди
нений.
Бензол — легкокипящая, бесцветная, нераствори
мая в воде жидкость со своеобразным запахом. При
охлаждении он легко застывает в белую кристалли
ческую массу с температурой плавления 5,5 °С. Пары
бензола с воздухом образуют взрывчатую смесь.
Жидкий бензол и пары бензола ядовиты.
53. пОлучение аренОв
1. из продуктов сухой перегонки (коксования)
каменного угля.
2. из нефти — как при первичной ее обработке, так
и в результате ароматизации.
3. дегидрирование шестичленных алицикли-
ческих углеводородов: пропускание паров алицик
лических углеводородов над катализаторами (Mo
2
O
3
,
Al
2
O
3
или Pd) при высоких температурах (500—600 °C)
и давлении (2—3 MПа) (Н.Д. Зелинский).
4. дегидроциклизация алканов и алкенов, со
держащих не менее шести атомов углерода (усло
вия — катализаторы (платинированный уголь, оксид
хрома), температура 300—500 °C), Б.А. Казанский,
В.Л. Молдавский, А.Ф. Платэ.
5. синтез вюрца—фиттига — получение произ
водных бензола (обработка смеси алифатического и
ароматических галогенпроизводных металлическим
натрием).
6. получение бензола из ацетилена (Н.Д. Зе-
линский, Б.А. Казанский).
3НС≡CH
С, 600 °C
54. химические свОйства аренОв:
реакции присОединения и Окисления
По химическим свойствам арены занимают проме
жуточное место между предельными и непредельны
ми углеводородами.
1. реакции присоединения.
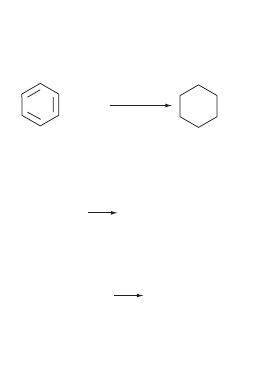
а) Гидрирование (присоединение водорода):
циклогексан
бензол
+ 3Н
2
Ni, Pt, Pd
б) Присоединение хлора или брома по радикально
му механизму (при освещении ультрафиолетовыми
лучами).
2. реакция окисления.
а) Озонирование:
б) При длительном нагревании толуола с KMnO
4
все
же происходит обесцвечивание раствора, но в этом
случае происходит окисление метильной группы, а не
разрушение бензольного кольца:
в) Как все углеводороды, бензол горит коптящим
пламенем.
C
6
H
6
+ 3О
2
3HC(О)—C(О)H
бензол
глиоксаль
C
6
H
5
CH
3
+ 2[О]
C
6
H
5
COOH
бензойная кислота