Добавлен: 06.02.2019
Просмотров: 15972
Скачиваний: 9
186
0.6
0.8
1.0
1.2
1.4
1.6
1.8
2.0
2.2
2.4
2.6
-0.8
-0.6
-0.4
-0.2
0.0
0.2
0.4
0.6
i, A/c
м
2
E, В
1.8
1.9
2.0
2.1
2.2
2.3
2.4
2.5
2.6
-0.1
0.0
0.1
0.2
0.3
0.4
i, A/
см
2
E, В
Рис. 142. Циклические вольтамперограммы медного электрода в расплаве с КО 1.3.
Скорость развертки потенциала 10 мВ/с.
Табл. 4. Термодинамические оценки потенциалов (шкала алюминиевого электрода сравнения) для
возможных реакций с участием соединений олова при различных температурах
KO=1.8 (920
o
C) KO=1.3
(750
o
C)
Реакция
Редокс-
процесс
∆G
1193
,
кДж/моль
E, В
∆G
1023
,
кДж/моль
E, В
2Al
2
O
3
= 4Al+ 3O
2(g)
Al
2
O
3
/O
2
2594 2.240 2707 2.338
Al
2
O
3
+ 6Cu = 3Cu
2
O + 2Al
Cu/Cu
2
O 1052 1.817 1072 1.851
Al
2
O
3
+ 3Cu = 3CuO + 2Al
Cu/CuO
1146
1.979
1160
2.003
Al
2
O
3
+ 3Cu
2
O = 6CuO + 2Al
Cu
2
O/CuO
1241 2.143 1249 2.157
2Al
2
O
3
+ 1.5Cu = 1.5CuAl
2
O
4
+ Al
Cu/CuAl
2
O
4
384 1.326 394 1.361
2Al
2
O
3
+ 3Cu = 3CuAlO
2
+ Al
Cu/CuAlO
2
506 1.747 514 1.775
AlF
3
+ 3Cu = Al + 3CuF
Cu/CuF
636
2.197
655
2.262
AlF
3
+ 1.5Cu = Al + 1.5CuF
2
Cu/CuF
2
687 2.373 664 2.293
0.0
0.6
1.2
1.8
2.4
3.0
3.6
-4
-2
0
2
4
i, A
/см
2
E, B
без добавок
+0,4 % Al
2
O
3
+0,8 % Al
2
O
3
+1,2 % Al
2
O
3
+1,6 % Al
2
O
3
Рис. 143. Циклические вольтамперограммы медного электрода, зарегистрированные в
низкоглиноземном расплаве c КО 1.8 после введения в расплав различных концентра-
ций глинозема. Площадь электрода 0.9 см
2
. Скорость развертки потенциала 100 мВ/с.
187
3.1.4. Электрохимическое поведение керамики SnO
2
+1.5 мас.% CuO+1.5 мас.% Sb
2
O
3
Электрохимическое поведение керамик на основе диоксида олова изучалось пре-
имущественно в высокотемпературных расплавах (КО=2.5–3.0) [669, 673, 693, 694]. Ин-
формация о средне- и низкотемпературных расплавах крайне отрывочна [670]. Экспери-
ментальные результаты, полученные в настоящей работе, хорошо согласуются с литера-
турными данными. Стационарный потенциал керамических электродов при разомкнутой
цепи в расплавах разного состава отличается незначительно и составляет 1.6–1.7 В, в хо-
рошем соответствии с данными [669, 693]. С учетом сводных данных рис. 140 можно за-
ключить, что компромиссный потенциал навязывается процессом восстановления диок-
сида олова с образованием растворимых оловосодержащих частиц SnO
2
/Sn(II).
Типичные вольтамперограммы керамических электродов в расплавах с КО 1.8
(920
о
С), 2.0 (950
o
C) и 2.3 (980
o
C) представлены на рис. 144. Сопоставление кривых по-
казывает, что по мере снижения температуры расплава происходит выраженное увели-
чение перенапряжения процесса выделения кислорода. Ранее аналогичная тенденция
отмечалась в [670]. Представленные на рис. 144б вольтамперограммы, скомпенсиро-
ванные на величину омического скачка, показывают, что наблюдаемый эффект не свя-
зан с ростом омического сопротивления в системе. В области выделения кислорода, как
и в большинстве опубликованных ранее работ [669, 673, 693], регистрируемая вольтам-
перограмма представляет собой прямую линию, что указывает на определяющий вклад
омических искажений. Грубые оценки, выполненные методом импедансной спектро-
скопии, показали, что омическое сопротивление в этой области потенциалов возрастает
при увеличении анодной плотности тока, что может быть связано как с изменяющимся
газонаполнением в приэлектродном слое, так и с какими-либо изменениями в самой
керамике. Как уже указывалось ранее, имеющееся оборудование не позволяет осущест-
влять динамическую компенсацию омического скачка в ходе измерений вольтампер-
ных кривых, поэтому прецизионный анализ кинетики выделения кислорода невозмо-
жен. Приближенные оценки, выполненные по уравнению Тафеля с учетом омической
составляющей, подтверждают, что при переходе от КО 2.3 к 1.8 происходит увеличение
тафелевского наклона поляризационной зависимости от ~0.1 до ~0.2 В. Токи обмена
для анодной реакции во всех исследованных расплавах не превышают 10–20 мА/см
2
.
Для высокотемпературного расплава с КО 2.7 (1000
о
С) ранее были получены величины
тафелевского наклона 0,065-0,086 В [669, 694] причем точность определения этих вели-
чин также была невелика. Токи обмена по данным разных авторов не превышают 20–30
мА/см
2
[669, 693]. Лишь в работе [694] были получены токи обмена около 50 мА/см
2
, что,
вероятно, связано с небольшими сдвигами потенциала электрода сравнения.
188
1.6
1.8
2.0
2.2
2.4
2.6
2.8
-0.07
0.00
0.07
0.14
0.21
0.28
0.35
0.42
i, A/
см
2
E, B
KO=2.3
KO=2.0
KO=1.8
a
1.6
1.8
2.0
2.2
2.4
2.6
-0.10
-0.05
0.00
0.05
0.10
0.15
0.20
0.25
0.30
0.35
0.40
i, A
/см
2
E, B
KO=1.8
KO=2.0
KO=2.3
б
Рис. 144. Циклические вольтамперограммы, зарегистрированные на керамическом элек-
троде SnO
2
+ 1.5% CuO + 1.5 % Sb
2
O
3
в расплавах с различным КО, содержащим 2% гли-
нозема до (а) и после (б) IR компенсации. Скорость развертки потенциала 50 мВ/с.
Как уже указывалось ранее, при смещении потенциала в сторону отрицательных
значений примерно при 1.6 В на кривых (рис. 136) возникает катодный ток, отвечаю-
щий процессу восстановления диоксида олова с образованием растворимого оловосо-
держащего продукта. Кроме того, на всех кривых можно выделить четкий окислитель-
но-восстановительный процесс, которому отвечает формальный потенциал около 2.1 В.
Наиболее четко отклик этого процесса проявляется в расплаве с низким КО (рис. 145).
Он может быть отнесен к окислительно-восстановительным превращения меди
Cu(I)/Cu(II) в составе керамики (ср. рис. 141). Таким образом, спекающая добавка ок-
сида меди активно участвует в электрохимических реакциях на поверхности керамиче-
ского анода. Нужно отметить, что согласно данным электронной микроскопии основ-
ная часть спекающей добавки Cu
2
O локализуется в керамике в виде включений, со-
стоящих из оксидов меди и Cu
4
SbO
4.5
(идентифицирован методом рентгенофазового
анализа) (рис. 146). Кроме того, оксид меди присутствует на поверхности пор в кера-
мике. Обнаружить значимые количества меди непосредственно в объеме кристаллов
SnO
2
не удается. Поэтому можно предположить, что наблюдаемые электрохимические
отклики связаны, в первую очередь, с окислительно-восстановительными превраще-
ниями меди, содержащейся во включениях. Однако с учетом того факта, что включения
должны неизбежно быстро растворяться в расплаве при циклировании, а наблюдаемые
отклики остаются стабильными в ходе длительных измерений, нельзя исключить и уча-
стия в редокс-процессе незначительных количеств меди, входящей в состав основной
фазы керамики. Согласно [695], в системе Sn-Sb-Cu-O возможно образование твердого
раствора Sn
1-x
Cu
x/3
Sb
2x/3
O
2
(x
≤ 0.25). Твердый раствор со степенью замещения x=0.25
устойчив при температуре ниже 1200
о
С, однако температурная устойчивость этого со-
единения значительно возрастает при снижении степени замещения. Поэтому, несмот-
189
ря на то, что твердофазное спекание керамики проводилось при высоких температурах
(обычно 1280
о
С), образованием фазы твердого раствора с малой степенью замещения
не может быть однозначно исключено.
В расплаве с КО=1.8 при потенциалах около 2.4 В наблюдается еще один редокс-
процесс (рис. 145), который, возможно, связан с окислительно-восстановительными ре-
акциями с участием сурьмы, либо с участием каких-либо частиц в керамике или рас-
плаве. В более высокотемпературных расплавах данный процесс практически незаме-
тен на фоне основной кислородной реакции.
1.4
1.6
1.8
2.0
2.2
2.4
2.6
2.8
3.0
-0.2
-0.1
0.0
0.1
0.2
0.3
0.4
I, A
E, B
Рис. 145. Циклические вольтамперограммы с переменным катодным пределом, зарегист-
рированные на керамическом электроде SnO
2
+ 1.5% CuO + 1.5 % Sb
2
O
3
в расплаве с КО
1.8 (2% Al
2
O
3
). Скорость развертки потенциала 50 мВ/с. Площадь электрода 2 см
2
.
Характерной особенностью анодного хода поляризационных кривых для олово-
содержащей керамики является наличие фоновых токов, предшествующих началу вы-
деления кислорода (предволны). Согласно [669, 693] они не превышают 20–30 мА/см
2
и
исчезают на обратном ходе развертки. Авторы объясняли наличие этих токов процес-
сами окисления небольших количеств двухвалентного олова, образующегося при вос-
становлении керамики растворенным алюминием или CO. На вольтамперограмах (рис.
144) в высокотемпературных расплавах также присутствует данная предволна (фоно-
вые токи 25 мА/см
2
). Однако снижение температуры расплава до 920
о
С приводит к
практически полному ее исчезновению. Поскольку в данных экспериментах присутст-
вие в расплаве значительных количеств растворенного алюминия практически исклю-
чено, наличие предволны может быть связано в первую очередь именно с наличием в
расплаве растворенного монооксида углерода.
190
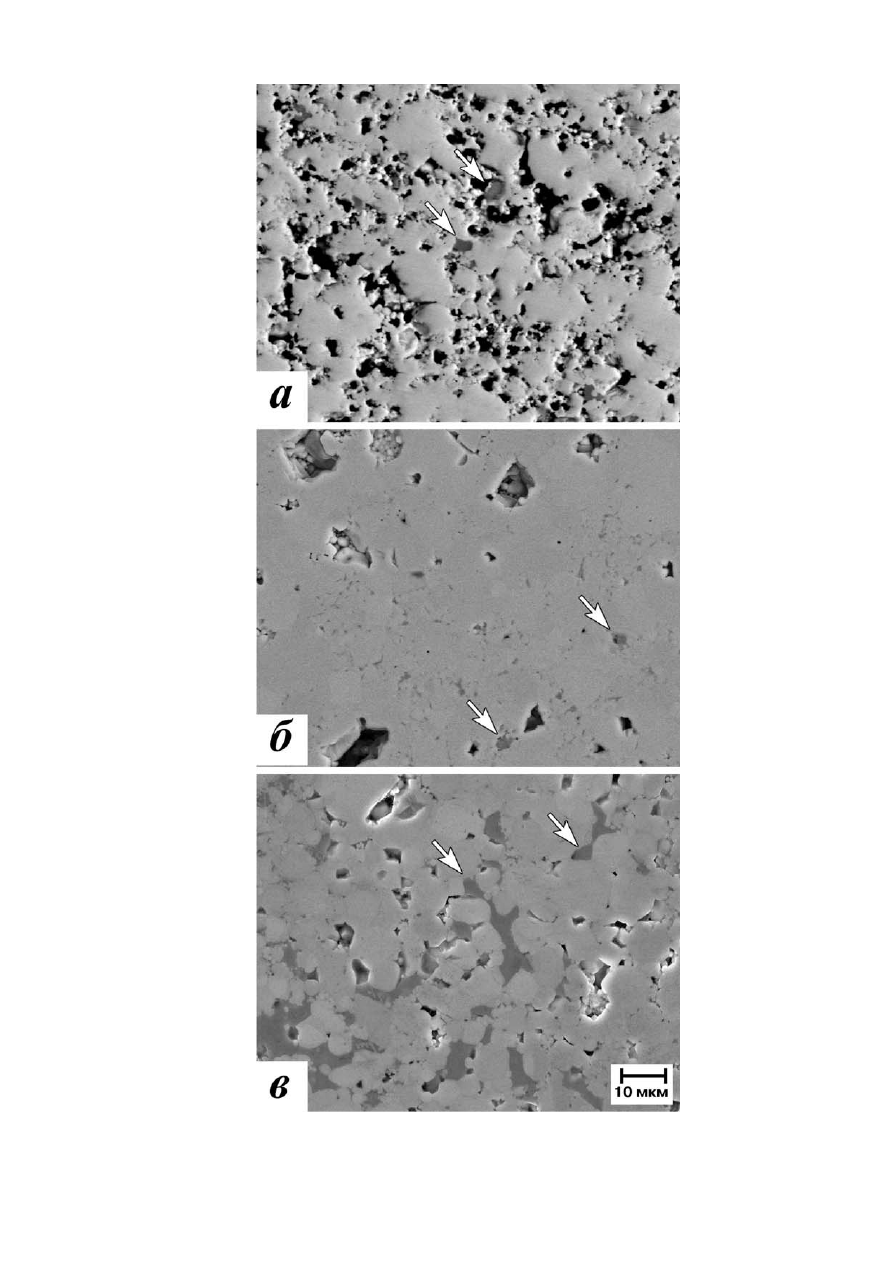
Рис. 146. Микроструктура исходного керамического материала состава 97 мас.% SnO
2
+
1.5 мас.% CuO + 1.5 мас.% Sb
2
O
3
с плотностью 6.4 (a) и 6.8 (б) г/см
3
и 90 мас.% SnO
2
+
5 мас.% CuO + 5 мас.% Sb
2
O
3
(в). Стрелками показаны включения медьсодержащей фазы.