Файл: белорусский государственный технологический университет.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 11.12.2023
Просмотров: 1112
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
пуска во всех биореакторах при двух вариантах рН отмечено газообразование на среде с лактозой, тогда как на среде с уксусной кислотой газообразова- ние наблюдалось в 3 случаях из 36. Повышение нагрузки по органиче- ским загрязнителям приводит к газообразованию на средах с лактозой при рН 7,0-7,2 во всех случаях, тогда как при рН 5,6-6,2 газообразова- ние наблюдалось только при низких нагрузках по органическим веще- ствам. Высев на средах с уксусной кислотой сопровождался газообра- зованием только при высоких нагрузках по органическим веществам при рН 5,6-6,2 и 7,0-7,2. Выбор реагента для регулирования рН оказы- вал незначительное влияние.
УДК 663.252:543.421/.424
Магистрант М.Н. Гуцу
Науч. рук. доц. Т.М. Тананайко (кафедра биотехнологии, БГТУ)
Несмотря на сложный химический состав натурального вино- градного вина, в последнее время оно все чаще становится объектом фальсификации. Большую часть поддельной винодельческой продук- ции составляет суррогатная продукция и продукция, произведенная с нарушением основных правил и регламентов производства [1].
Наиболее распространенными способами фальсификации вино- дельческой продукции являются [2]: петиотизация (сбраживание вино- градной выжимки на сахарном сиропе), шеелизация (добавление гли- церина в излишне кислые вина для корректировки органолептических показателей), галлизация (разбавление вина водой и доведение крепо- сти до исходной техническим этанолом), а также использование синте- тических красителей для исправления некачественных красных вин или для маскировки дешёвых белых вин под дорогие красные вина. Ос- новным способом выявления петиотизации является определение со- держания пролина. В натуральных белых винах содержание пролина составляет от 100 до 800 мг/дм3 (в красных винах до 2000 мг/дм3), а в виноградной выжимке – не более 30 мг/дм3 [3]. Метод основан на про- ведении реакции с нингидрином, в ходе которой пролин даёт жёлтое окрашивание. Его концентрация определяется на спектрофотометре в стеклянных кюветах толщиной 1 см и длине волны 509 нм. Выявление шеелизации также возможно с помощью спектрофотометра. Содержа- ние глицерина в натуральных винах – до 15 г/дм3, но в случае шеелиза- ции это значение будет превышено. Данный метод основан на окисле- нии глицерина вина йодной кислотой с образованием формальдегида, который вступает в реакцию с флороглюцином, образуя окрашенное соединение с максимумом
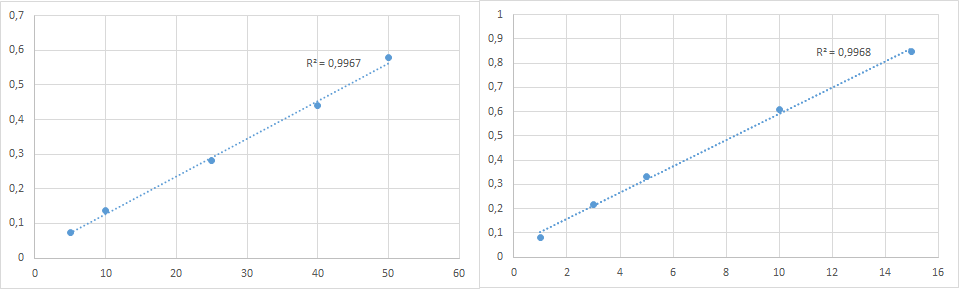
поглощения при длине волны 480 нм. Пред- варительно виноматериал пропускают через анионообменную смолу для фиксации сахаров, маннитов и сорбитов. На рисунке 1 представ- лены градуировочные графики для определения пролина и глицерина. Для выявления галлизации возможно применение ИК-спектроскопии. При оценке возможности применения метода проводили намеренную фальсификацию путём добавления воды в вино объёмом 30% от исход- ного объёма вина, т. к. данная степень разбавления соответствует гра- нице органолептического определения фальсификации путём разбавле- ния [3]. При анализе ИК-спектров была выявлена полоса поглощения,
 интенсивность которой при галлизации значительно снижалась. Дан- ная полоса поглощения лежит в диапазоне 1100-1300 см-1. Таким обра- зом, ИК-спектроскопию возможно применять в качестве метода выяв- ления галлизации, однако для этого необходимо иметь контрольный спектр неразбавленного исследуемого виноматериала.
интенсивность которой при галлизации значительно снижалась. Дан- ная полоса поглощения лежит в диапазоне 1100-1300 см-1. Таким обра- зом, ИК-спектроскопию возможно применять в качестве метода выяв- ления галлизации, однако для этого необходимо иметь контрольный спектр неразбавленного исследуемого виноматериала.
Рисунок_1_–_Градуировочные_графики_для_определения_концентрации'>Рисунок 1 – Градуировочные графики для определения концентрации пролина (слева) и глицерина (справа)
 Доступным методом определения синтетических красителей яв- ляется метод ТСХ. Виноматериал обрабатывали порошком полиамид- ной смолы для фиксации красителей в течение 2 ч при постоянном пе- ремешивании. Натуральные красители элюировали 50 % раствором ук- сусной кислоты, а синтетические – 5 % раствором аммиака в метаноле. Подвижная фаза – смесь хлороформ:метанол в соотношении 9:1. Ре- зультаты ТСХ представлены на рисунке 2. Примечание: 1 – стандарт- ный раствор конго красного; 2,5 –
Доступным методом определения синтетических красителей яв- ляется метод ТСХ. Виноматериал обрабатывали порошком полиамид- ной смолы для фиксации красителей в течение 2 ч при постоянном пе- ремешивании. Натуральные красители элюировали 50 % раствором ук- сусной кислоты, а синтетические – 5 % раствором аммиака в метаноле. Подвижная фаза – смесь хлороформ:метанол в соотношении 9:1. Ре- зультаты ТСХ представлены на рисунке 2. Примечание: 1 – стандарт- ный раствор конго красного; 2,5 –
натуральный виноматериал; 3 – ви- номатериал, содержащий конго красный; 4 – стандартный раствор тарт- разина; 6 – виноматериал, содержащий тартразин.
Рисунок 2 – Хроматограмма для определения синтетических красителей
ЛИТЕРАТУРА
УДК 634.73
Студ. А.В. Бугаева Науч. рук. доц. Е.А. Флюрик (кафедра биотехнологии, БГТУ)
Перед нами стояла задача получить растительные порошки из растительных настоек экстрактов. В качестве объекта для изучения ис- пользовали экстракт ягод голубики, полученный с помощью аппарата Сокслета. После удаления этилового спирта из экстракта с помощью вакуум-выпарной установки (IKA RV 05 basic), концентрат был под- вергнут лиофильному высушиванию. Для этого использовали лио- фильную сушилку Cool Safe 100-9 PRO. Однако в ходе сушки была от- мечена такая особенность: растительные образцы невозможно высу- шить до порошкообразного состояния т. к. получается вязкая, клейкая субстанция, представленная на рис. б, которая при увеличении времени сушки не изменяет свой внешний вид. Поэтому нами был произведен литературный поиск, в ходе которого установили, что для получения растительных порошков можно в жидкий образец внести определенное количество Трилона Б. Данное вещество обладает хорошей раствори- мостью в воде, применяется в качестве антиоксиданта. На рисунке апоказан образец экстракта, высушенный с добавлением указанной до- бавки.

а– с добавлением Трилона Б б – без добавок
Рисунок – Лиофильная сушка образцов растительного экстракта
Дальнейшая работа будет направлена на определение оптималь- ной концентрации Трилона Б, которую необходимо вносить в образец для получения растительных порошков.
УДК 582.883.4
Учащ. Д.В. Булат, Д.В. Шикарев (Национальный детский технопарк)
Науч. рук.
УДК 663.252:543.421/.424
Магистрант М.Н. Гуцу
Науч. рук. доц. Т.М. Тананайко (кафедра биотехнологии, БГТУ)
МЕТОДЫ АНАЛИЗА И ВЫЯВЛЕНИЯ ФАЛЬСИФИКАЦИИ ВИНОМАТЕРИАЛОВ
Несмотря на сложный химический состав натурального вино- градного вина, в последнее время оно все чаще становится объектом фальсификации. Большую часть поддельной винодельческой продук- ции составляет суррогатная продукция и продукция, произведенная с нарушением основных правил и регламентов производства [1].
Наиболее распространенными способами фальсификации вино- дельческой продукции являются [2]: петиотизация (сбраживание вино- градной выжимки на сахарном сиропе), шеелизация (добавление гли- церина в излишне кислые вина для корректировки органолептических показателей), галлизация (разбавление вина водой и доведение крепо- сти до исходной техническим этанолом), а также использование синте- тических красителей для исправления некачественных красных вин или для маскировки дешёвых белых вин под дорогие красные вина. Ос- новным способом выявления петиотизации является определение со- держания пролина. В натуральных белых винах содержание пролина составляет от 100 до 800 мг/дм3 (в красных винах до 2000 мг/дм3), а в виноградной выжимке – не более 30 мг/дм3 [3]. Метод основан на про- ведении реакции с нингидрином, в ходе которой пролин даёт жёлтое окрашивание. Его концентрация определяется на спектрофотометре в стеклянных кюветах толщиной 1 см и длине волны 509 нм. Выявление шеелизации также возможно с помощью спектрофотометра. Содержа- ние глицерина в натуральных винах – до 15 г/дм3, но в случае шеелиза- ции это значение будет превышено. Данный метод основан на окисле- нии глицерина вина йодной кислотой с образованием формальдегида, который вступает в реакцию с флороглюцином, образуя окрашенное соединение с максимумом
поглощения при длине волны 480 нм. Пред- варительно виноматериал пропускают через анионообменную смолу для фиксации сахаров, маннитов и сорбитов. На рисунке 1 представ- лены градуировочные графики для определения пролина и глицерина. Для выявления галлизации возможно применение ИК-спектроскопии. При оценке возможности применения метода проводили намеренную фальсификацию путём добавления воды в вино объёмом 30% от исход- ного объёма вина, т. к. данная степень разбавления соответствует гра- нице органолептического определения фальсификации путём разбавле- ния [3]. При анализе ИК-спектров была выявлена полоса поглощения,
 интенсивность которой при галлизации значительно снижалась. Дан- ная полоса поглощения лежит в диапазоне 1100-1300 см-1. Таким обра- зом, ИК-спектроскопию возможно применять в качестве метода выяв- ления галлизации, однако для этого необходимо иметь контрольный спектр неразбавленного исследуемого виноматериала.
интенсивность которой при галлизации значительно снижалась. Дан- ная полоса поглощения лежит в диапазоне 1100-1300 см-1. Таким обра- зом, ИК-спектроскопию возможно применять в качестве метода выяв- ления галлизации, однако для этого необходимо иметь контрольный спектр неразбавленного исследуемого виноматериала.Рисунок_1_–_Градуировочные_графики_для_определения_концентрации'>Рисунок 1 – Градуировочные графики для определения концентрации пролина (слева) и глицерина (справа)
 Доступным методом определения синтетических красителей яв- ляется метод ТСХ. Виноматериал обрабатывали порошком полиамид- ной смолы для фиксации красителей в течение 2 ч при постоянном пе- ремешивании. Натуральные красители элюировали 50 % раствором ук- сусной кислоты, а синтетические – 5 % раствором аммиака в метаноле. Подвижная фаза – смесь хлороформ:метанол в соотношении 9:1. Ре- зультаты ТСХ представлены на рисунке 2. Примечание: 1 – стандарт- ный раствор конго красного; 2,5 –
Доступным методом определения синтетических красителей яв- ляется метод ТСХ. Виноматериал обрабатывали порошком полиамид- ной смолы для фиксации красителей в течение 2 ч при постоянном пе- ремешивании. Натуральные красители элюировали 50 % раствором ук- сусной кислоты, а синтетические – 5 % раствором аммиака в метаноле. Подвижная фаза – смесь хлороформ:метанол в соотношении 9:1. Ре- зультаты ТСХ представлены на рисунке 2. Примечание: 1 – стандарт- ный раствор конго красного; 2,5 –
натуральный виноматериал; 3 – ви- номатериал, содержащий конго красный; 4 – стандартный раствор тарт- разина; 6 – виноматериал, содержащий тартразин.
Рисунок 2 – Хроматограмма для определения синтетических красителей
ЛИТЕРАТУРА
-
Николаева, М.А., Положишникова, М.А. Идентификация и об- наружение фальсификации продовольственных товаров: учебное посо- бие. – М.: ИД «ФОРУМ»: ИНФРА–М, 2009. – 464 с. -
Holmberg, L. Wine fraud // International Journal of Wine Research. 2010. V. 2. P. 105–113. -
Вино – энциклопедия виноделия [Электронный ресурс] / Фаль- сификация. Режим доступа: https://eniw.ru/. Дата доступа: 05.04.2022.
УДК 634.73
Студ. А.В. Бугаева Науч. рук. доц. Е.А. Флюрик (кафедра биотехнологии, БГТУ)
ПРОБЛЕМЫ, ВОЗНИКАЮЩИЕ ПРИ ЛИОФИЛЬНОЙ СУШКЕ РАСТИТЕЛЬНЫХ ЭКСТРАКТОВ
Перед нами стояла задача получить растительные порошки из растительных настоек экстрактов. В качестве объекта для изучения ис- пользовали экстракт ягод голубики, полученный с помощью аппарата Сокслета. После удаления этилового спирта из экстракта с помощью вакуум-выпарной установки (IKA RV 05 basic), концентрат был под- вергнут лиофильному высушиванию. Для этого использовали лио- фильную сушилку Cool Safe 100-9 PRO. Однако в ходе сушки была от- мечена такая особенность: растительные образцы невозможно высу- шить до порошкообразного состояния т. к. получается вязкая, клейкая субстанция, представленная на рис. б, которая при увеличении времени сушки не изменяет свой внешний вид. Поэтому нами был произведен литературный поиск, в ходе которого установили, что для получения растительных порошков можно в жидкий образец внести определенное количество Трилона Б. Данное вещество обладает хорошей раствори- мостью в воде, применяется в качестве антиоксиданта. На рисунке апоказан образец экстракта, высушенный с добавлением указанной до- бавки.

а– с добавлением Трилона Б б – без добавок
Рисунок – Лиофильная сушка образцов растительного экстракта
Дальнейшая работа будет направлена на определение оптималь- ной концентрации Трилона Б, которую необходимо вносить в образец для получения растительных порошков.
УДК 582.883.4
Учащ. Д.В. Булат, Д.В. Шикарев (Национальный детский технопарк)
Науч. рук.