Файл: Отчет по лабораторной работе 3 По дисциплине Термодинамика и кинетика.docx
Добавлен: 11.12.2023
Просмотров: 105
Скачиваний: 7
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
8. Среднее квадратичное отклонение σ рассчитывают по уравнению:
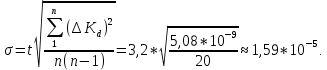
t = 3,2 – коэффициент Стьюдента для 95 %.
9. Окончательный результат:
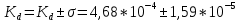 .
.Вывод: в ходе лабораторной работы методом кондуктометрического анализа был найден эквивалентный объём щелочи и концентрация кислоты. Возрастание электропроводимости до точки эквивалентности обусловлено заменой слабо-диссоциирующих молекул муравьиной кислоты на полностью диссоциирующий формиат натрия. Более резкое увеличение электропроводимости после точки эквивалентности вызвано появлением в растворе избытка весьма подвижных гидроксид-ионов.
Также получена константа диссоциации слабого электролита, она составила:
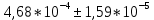
Было установлено, что с уменьшением концентрации кислоты её степень и константа диссоциации возрастают, что подтверждает закон разбавления Оствальда. Это объясняется тем, что с увеличением количества воды, т.е. с разбавлением раствора, число диссоциированных ионов возрастает, то есть процесс диссоциации происходит более активно.