Добавлен: 12.12.2023
Просмотров: 173
Скачиваний: 2
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
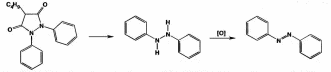
При действии раствора дихромата калия в концентрированной серной кислоте феназон и метамизол-натрий приобретают зеленое окрашивание, а фенилбутазон — темно-красное. Идентифицировать производные пиразола можно с помощью цветных реакций, которые они дают с различными реактивами: концентрированной азотной кислотой, смесью концентрированных азотной и серной кислот, с 0,5%-ным раствором ванадата аммония в концентрированной серной кислоте, 1 %-ным раствором и-диметиламинобензалъдегида в разведенной хлороводородной кислоте (после погружения в кипящую водяную баню).
Фенилбутазон можно идентифицировать реакциями осаждения солями: меди (осадок бледно-голубого цвета); серебра (белого цвета) и т. д. Для выполнения реакции вначале получают натриевую соль фенилбутазона, действуя раствором гидроксида натрия (происходит образование енольной формы):
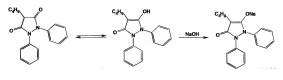
Затем к натриевой соли добавляют раствор сульфата меди:
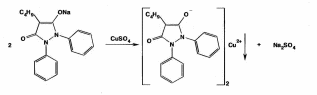
Феназон и метамизол-натрий под действием раствора сульфата меди (II) приобретают зеленое окрашивание. Производные пиразола ввиду наличия основных свойств дают характерные реакции с осадительными (общеалкалоидными) реактивами. При нагревании метамизола-натрия с реактивом Миллона (раствор ртути в азотной кислоте) возникает темно-синее окрашивание.
При испытаниях на чистоту особое внимание следует уделять обнаружению специфических примесей. В феназоне обнаруживают органические примеси, а также бензолсульфонат натрия (по прозрачности 10%-ного раствора в дихлорэтане). Посторонние примеси (не более 0,5%) в метамизоле-натрия устанавливают методом ТСХ на пластинках Силуфол УФ-254, сравнивая с СОВС 4-аминофеназона. Хроматографируют восходящим методом в камере с системой хлороформ-метанол (9:1), сушат и просматривают в УФ-свете при 254 нм, сравнивая пятна и значения Rf. В фенилбутазоне устанавливают отсутствие примеси гидразобензола по отрицательной цветной реакции с хлоридом железа (III) в среде концентрированной серной кислоты.
Йодхлорометрическое определение, основанное на реакции замещения, можно использовать для определения фе- нилбутазона, который растворяют при нагревании в 0,1 М растворе гидроксида натрия
, нейтрализуют 0,1 М раствором хлороводородной кислоты и в среде натрия гидрокарбоната титруют 0,1 М раствором йодмонохлорида (индикатор крахмал):
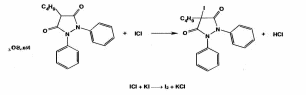
Количественное определение пропифеназона выполняют методом неводного титрования, используя в качестве растворителя диоксан. Титрантом служит 0,1 М раствор хлорной кислоты в ледяной уксусной кислоте (индикатор кристаллический фиолетовый).
Количественное определение фенилбутазона по ФС основано на нейтрализации раствора навески в ацетоне 0,1 М раствором гидроксида натрия с применением индикатора фенолфталеина. В этом способе использованы кислотные свойства енольной формы фенилбутазона:

Количественное определение пропифеназона в лекарственных формах выполняют методом ВЭЖХ, одновременно подтверждая его подлинность. На хроматограмме испытуемого раствора образуется пик с временем удерживания и УФ-аб- сорбционными характеристиками, аналогичными хроматограмме раствора сравнения пропифеназона. Для количественного определения используют обращенно-фазовый вариант ВЭЖХ. Неподвижная фаза — октадецилсилил на силикагеле (5 мкм), подвижная фаза — метанол-вода-0,01 М фосфорная кислота.
Предложены также способы количественного определения методом И К-спектрофотометрии в области «отпечатков пальцев»: феназона (1140 см-1), фенилбутазона (1590 см ')- В качестве растворителей использовали хлороформ или тетра- хлорметан. Относительная погрешность определения ±0,5-1,0%.
Производные пиразола хранят в хорошо укупоренной таре, предохраняющей от действия света, по списку Б
Производные пиразола применяют в качестве болеутоляющих, жаропонижающих и противовоспалительных средств. пропифеназон назначают внутрь при головных болях, невралгиях, артритах и других заболеваниях по 0,25-0,5 г на приемФенилбутазон назначают главным образом при острых формах ревматизма и полиартритов по 0,1 -0,15 г. Пропифеназон проявляет анальгезирующее действие в несколько раз более сильное, чем феназон. Он входит в состав анальгетических лекарственных форм (саридон) по 0,15 г.
БИЛЕТ 38
Фармацевтическая фирма-дистрибьютер закупила таблетки фенобарбитала и бензонала и лекарственное растительное сырьё ьрава горца перечного
Для этого:
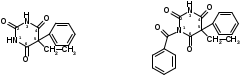
Фенобарбитал (МНН). Phenobarbitalum Бензобарбитал (МНН)
5-этил-5-фенилбарбитуровая кислота Benzobarbitalum
Бензонал
1-бензоил-5-этил-5-
фенилбарбитуровая кислота
Фенобарбитал и бензонал относятся к производным барбитуровой кислоты.
Подлинность фенобарбитала и бензонала можно установить по УФ- и ИК-спектрам.
Для испытания подлинности фенобарбитала и бензонала используют химические реакции, основанные на соле- и комплексообразовании с солями тяжелых металлов.
Фенобарбитал и бензонал образуют нерастворимые соли с ионами серебра, ртути (II), меди (II), кобальта (II).
При взаимодействии с ионами серебра происходит образование однозамещенных (растворимых в воде) и двузамещенных (нерастворимых в воде) солей серебра:
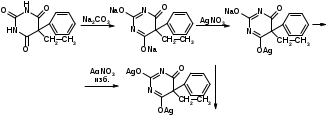
В отличие от фенобарбитала, бензонал, содержащий заместитель у N1, образует только однозамещенные соли.
Фенобарбитал и бензонал можно идентифицировать сплавлением с едкими щелочами, так как они при этом разрушаются с выделением аммиака:
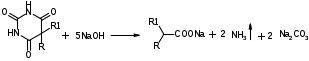
Фенильный радикал в фенобарбитале и бензонале обнаруживают по образованию нитросоединений, окрашенных в желтый цвет:
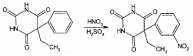
Специфичной для бензонала является реакция с хлоридом железа (III) после предварительного гидролиза. Образующийся при гидролизе бензонала бензоат-ион образует с ионом железа (III) розовато-желтый осадок:
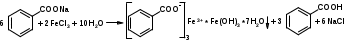
Поскольку фенобарбитал и бензонал проявляют слабые кислотные свойства, для количественного определения применяют неводное титрование в среде диметилформамида.
Титруют 0,1 М раствором натрия гидроксида (в смеси метанола и бензола). Диметилформамид, являясь основным растворителем, присоединяет протон, усиливая при этом кислотные свойства барбитуратов:

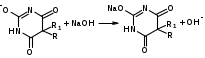
HCO+NH(CH3)2 + OH- → HCON(CH3)2 + H2O
Количественное определение бензонала выполняют в спиртовом растворе, титруя его 0,1 М водным раствором гидроксида натрия до синего окрашивания.
БИЛЕТ 39
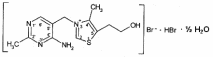 Тиамина бромид. Thiamini bromidum Тиамин (МНН) 4-метил-5-β-оксиэтил-N-(2'-метил-4'-амино-5'-метилпиримидил)-тиазолий бромида гидробромида полугидрат
Тиамина бромид. Thiamini bromidum Тиамин (МНН) 4-метил-5-β-оксиэтил-N-(2'-метил-4'-амино-5'-метилпиримидил)-тиазолий бромида гидробромида полугидратОснову химической структуры тиамина составляют два гетероцикла — пиримидин и тиазол. Гиповитаминозы и авитаминозы В;
Воспалительные и дегенеративные процессы в периферических нервах: различные формы невритов, алкогольные и постинфекционные полиневриты, радикулиты, невралгии, периферические парезы и параличи различного происхождения, болезнь Меньера, психоз Корсакова, полиомиелит и энцефаломиелит, болезнь Вернике;
Поражения центральной нервной системы в результате травмы, коммоций, особенно при резких болях; вегетативные неврозы, мигрени;
Сердечно-сосудистые неврозы, сопровождающиеся тахикардией, миастения;
Язвенная болезнь желудка и двенадцатиперстной кишки, Ослабление секреторной и двигательной функций желудочно-кишечного тракт (атония кишечника и др.);
Ухудшение регенерации тканей после ранений, раневое истощение; Нарушения питания (алиментарная дистрофия); Дистрофия миокарда, нарушения коронарного кровообращения у больных стенокардией; Тиреотоксикоз; Эндартериит; Неврогенные дерматозы
Наличие пиримидинового и тиазолового ядра в молекуле тиамина бромида обусловливает характерные ИК- и УФ-спектры.
Идентифицируют тиамина бромида с помощью реакции, основанной на окислении тиамина в щелочной среде. Эта реакция известна под названием тиохромной пробы:
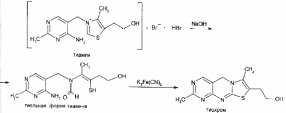
Тиохром из водных растворов извлекают бутиловым или изоамиловым спиртом. Спиртовые растворы при ультрафиолетовом облучении имеют характерную синюю флуоресценцию.
Тиамина бромид дает характерные реакции на бромиды: по реакции окисления до свободного брома (который окрашивает слой хлороформа в желто-бурый цвет) и по реакции с серебра нитратом:
2HBr + Cl2 → Br2 + 2HCl
NaBr + AgNO3 → AgBr↓ + NaNO3
Основание тиамина из растворов осаждается общеалкалоидными реактивами.
Тиамина бромид количественно определяют в водной среде способом, основанным на нейтрализации гидробромида и последующем аргентометрическом титровании суммы бромид-ионов:
Смотрите также файлы
- Итоговый проект по литературе Мир пушкинской лирики в исследованиях В. А. Грехнёва Автор работы.docx
- Отчет по лабораторной работе 10 определение модуля упругости (модуля юнга) по деформации изгиба.docx
- Реферат по дисциплине Психология Влияние речи родителей на развитие речи детей раннего возраста.docx