ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 12.12.2023
Просмотров: 235
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Цха мен Цха3 тің тотығуы кезінде 102 кДж энергия бөлінеді және көп мөлшерде жылу да бөлінеді.
БТның соңғы сатысында әрбір активті ионданған оттек , убихинонның тотықсыздануында түзілген 2 Н+ пен әрекеттесіп эндогенді суды түзеді.
Сонымен, БТның үш сатысында энергия бөлінеді, ПФ, Цхb, Цха және Цха3 тотыққанда түзілген энергия АТФ түзуге жеткілікті. БТ ның бұл сатыларын БТ мен ТФ ның қабысу нүктелері деп аталады.
4 саты ТФ(тотығудан фосфорлану)- энергия алмасу сатысы. Бұл БТ да бөлінген энергияны пайдаланып, АДФ пен бейорганикалық фосфаттың әрекеттесуінен АТФ тің түзілу процесі. Процесс АТФ-синтетаза ферментімен жылдамдатылады:
АДФ + Н3РО4 + WБО АТФ + Н2О
Тынысалу комплекстері. БТ ға қатысатын ферменттер , нәруыз жағымен митохондрия мембраналарына ілінеді, ал олардың коферменттері бос, сондықтан тербелгіш немесе айналғыш қозғалыста болады. Бұл БТның тізбегіне қатысатын ферменттердің протондарды немесе электрондарды бір біріне тасымалдауына ыңғайлылықты туғызады. БТ ферменттері тынысалу комплекстері немесе тынысалу ансамльдері түрінде орналасады. Тынысалу комплексін 4 ке бөледі: 1-комплекс құрамына коферменті ФМН болатын ФП, 2-ші коферменті ФАД болатын ФП, 3-ші Цхb мен Цхс1, 4-ші Цха мен Цха3. Сонымен бірге алғашқы үш комплекске күкіртті темірі бар нәруыздар кіреді, олардың рөлдері әлі толық анықталмаған, бірақ белгілі, олар оттектің бір электрондық тотықсыдануына қатысады, яғни олар пероксидтік тотығу түріне жатады. КоQ мен Цхс комплекстер құрамына кірмейді, себебі олардың біреуі майда, ал екіншісі суда ериді де, комплекстерді бір біріне байланыс- тырады: КоQ I мен II,111 комплекстерді , ал Цхс IIIті IV-комплекспен байланыстырады.
Тынысалу тізбегінде электрондардың тасымалдануы протондық градиентті туғызады, ал ол АТФ тің синтезіне әкеледі.
Тынысалу тізбегі арқылы өтетін электрондар ағымы тотығудан фосфорлану жолымен АТФ түрінде жинақталады.
АТФ тің түзілуі. Митчеллдің хемиосмотикалық теориясы
АТФ тің АДФ пен бейорганикалық фосфаттан тотығудан фосфорлану арқылы түзілуі митахондриялық мембананың ішкі жағымен қамтамасыз етіледі. БТ ның ферменттері митахондриялық мембананың ішкі бетінде орналасқан және протондар мен электрондарды тасымалдауға қатысады. Протондар НАДН2 ден убихинонға тасымалданғанда , протондар мембананың ішкі цитоплазмалық жағына қарай лақтырылады ( мембрана- аралық кеңістікке – митохондриялық мембрананың ішкі және сыртқы жақтарының аралық кеңіістігі), ал электрондар цитохромдық жүйе арқылы оттекке жіберіледі. Осының нәтижесінде митохондрия мембранасының ішкі және сыртқы беттері арасында потенциал айырымы туады. Потенциал айырымы митохондриялық мембрананың ішкі бетінің сыртқы жағында протондардың артық мөлшерінің, ал митохондриялық мембрананың ішкі бетінің ішкі жағында протондардың мөлшері кем болуының арқасында протондық градиент түзілуінен пайда болады. Мұндай протондардың айырымы протондардың қозғалысын протондық канал арқылы кері бағытта қамтамасыз етеді – митохондриялық матрикс кеңістігіне протондық канал арқылы. Бұл канал митохондриялық мембрананың ішкі бетінің ішкі жағында орналасқан АТФ-синтетазаның белсенділігін тудырады және ол АДФ пен бейорганикалық фосфаттан АТФ тің түзілуін қамтамасыз етеді. Сонымен, митохондрия матриксінде АТФ түзіледі. Осыдан АТФ ерекше тасымалдаушының көмегімен (транслоказа) жасуша цитоплазмасына тасымалданады. Осымен қатар бір уақытта осы фермент кері бағытта АДФ ты тасымалдайды. Бейорганикалық фосфаттың тасымалдануы 2 жүйемен іске асады – біріншісі рН градиентіне тәуелді, екіншісі - фосфаттың матрикске диффузиясын кері бағытта дикарбон қышқылы иондарына айырбастау (малат, ГЛУ) арқылы.
Хемиосмотикалық теория тынысалуды бақылауды, ажырату әсерін және митохондриальды жүйенің қызметін, алмаса тасымалдау жүйесін түсіндіре алады.
АТФ-синтаза, құрылысы және рөлі
АТФ ті синтездеудегі айналмалы катализдік механизм
АТФ-синтазаның қатысымен АТФ синтезінің механизмі айналмалы катализ деген атқа ие болды( роторлық катализ, ротациондық катализ).
АТФ-синтаза ферменті көптеген нәруыздық тізбектер арқылы, екі үлкен қалыптасқан тізбекті түзеді:
-
Fо компоненті (олигомицинге-сезімтал) – оның қызметі канал түзуші, ол арқылы тартылып шығарылған сутек иондары сыртқы матрикске қарай ағады. -
F1 компоненті (fraction 1, англ. -1 бөлім) – оның қызметі каталитикалық. Тек осы компонент протондық градиентті пайдаланып, АТФ ті синтездейді.
Fо компонентінің құрылысы
Бұл компонент мембранаға батырылған, цилиндр пішіндегі интегралды нәруыз, a және b типтегі суббірліктер мен 10-12 с типті суббірлік біріктірілгенкомплекс түрінде түзіледі. Әрбір c-суббірлік протондарды байланыстыратын теріс зарядты орталық – аспарагин қышқылының қалдығы. Бұл орталықтар сыртқа (мембранааралық кеңістікке) және ішке ( матрикске) қарай ашылған H+ иондарына арналған жартылай каналдармен әрекеттеседі, a- мен b-суббірліктер құрылымдық. Олардың қызметі - F1-компонентін мембранаға байланыстыруды қамтамасыз ету.
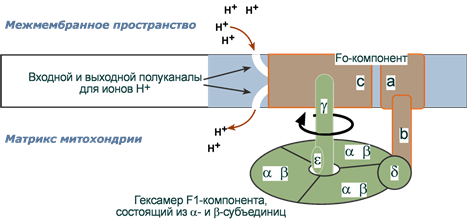
АТФ-синтазаның құрылысы
F1 компонентінің құрылысы
Бұл компоненттің молекуласы бес түрлі (3α, 3β, γ, δ, ε) тоғыз суббірліктерден тұрады. F1-компоненттің негізгі қызмет атқаратын суббірліктері 3α- және 3β-суббірліктерден тұратын гексамер. Гексамер δ-суббірлік арқылы b-суббірлікке байланысқан (Fo), ал ол өз кезегінде мембра- наға Fo-компонентттің a-суббірлігіне ілінген. Сонымен 3αβ гексамер бекітілген және қозғалмайды. АТФ синтезі жүретін каталитикалық орталық β-суббірлігінде болады.
γ-Суббірлік бір басымен мықты c-суббірлік (Fo) комплексімен байланысқан, ал басқа басымен 3αβ гексамердің ішіне кіріп тұрады. Онымен қоса қосымша минорлы ε суббірлік байланысқан.
F1 мен Fo дің бір бірімен әрекеттесуі
АТФ синтезі босатылған протондардың F0 комплексінің каналы арқылы өткен протондардың энергияларынан түзіледі .
Протондар мембранааралық кеңістіктен өздерінің байланысатын орталығы с-суббірлікке (Fo) жартылай канал арқылы жетеді, одан аспартатқа байланысады да оның теріс зарядтарын бейтараптайды. Зарядын жоғалтқан с-суббірлік өзінің конформациясын өзгертеді және Fo-комплексінің өз осі бойынша айналуын туғызады, ол сол уақытта митохондрия матриксіне бағытталған протондарды басқа жартылай каналға апарады. Матриксте H+ иондарының концентрациясы төмен болғандықтан, протондар оңай аспартаттан бөлініп шығады да ішке қарай кетеді, ал зарядталып қалған аспартат комплекстің басқа бағытта айналуына мүмкіндік бермейді.
H+ иондарын байланыстырғанда Fo-компоненттің c-суббірлік комплексі ғана айналып қоймайды, сонымен қатар онымен мықты байланыстағы F1-компоненттің γ-суббірлігі де айналады. γ–суббірлігінің өзегі қозғалмайтын 3αβ гексамердің ішінде айналады және әрбір айналыста 120° қа бұрылған уақытта кезек -кезек β-суббірліктерімен каталитикалық байланысқа түседі де олардың қызметін өзгертеді.
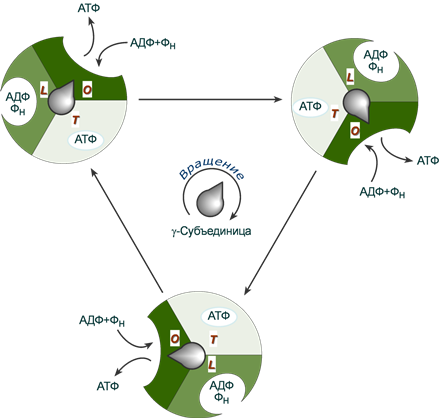
АТФ синтезі кезіндеγ-суббірлікің β-суббірлікпен әрекеттесуі
β-субьірліктер жұмыс істеу кезінде үш түрлі конформацияда бола алады:
-
loose, L (англ. Әлсіз байланысқан) – АДФ пен фосфат ионын ұстап тұрады, -
tight, T (англ. тығыз) –АДФ пен фосфат-ионын "қысады",яғни АТФ синтезі жүреді, -
open, O (англ. ашық) – осы жағдайда суббірлік АТФ ті босатады да , АДФ пен фосфат ионын алып қалады .
γ-суббірліктің әрбір бір айналымында (360º) АТФ тің үш молекуласы түзіледі.
Тынысалуды бақылау коэффициенті -Р/О туралы түсінік
Тотығудан фосфорлану(ТФ) қарқындылығы туралы пікірді эстерленген фосфаттың сіңірілген оттекке қатынасындағы шамасымен айтуға болады. Бұл қатынас Р/О коэффициентімен белгіленеді. Р/О коэффициенті–бейорганикалық фосфаттың моль санының АТФ түзуге кеткен әрбір сіңірілген оттек атомының санына қатынасы. Қалыпты жағдайда , егер БТ тізбегі ПФдан басталса , онда сіңірілген 1 атом оттекке 3 молекула бейорганикалық фосфат жұмсалады, бұл жағдайда Р/О = 3 ке тең болады. Коэффициент Р/О коэффициенті екіге тең болуы да мүмкін, егер БТ тізбегі ФАД қа тәуелді ДГдан басталса.
ТФ тынысалуды бақылауды жүргізу арқылы БТ жылдамдығын бақылайды. Тынысалуды бақылау – бұл бұзылмаған митохондриялардың қасиеттері. БТ ның барлық компоненттері бар болып, бірақ АДФ жоқ болса БТ ның жылдамдығы тежеледі. АДФ тың мөлшері көбейіп, ал АТФ тің мөлшері азайса, БТ ның жылдамдығы артады.
Тынысалуды бақылаудың бес жағдайы
| №№ | Тіндік тынысалу деңгейін шектейтін шарттар (гипоэнергетикалық жағдайдың себептері ) |
| 1жағдай | АДФ пен субстраттың жеткіліктігі |
| 2 жағдай | Тек субстраттың жеткіліктігі |
| 3 жағдай | БТ тізбегінің барлық субстраттары мен компоненттерінің концентрациялары қаныққан күйде болғанда осы тізбектің өзіндік қабілеттілігі. |
| 4 жағдай | Тек АДФ тың жеткіліктігі |
| 5 жағдай | Тек оттектің жеткіліктігі |
Кәзіргі кезде БТ мен ТФ ның арасында тығыз байланыс бар екендігін белгілі заттар мен басқа факторларды – БТ мен ТФ ны ажыратқыштарды, мысалға ала отырып (нитро- және фенолдың