Файл: Методические рекомендации по выполнению контрольной работы по дисциплине Химия.docx
Добавлен: 12.01.2024
Просмотров: 284
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
С2Н4(г) + 3О2(г) = 2СО2(г) + 2Н2О(г)
При сгорании 1 л С2Н4 (н.у.) выделяется 59,06 кДж теплоты. Определите стандартную энтальпию образования этилена.
30. Вычислите тепловой эффект и напишите термохимическое уравнение реакции между СО(г) и Н2(г), в результате которой образуются СН4(г) и Н2О(г). Сколько теплоты выделится в этой реакции, если получено 67,2 л метана в пересчете на нормальные условия?
31. Вычислите, сколько теплоты выделится при сгорании 165 л (н.у.) ацетилена С2Н2, если продуктами сгорания являются диоксид углерода и пары воды?
32. Тепловой эффект какой реакции равен теплоте образования метана? Вычислите теплоту образования 20 м3 метана, исходя из следующих термохимических уравнений:
Н2 (г) +1/2О2(г) = Н2О(ж); ∆Н0= -285,84 кДж;
С(к) + О2(г) = СО2(г); ∆Н0= -393,51 кДж;
СН4 (г) + 2О2(г) = 2Н2О(ж) + СО2(г); ∆Н0= -890,31 кДж.
33. При взаимодействии газообразных сероводорода и диоксида углерода образуются пары воды и сероуглерод CS2(г). Напишите термохимическое уравнение этой реакции и вычислите тепловой эффект образования 10 л сероуглерода.
34. Реакция горения аммиака выражается термохимическим уравнением
4NH3(г) + ЗО2 (г) = 2N2(r) + 6Н2О(ж); ∆Н0= -1530,28 кДж.
Вычислите теплоту образования 5 л NH3(г).
35. При восстановлении 25,4 г оксида меди (II) углем (с образованием СО) поглощается 16,48 кДж энергии. Определите стандартную энтальпию образования СuO.
36. Тепловой эффект какой реакции равен теплоте образования гидроксида кальция? Вычислите теплоту образования 20 кг гидроксида кальция, исходя из следующих термохимических уравнений:
Са(к) + 1/2О2 (г) = СаО(к); ∆Н0= -635,60 кДж;
Н2 (г) + 1/2О
2(г) = Н2О(ж); ∆Н0= -285,84 кДж;
СаО(к) + Н2О(ж) = Са(ОН)2(к); ∆Н0=-64,76 кДж.
37. При сгорании 1 л ацетилена (н.у) выделяется 56,053 кДж теплоты. Напишите термохимическое уравнение реакции, в результате которой образуются пары воды и диоксида углерода. Вычислите теплоту образования С2Н2(г).
38. Вычислите тепловой эффект и напишите термохимическое уравнение реакции горения 1 моль этана С2Н6(г), в результате которой образуются пары воды и диоксид углерода. Сколько теплоты выделится при сгорании 1 м3 этана в пересчете на нормальные условия?
39. При сгорании газообразного аммиака образуются пары воды и оксид азота. Сколько теплоты выделится при этой реакции, если получено 44,8 л NO в пересчете на нормальные условия?
40. Тепловой эффект реакции сгорания жидкого бензола с образованием паров воды и диоксида углерода равен -3135,58 кДж. Составьте термохимическое уравнение этой реакции и вычислите теплоту образования 10 л С6Н6(ж).
41. При сгорании 23г жидкого этилового спирта выделилось 617,42 кДж теплоты. Напишите термохимическое уравнение реакции, в результате которой образуются пары воды и диоксид углерода. Вычислите теплоту образования С2Н5ОН(ж).
42. Тепловой эффект какой реакции равен теплоте образования NO? Вычислите стандартную энтальпию образования NO из простых веществ, исходя из следующих термохимических уравнений:
4NH3(г) + 5О2(г) = 4NO (г) + 6 Н2О(ж), ∆Н0(1)= –1168,80 кДж (1)
4NH3(г) + 3О2(г) = 2N2 (г) + 6 Н2О(ж), ∆Н0(2) = –1530,28 кДж (2)
Сколько теплоты выделится при образовании 5 м3 NO?
43. Газообразный этиловый спирт С2H5OH можно получить при взаимодействии этилена С2Н4(г) и водяных паров. Вычислите тепловой эффект этой реакции и напишите термохимическое уравнение. Сколько теплоты выделится, если в реакции было израсходовано 100 л этилена (н.у.)?
44. Вычислите, какое количество теплоты выделилось при восстановлении Fe
2O3 металлическим алюминием, если было получено 335,1 г железа.
45 Реакция горения бензола выражается термохимическим уравнением
С6Н6(ж) + 71/2 О2 (г) = 6СО2(г) + ЗН2О(г); ∆Н0= ?
Вычислите тепловой эффект этой реакции, если известно, что молярная теплота парообразования бензола равна +33,9 кДж.
46. При растворении 16 г СаС2 в воде выделяется 31,27 кДж теплоты. Определите стандартную энтальпию образования Са(ОН)2.
47. Определите количество теплоты, выделившейся при взаимодействии 50 г фосфорного ангидрида с водой по реакции Р2О5(к) + H2O(ж) = 2HPO3(ж), если тепловые эффекты реакции равны
2Р (к) + 5½O2(г) = Р2О5(к), ∆Н0 = –1492 кДж
2Р (к) + H2(г) + 3O2(г) = 2HPO3(ж), ∆Н0 = –1964,8 кДж
48. Реакция горения метилового спирта выражается термохимическим уравнением
СН3ОН(ж) +3/2О2(г) = СО2(г) + 2Н2О (ж); ∆Н0= ?
Вычислите тепловой эффект этой реакции, если известно, что молярная теплота парообразования СН3ОН(ж) равна +37,4 кДж.
49. Определите стандартную энтальпию образования 200 г пентахлорида фосфора из простых веществ, исходя из следующих термохимических уравнений:
2Р + 3Сl2 = 2РСl3, ∆Н0(1)= –554,0 кДж (1)
РСl3 + Сl2 = РСl5, ∆Н0(2) = –92,4 кДж (2)
50. Кристаллический хлорид аммония образуется при взаимодействии газообразных аммиака и хлороводорода. Напишите термохимическое уравнение этой реакции, предварительно вычислив ее тепловой эффект. Сколько теплоты выделится, если в реакции было израсходовано 10 л аммиака в пересчете на нормальные условия?
3.Направленность химических процессов. Примеры решения задач.
При решении задач этого раздела следует пользоваться табл. 1-3 приложения.
Пример 3.1. Прямая или обратная реакция будет протекать при стандартных условиях в системе
СН4(г) + СО2 = 2СО(г) + 2Н2(г)
Решение.Вычислим ∆G прямой реакции. (Значения ∆G соответствующих веществ приведены в табл. 6.) Зная, что ∆Gесть функция состояния и что ∆Gдля простых веществ, находящихся в устойчивых при стандартных условиях агрегатных состояниях, равны нулю, находим ∆G процесса:
∆G298 = 2(-137,27) + 2(0) - (-50,79 - 394,38) = + 170,63 кДж.
То, что ∆G > 0, указывает на невозможность самопроизвольного протекания прямой реакции при Т = 298 0К и давлении взятых газов равном 1,013 • 105 Па (760 мм рт. ст. = 1 атм).
Пример 3.2. Определите температуру, при которой установится равновесие в системе СаСО3 (к)
Решение. Для определения температуры, при которой установится равновесие, воспользуемся уравнением:Травн.=
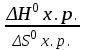 . Для этого сначала вычисляем ∆Н0х.р. и ∆S0х.р.по формулам:
. Для этого сначала вычисляем ∆Н0х.р. и ∆S0х.р.по формулам: 0х.р. = (f 0СаО + f 0СО2) – f 0СаСО3,
S0х.р. = (S0СаО + S0СО2)– S0СаСО3
Используя справочные данные из табл.1, получаем
0х.р. = [– 635,5 + (–393,5)] – (–1207,1) = 178,1 кДж,
S0х.р. = (39,7 + 213,7) – 92,9 = 160,5 Дж/К или 0,1605 кДж/К
Отсюда, температура, при которой устанавливается равновесие:
Травн = 178,1 / 0,1605 = 1109,50 К
Пример 3.3. Вычислите 0х.р, ∆S 0х.р. и G 0T реакции, протекающей по уравнению: Fe2O3(к) + 3C(к) = 2Fe(к) + 3CO(г).
Возможна ли реакция восстановления Fe2O3углеродом при температуре 298 и 1000
0 К? Зависимостью 0х.р. и S0х.р от температуры пренебречь.
Решение.Вычисляем 0х.р. и S0х.р.
0х.р. = (3f 0CO + 2f 0Fe) – (f 0Fe2O3 + 3f 0 C)
0х.р.= [3(–110,5) + 2·0] – [–822,2 + 3·0] = –331,5 + 822,2 = +490,7 кДж;
S0х.р. = (2S0Fe +3S0CO) – (S0 Fe2O3 + 3S0C)
S0х. р = (2·27,2 +3·197,5) – (89,9 + 3·5,7) = 539,9 Дж/К или 0,540 кДж/0К
Энергию Гиббса при соответствующих температурах находим из соотношения
G0х.р=0х.р – ТS0х.р
G0298 = 490,7 – 2980,540 = +329,8 кДж
G01000 = 490,7 – 10000,540 = –49,3 кДж
Так как G0298 > 0, а G01000 < 0, то восстановление Fe2O3 углеродом возможно при 1000 0К и невозможно при 298 0К.
Контрольные вопросы
51. Уменьшается или увеличивается энтропия при переходах: а) из воды в пар; б) графита в алмаз? Почему? Вычислите ∆G0х.р для каждого превращения. Сделайте вывод о количественном изменении энтропии при фазовых и аллотропических превращениях.
52. Какие из карбонатов: ВеСО3, СаСО3 или ВаСО3 — можно получить при взаимодействии соответствующих оксидов с СО2? Какая реакция идет наиболее энергично? Сделайте вывод, вычислив ∆G0298 реакций.
53. Какой из двух процессов разложения нитрата аммония наиболее вероятен при 298К?
NH4NO3 (к) → N2O (г) + 2H2O(г) (1)
NH4NO3 (к) → N2 (г) + ½O2 (г) + 2H2O(г) (2)
Ответ обоснуйте, рассчитав ∆G0х.р.
54. Чем можно объяснить, что при стандартных условиях невозможна экзотермическая реакция:
Н2(г) + СО2(г) = СО(г) + Н2О(ж); ∆Н0х.р.