Файл: Методические рекомендации по выполнению контрольной работы по дисциплине Химия.docx
Добавлен: 12.01.2024
Просмотров: 283
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
, = -2,85 кДж.
Зная тепловой эффект реакции и абсолютные стандартные энтропии соответствующих веществ, определите ∆G0298 этой реакции.
55. Исходя из стандартных теплот образования и абсолютных стандартных энтропий соответствующих веществ, вычислите реакции, протекающей по уравнениям:
4NH3(г) + 5О2(г) = 4NO(г) + 6Н2О(г)
NH3(г) + НС1(г) = NH4CI(к)
Может ли эта реакция при стандартных условиях идти самопроизвольно?
56. На основании стандартных теплот образования и абсолютных стандартных энтропии соответствующих веществ вычислите ∆G0298 реакций, протекающих по уравнениям:
СО(г) + ЗН2(г) = СН4(г) + Н2О(г)
N2 (г) + 3Н2(г) = 2NH3(г).
Возможна ли эта реакция при стандартных условиях?
57. Реакция горения ацетилена идет по уравнению:
С2Н2(г) + 5/2О2(г) = 2СО2(г) + Н2О(ж)
Вычислите ∆G0298 и ∆S0298 реакции. Объясните уменьшение энтропии в результате этой реакции.
58. При какой температуре наступит равновесие системы
4НС1(г) + О2(г) = 2Н2О(г) + 2С12(г); ∆Н0х.р., = -114,42 кДж ?
Хлор или кислород в этой системе является более сильным окислителем и при какой температуре?
59. Вычислите ∆Н0 298, ∆S0298 и ∆G0298 реакции, протекающей по уравнению
ТiО2(к) + 2С(к) = Ti(к) + 2СО(г)
Возможна ли реакция восстановления TiO2 углеродом при 1000 и 3000 К?
60. Вычислите ∆Н0х.р.
, ∆S0х.р. и ∆G0Т реакции, протекающей по уравнению
Fe2O3(к) + 3Н2(г) = 2Fe(к) + 3Н2O(г).
Возможна ли реакция восстановления Fe2O3 водородом при температурах 500 и 1500 К? Зависимостью ∆Н0х.р., ∆S0х.р от температуры пренебречь.
61. Вычислите ∆G0298 для следующих реакций:
a) 2NaF(к) + Cl2(г) = 2NaCl(к) + F2(г)
б) PbO2(к) + 2Zn(к) = Pb(к) + 2ZnO(к)
Можно ли получить фтор по реакции (а) и восстановить PbO2 цинком по реакции (б).
62. Вычислите значения ∆G0х.р. следующих реакций восстановления оксида железа (III)
Fe2O3 (к) + 3Н2(г) = 2Fe(к) + 3Н2О(г) (1)
2Fe2O3 (к) + 3С(к) = 4Fe(к) + 3СО2(г) (2)
Fe2O3 (к) + 3СO(г) = 2Fe(к) + 3СО2(г) (3)
Протекание какой из этих реакций наиболее вероятно ?
63. Вычислите изменения энтропии для реакций, протекающих по уравнениям:
2СН4(г) = С2Н2(г) + ЗН2(г)
N2(г) + 3H2(г) = 2NH3(г)
С (графит) + О2(г) = СО2(г)
Почему в этих реакциях 0 > ∆S0298 > 0.
64. Рассчитайте энергию Гиббса химических реакций, протекающих по уравнениям:
CaO(к) + Н2О(г) = Са(ОН)2 (к) (1)
Р2О5(к) + 3Н2О(г) = 2Н3РО4 (к) (2)
и определите, какой из двух оксидов CaO или Р2О5 при стандартных условиях лучше поглощает водяные пары.
65. Восстановление Fe3O4 оксидом углерода идет по уравнению:
Fe3O4(к) + СО(г) = 3FeO(K) + СО2(г)
Вычислите ∆G0298 и сделайте вывод о возможности самопроизвольного протекания этой реакции при стандартных условиях. Чему равна ∆S0298 в этом процессе? При какой температуре начнется реакция восстановления Fe3O4?
4. Химическая кинетика и равновесие. Примеры решения задач
Пример 4.1. При 3230 К некоторая реакция заканчивается за 30 с. Определите, как изменится скорость реакции и время ее протекания при 2830 К, если температурный коэффициент скорости реакции равен 2.
Решение. По правилу Вант-Гоффа находим, во сколько раз изменится скорость реакции:
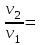
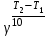 =
= 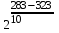 = 2–4 =
= 2–4 = 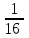 .
.
Скорость реакции уменьшается в 16 раз. Скорость реакции и время ее протекания связаны обратно пропорциональной зависимостью. Следовательно, время протекания данной реакции увеличится в 16 раз и составит 30 16 = 480с = 8 мин.
Пример 4.2. При некоторой температуре в системе
N2(г) + 3Н2(г) 2NH3(г)
2NH3(г)
равновесные концентрации составляли (моль/л): [N2]= 1,5; [H2] = 1,7; [NH3] = 2,6.
Вычислите константу равновесия этой реакции и исходные концентрации азота и водорода.
Решение. Константа равновесия данной реакции выражается уравнением
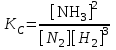 . Подставляя данные задачи, получаем
. Подставляя данные задачи, получаем 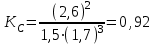 .
.
Исходные концентрации азота и водорода находим на основе уравнения реакции. Согласно уравнению реакции на образование 2 моль NH3 расходуется 1 моль N.2. По условию задачи образовалось 2,6 моль NH
3, на что израсходовалось 1,3 моль N2. Учитывая равновесную концентрацию азота, находим его исходную концентрацию СN2 = 1,5 + 1,3 = 2,8 моль/л.
По уравнению реакции на образование 2 моль NH3 необходимо 3 моль H2, а для получения 2,6 моль NH3 требуется 32,6 / 2 = 3,9 моль H2. Исходная концентрация водорода равна СН2 = 1,7 + 3,9 = 5,6 моль/л. Таким образом, КС = 0,92, исходные концентрации составляли СN2 = 2,8 моль/л, СH2 = 5,6 моль/л.
Пример 4.3. Эндотермическая реакция разложения пентахлорида фосфора протекает по уравнению
РС15(г) РС13(г) + С12(г); ∆Н0х.р =+92,59 кДж.
РС13(г) + С12(г); ∆Н0х.р =+92,59 кДж.
Как надо изменить: а) температуру; б) давление; в) концентрацию, чтобы сместить равновесие в сторону прямой реакции — разложения РС15?
Решение. Смещением или сдвигом химического равновесия называют изменение равновесных концентраций реагирующих веществ в результате изменения одного из условий реакции. Направление, в котором сместилось равновесие, определяется по принципу Ле Шателье: а) так как реакция разложения РС15 эндотермическая (∆Н0х.р > 0), то для смещения равновесия в сторону прямой реакции нужно повысить температуру: б) так как в данной системе разложение РС15 ведет к увеличению объема (из одной молекулы газа образуются две газообразные молекулы), то для смещения равновесия в сторону прямой реакции надо уменьшить давление; в) смещения равновесия в указанном направлении можно достигнуть как увеличением концентрации РС15, так и уменьшением концентрации РС13 или С12.
Пример 4.4. Реакция между веществами А и В выражается уравнением 2А + В = D. Начальные концентрации составляют: СА = 5 моль/л, СВ = 3,5 моль/л. Константа скорости равна 0,4. Вычислите скорость реакции в начальный момент и в тот момент, когда в реакционной смеси останется 60% вещества А.
Решение. По закону действия масс v =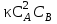 . В начальный момент скорость v1 = 0,4 52 3,5 = 35. По истечении некоторого времени в реакционной смеси останется 60% вещества А, т. е. концентрация вещества А станет равной 5 0,6 = 3 моль/л. Значит, концентрация А уменьшилась на 5 – 3 = 2 моль/л. Так как А и В взаимодействуют между собой в соотношении 2:1, то концентрация вещества В уменьшилась на 1 моль и стала равной 3,5 – 1 = 2,5 моль/л. Следовательно, v2 = 0,4 32 2,5 = 9.
. В начальный момент скорость v1 = 0,4 52 3,5 = 35. По истечении некоторого времени в реакционной смеси останется 60% вещества А, т. е. концентрация вещества А станет равной 5 0,6 = 3 моль/л. Значит, концентрация А уменьшилась на 5 – 3 = 2 моль/л. Так как А и В взаимодействуют между собой в соотношении 2:1, то концентрация вещества В уменьшилась на 1 моль и стала равной 3,5 – 1 = 2,5 моль/л. Следовательно, v2 = 0,4 32 2,5 = 9.
Пример 4.5. Реакция протекает по уравнению А + В D + F. Определите равновесные концентрации реагирующих веществ, если исходные концентрации веществ А и В соответственно равны 2 и 1,2 моль/л, а константа равновесия реакции КС = 1.
D + F. Определите равновесные концентрации реагирующих веществ, если исходные концентрации веществ А и В соответственно равны 2 и 1,2 моль/л, а константа равновесия реакции КС = 1.
Решение. Так как все вещества в данной реакции реагируют в одинаковых соотношениях, обозначим изменение концентрации всех реагирующих веществ через x. К моменту установления равновесия образовалось х моль D и х моль F и соответственно [D] = x; [F] = x. По уравнению реакции на столько же уменьшились концентрации А и В, т. е. [A] = 2 – x; [B] = 1,2 – x. Подставим равновесные концентрации в выражение константы равновесия
КС=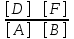 ; 1=
; 1=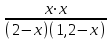 ; х = 0,75.
; х = 0,75.
Отсюда равновесные концентрации равны: [D] = 0,75 моль/л; [F] = 0,75 моль/л; [A] = 2 – 0,75 = 1,25 моль/л; [B] = 1,2 – 0,75 = 0,45 моль/л.
Пример 4.6. Реакция протекает по уравнению 2SO2 + O2 2SO3. В каком направлении сместится химическое равновесие, если объем системы уменьшить в 3 раза?
2SO3. В каком направлении сместится химическое равновесие, если объем системы уменьшить в 3 раза?
Решение. В начальный момент времени скорости прямой и обратной реакции были следующие: Vпр =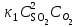 Vобр =
Vобр = 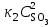
Зная тепловой эффект реакции и абсолютные стандартные энтропии соответствующих веществ, определите ∆G0298 этой реакции.
55. Исходя из стандартных теплот образования и абсолютных стандартных энтропий соответствующих веществ, вычислите реакции, протекающей по уравнениям:
4NH3(г) + 5О2(г) = 4NO(г) + 6Н2О(г)
NH3(г) + НС1(г) = NH4CI(к)
Может ли эта реакция при стандартных условиях идти самопроизвольно?
56. На основании стандартных теплот образования и абсолютных стандартных энтропии соответствующих веществ вычислите ∆G0298 реакций, протекающих по уравнениям:
СО(г) + ЗН2(г) = СН4(г) + Н2О(г)
N2 (г) + 3Н2(г) = 2NH3(г).
Возможна ли эта реакция при стандартных условиях?
57. Реакция горения ацетилена идет по уравнению:
С2Н2(г) + 5/2О2(г) = 2СО2(г) + Н2О(ж)
Вычислите ∆G0298 и ∆S0298 реакции. Объясните уменьшение энтропии в результате этой реакции.
58. При какой температуре наступит равновесие системы
4НС1(г) + О2(г) = 2Н2О(г) + 2С12(г); ∆Н0х.р., = -114,42 кДж ?
Хлор или кислород в этой системе является более сильным окислителем и при какой температуре?
59. Вычислите ∆Н0 298, ∆S0298 и ∆G0298 реакции, протекающей по уравнению
ТiО2(к) + 2С(к) = Ti(к) + 2СО(г)
Возможна ли реакция восстановления TiO2 углеродом при 1000 и 3000 К?
60. Вычислите ∆Н0х.р.
, ∆S0х.р. и ∆G0Т реакции, протекающей по уравнению
Fe2O3(к) + 3Н2(г) = 2Fe(к) + 3Н2O(г).
Возможна ли реакция восстановления Fe2O3 водородом при температурах 500 и 1500 К? Зависимостью ∆Н0х.р., ∆S0х.р от температуры пренебречь.
61. Вычислите ∆G0298 для следующих реакций:
a) 2NaF(к) + Cl2(г) = 2NaCl(к) + F2(г)
б) PbO2(к) + 2Zn(к) = Pb(к) + 2ZnO(к)
Можно ли получить фтор по реакции (а) и восстановить PbO2 цинком по реакции (б).
62. Вычислите значения ∆G0х.р. следующих реакций восстановления оксида железа (III)
Fe2O3 (к) + 3Н2(г) = 2Fe(к) + 3Н2О(г) (1)
2Fe2O3 (к) + 3С(к) = 4Fe(к) + 3СО2(г) (2)
Fe2O3 (к) + 3СO(г) = 2Fe(к) + 3СО2(г) (3)
Протекание какой из этих реакций наиболее вероятно ?
63. Вычислите изменения энтропии для реакций, протекающих по уравнениям:
2СН4(г) = С2Н2(г) + ЗН2(г)
N2(г) + 3H2(г) = 2NH3(г)
С (графит) + О2(г) = СО2(г)
Почему в этих реакциях 0 > ∆S0298 > 0.
64. Рассчитайте энергию Гиббса химических реакций, протекающих по уравнениям:
CaO(к) + Н2О(г) = Са(ОН)2 (к) (1)
Р2О5(к) + 3Н2О(г) = 2Н3РО4 (к) (2)
и определите, какой из двух оксидов CaO или Р2О5 при стандартных условиях лучше поглощает водяные пары.
65. Восстановление Fe3O4 оксидом углерода идет по уравнению:
Fe3O4(к) + СО(г) = 3FeO(K) + СО2(г)
Вычислите ∆G0298 и сделайте вывод о возможности самопроизвольного протекания этой реакции при стандартных условиях. Чему равна ∆S0298 в этом процессе? При какой температуре начнется реакция восстановления Fe3O4?
4. Химическая кинетика и равновесие. Примеры решения задач
Пример 4.1. При 3230 К некоторая реакция заканчивается за 30 с. Определите, как изменится скорость реакции и время ее протекания при 2830 К, если температурный коэффициент скорости реакции равен 2.
Решение. По правилу Вант-Гоффа находим, во сколько раз изменится скорость реакции:
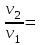
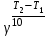 =
= 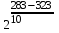 = 2–4 =
= 2–4 = 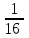 .
.Скорость реакции уменьшается в 16 раз. Скорость реакции и время ее протекания связаны обратно пропорциональной зависимостью. Следовательно, время протекания данной реакции увеличится в 16 раз и составит 30 16 = 480с = 8 мин.
Пример 4.2. При некоторой температуре в системе
N2(г) + 3Н2(г)
равновесные концентрации составляли (моль/л): [N2]= 1,5; [H2] = 1,7; [NH3] = 2,6.
Вычислите константу равновесия этой реакции и исходные концентрации азота и водорода.
Решение. Константа равновесия данной реакции выражается уравнением
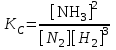 . Подставляя данные задачи, получаем
. Подставляя данные задачи, получаем 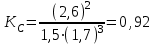 .
.Исходные концентрации азота и водорода находим на основе уравнения реакции. Согласно уравнению реакции на образование 2 моль NH3 расходуется 1 моль N.2. По условию задачи образовалось 2,6 моль NH
3, на что израсходовалось 1,3 моль N2. Учитывая равновесную концентрацию азота, находим его исходную концентрацию СN2 = 1,5 + 1,3 = 2,8 моль/л.
По уравнению реакции на образование 2 моль NH3 необходимо 3 моль H2, а для получения 2,6 моль NH3 требуется 32,6 / 2 = 3,9 моль H2. Исходная концентрация водорода равна СН2 = 1,7 + 3,9 = 5,6 моль/л. Таким образом, КС = 0,92, исходные концентрации составляли СN2 = 2,8 моль/л, СH2 = 5,6 моль/л.
Пример 4.3. Эндотермическая реакция разложения пентахлорида фосфора протекает по уравнению
РС15(г)
Как надо изменить: а) температуру; б) давление; в) концентрацию, чтобы сместить равновесие в сторону прямой реакции — разложения РС15?
Решение. Смещением или сдвигом химического равновесия называют изменение равновесных концентраций реагирующих веществ в результате изменения одного из условий реакции. Направление, в котором сместилось равновесие, определяется по принципу Ле Шателье: а) так как реакция разложения РС15 эндотермическая (∆Н0х.р > 0), то для смещения равновесия в сторону прямой реакции нужно повысить температуру: б) так как в данной системе разложение РС15 ведет к увеличению объема (из одной молекулы газа образуются две газообразные молекулы), то для смещения равновесия в сторону прямой реакции надо уменьшить давление; в) смещения равновесия в указанном направлении можно достигнуть как увеличением концентрации РС15, так и уменьшением концентрации РС13 или С12.
Пример 4.4. Реакция между веществами А и В выражается уравнением 2А + В = D. Начальные концентрации составляют: СА = 5 моль/л, СВ = 3,5 моль/л. Константа скорости равна 0,4. Вычислите скорость реакции в начальный момент и в тот момент, когда в реакционной смеси останется 60% вещества А.
Решение. По закону действия масс v =
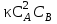 . В начальный момент скорость v1 = 0,4 52 3,5 = 35. По истечении некоторого времени в реакционной смеси останется 60% вещества А, т. е. концентрация вещества А станет равной 5 0,6 = 3 моль/л. Значит, концентрация А уменьшилась на 5 – 3 = 2 моль/л. Так как А и В взаимодействуют между собой в соотношении 2:1, то концентрация вещества В уменьшилась на 1 моль и стала равной 3,5 – 1 = 2,5 моль/л. Следовательно, v2 = 0,4 32 2,5 = 9.
. В начальный момент скорость v1 = 0,4 52 3,5 = 35. По истечении некоторого времени в реакционной смеси останется 60% вещества А, т. е. концентрация вещества А станет равной 5 0,6 = 3 моль/л. Значит, концентрация А уменьшилась на 5 – 3 = 2 моль/л. Так как А и В взаимодействуют между собой в соотношении 2:1, то концентрация вещества В уменьшилась на 1 моль и стала равной 3,5 – 1 = 2,5 моль/л. Следовательно, v2 = 0,4 32 2,5 = 9.Пример 4.5. Реакция протекает по уравнению А + В
Решение. Так как все вещества в данной реакции реагируют в одинаковых соотношениях, обозначим изменение концентрации всех реагирующих веществ через x. К моменту установления равновесия образовалось х моль D и х моль F и соответственно [D] = x; [F] = x. По уравнению реакции на столько же уменьшились концентрации А и В, т. е. [A] = 2 – x; [B] = 1,2 – x. Подставим равновесные концентрации в выражение константы равновесия
КС=
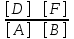 ; 1=
; 1=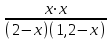 ; х = 0,75.
; х = 0,75.Отсюда равновесные концентрации равны: [D] = 0,75 моль/л; [F] = 0,75 моль/л; [A] = 2 – 0,75 = 1,25 моль/л; [B] = 1,2 – 0,75 = 0,45 моль/л.
Пример 4.6. Реакция протекает по уравнению 2SO2 + O2
Решение. В начальный момент времени скорости прямой и обратной реакции были следующие: Vпр =
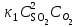 Vобр =
Vобр =