ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 29.04.2024
Просмотров: 117
Скачиваний: 2
СОДЕРЖАНИЕ
1. Основные положения, термины, определения
2. Исследование использования лекарственных средств при лечении хронических заболеваний
2.1 Источники информации при проведении фармакоэпидемиологических исследований
2.2 Частота и структура назначения лекарственных средств
2.6 Распределение лекарственных средств по степени затратности (авс-анализ)
2.7 Особенности исследования использования лекарственных средств при хронических заболеваниях
3. Моделирование применения лекарственных средств в реальной популяции больных
3.2 Математическое моделирование клинической эффективности применения лекарственных средств
3.3. Фармакоэкономическая оценка альтернатив при анализе лечения хронических заболеваний
P![]() (incremental)
– доля пациентов, имеющих показания к
лечению (eligible),
у которых возможно получить прирост
эффективности при назначении ЛС. Этот
показатель рассчитывается как разность
доли пациентов, имеющих показания к
лечению P
(incremental)
– доля пациентов, имеющих показания к
лечению (eligible),
у которых возможно получить прирост
эффективности при назначении ЛС. Этот
показатель рассчитывается как разность
доли пациентов, имеющих показания к
лечению P![]() (eligible)
и доли пациентов, которые уже получают
ЛС P
(eligible)
и доли пациентов, которые уже получают
ЛС P![]() (treated)
и имеют противопоказания P
(treated)
и имеют противопоказания P![]() (contra-indication)
и непереносимость P
(contra-indication)
и непереносимость P![]() (intolerance
) препарата:
(intolerance
) препарата:
|
P |
(17) |
r![]() (untreated)
–
риск
неблагоприятного клинического исхода
среди пациентов с интересующим
заболеванием, не принимающих лекарственный
препарат:
(untreated)
–
риск
неблагоприятного клинического исхода
среди пациентов с интересующим
заболеванием, не принимающих лекарственный
препарат:
|
r |
(18) |
где
(1-P![]() )
– доля пациентов, не принимающих препарат
)
– доля пациентов, не принимающих препарат
(P![]()
![]() (1-RRR))
– доля пациентов, принимающих ЛП, но
без эффекта
(1-RRR))
– доля пациентов, принимающих ЛП, но
без эффекта
risk – значение интересующих клинических исходов у пациентов с заболеванием в реальной клинической практике;
P![]() –
доля пациентов, имеющих показания к
лечению, но не получающих лечения.
Рассчитывается как разность между долей
пациентов имеющих показания к лечению
(P
–
доля пациентов, имеющих показания к
лечению, но не получающих лечения.
Рассчитывается как разность между долей
пациентов имеющих показания к лечению
(P![]() ),
и долями пациентов, имеющих противопоказания
(P
),
и долями пациентов, имеющих противопоказания
(P![]() )
и непереносимость (P
)
и непереносимость (P![]() ):
):
|
P |
(19) |
r![]() (
probability
of
event
/ mean
number
of
events
per
patien
per
eligible
but
untreated
patient)
– вероятность события или среднее число
событий для пациентов, имеющих показания
к лечению, но не получающих лечения.
Величина r
(
probability
of
event
/ mean
number
of
events
per
patien
per
eligible
but
untreated
patient)
– вероятность события или среднее число
событий для пациентов, имеющих показания
к лечению, но не получающих лечения.
Величина r![]() при
использовании в расчетах потенциального
эффекта для ранее не применявшихся
препаратов не требует коррекции и можно
использовать среднее число событий у
пациента с определенным заболеванием
без учета проводимого больным лечения;
при
использовании в расчетах потенциального
эффекта для ранее не применявшихся
препаратов не требует коррекции и можно
использовать среднее число событий у
пациента с определенным заболеванием
без учета проводимого больным лечения;
P![]() (adherence)
– приверженность к лечению (соблюдение
пациентом назначенного лечения). Если
данные о приверженности к лечению
отсутствуют, показатель равен единице
и считается, что все больные принимают
ЛС в соответствии с инструкцией (что на
самом деле бывает очень редко);
(adherence)
– приверженность к лечению (соблюдение
пациентом назначенного лечения). Если
данные о приверженности к лечению
отсутствуют, показатель равен единице
и считается, что все больные принимают
ЛС в соответствии с инструкцией (что на
самом деле бывает очень редко);
RRR (relative risk reduction) – снижение относительного риска, связанное с лечебным вмешательством. Снижение относительного риска отражает уменьшение исходного риска в группе изучаемого вмешательства в отношении интересующего клинического исхода.
Ряд
значений для проведения вычислений
получают из данных локального аудита
лекарственной терапии или локального
фармакоэпидемиологического исследования:
P![]() ,
P
,
P![]() ,
risk.
Данные о доле больных с противопоказаниями
(P
,
risk.
Данные о доле больных с противопоказаниями
(P![]() ),
непереносимостью (P
),
непереносимостью (P![]() )
и о приверженности (P
)
и о приверженности (P![]() )
больных либо берутся из РКИ, либо так
же могут быть получены при проведении
ФИ.
)
больных либо берутся из РКИ, либо так
же могут быть получены при проведении
ФИ.
Рассмотрим примеры проведения моделирования. В примерах рассчитаны показатели предотвращенных клинических исходов (PPE и NEPP) для ЛС, назначаемых при ХОБЛ (тиотропия бромид и ипратропия бромид) и в постинфарктном периоде (симвастатин) с целью предупреждения неблагоприятных событий. Оба показателя рассчитаны для населения Республики Беларусь.
Данные получены из проведенных в 2004 году в г. Минске фармакоэпидемиологических исследований 186 больных ХОБЛ и 405 больных, перенесших инфаркт. Сделаны следующие выводы:
при назначении лекарственного препарата «А» (тиотропия бромид) больным ХОБЛ по показаниям, соответствующим клиническим рекомендациям, у всех пациентов с диагностированным и учтенным системой здравоохранения заболеванием удалось бы избежать 37987 обострений в течение одного года. У 186 больных ХОБЛ при применении препарата «А» удалось бы предотвратить 46,5 обострений в течение одного года (пример 9).
при назначении препарата «Б» (ипратропия бромид) больным ХОБЛ по показаниям, соответствующим клиническим рекомендациям, у пациентов с диагностированным и учтенным системой здравоохранения заболеванием удалось бы избежать 8292 обострения в течение одного года. У 186 больных ХОБЛ при применении препарата «Б» удалось бы предотвратить 10 обострений в течение одного года (пример 10).
при назначении препарата «В» (симвастатин) больным, перенесшим инфаркт миокарда, по показаниям, соответствующим клиническим рекомендациям, удалось бы предотвратить 16 случаев сердечно-сосудистой смерти в течение трех лет (пример 11).
Пример 9: рассчитать число обострений, которое удалось бы предотвратить в течение одного года у пациентов при применении нового лекарственного препарата А.
Решение: Воспользуемся формулой (16), в которую подставим следующие числовые значения:
размер популяции n = 9600тыс. человек;
распространенность заболевания P
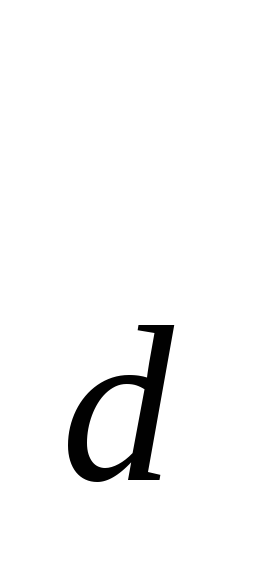 = 1583 на 100тыс. населения;
= 1583 на 100тыс. населения;доля пациентов, имеющих показания к лечению, по данным локального аудита схем лечения интересующего заболевания P
 = 0,98;
= 0,98;доля пациентов, у которых могут встречаться непереносимость ЛС P
 и (или) побочные эффекты P
и (или) побочные эффекты P равна 0,09 (по данным рандомизированных
клинических исследований – доля
пациентов в группе лечения выбывших
из исследования в связи с непереносимостью
или побочным действием препарата);
равна 0,09 (по данным рандомизированных
клинических исследований – доля
пациентов в группе лечения выбывших
из исследования в связи с непереносимостью
или побочным действием препарата);среднее число обострений на одного пациента в год r
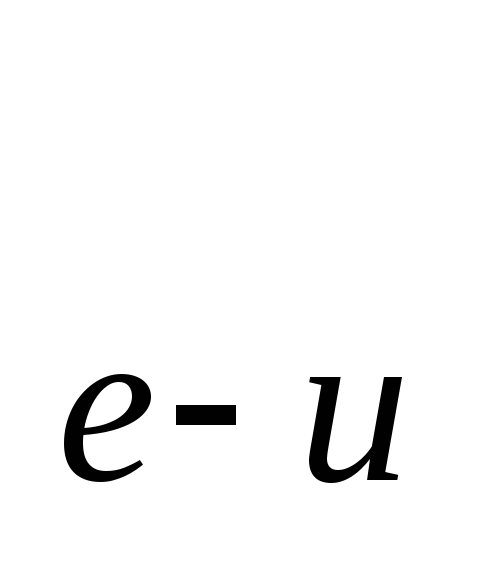 = 1,17;
= 1,17;снижение относительного риска для числа обострений на одного пациента в год по данным рандомизированных клинических исследований RRR = 0,24.
В результате получаем, что PPE = 37987 обострений:
PPE =
n![]() P
P![]()
![]() P
P![]()
![]() r
r![]()
![]() RRR
RRR![]() P
P![]() =
=
= 9600000
![]()
![]()
![]() (0,98
– 0,09)
(0,98
– 0,09)
![]() 1,17
1,17
![]() 0,24 = 37987
0,24 = 37987
Таким образом, при назначении ЛС «А» по показаниям, соответствующим клиническим рекомендациям, у всех пациентов с диагностированным и учтенным системой здравоохранения заболеванием удалось бы избежать 37987 обострений в течение одного года. Аналогичные расчеты были проведены для 186 больных, включенных в ФИ:
PPE
= n![]() P
P![]()
![]() P
P![]()
![]() r
r![]()
![]() RRR
RRR![]() P
P![]() =
=
= 186
![]() (0,98
– 0,09)
(0,98
– 0,09)
![]() 1,17
1,17
![]() 0,24
0,24
![]() 1
= 46,5.
1
= 46,5.
У 186 больных при применении препарата «А» удалось бы предотвратить 46,5 обострений в течение одного года.
Пример 10: Рассчитать число обострений, которое удалось бы предотвратить в течение одного года у пациентов при применении ЛС «Б». Препарат «Б» применяется редко или не в соответствии с рекомендуемыми режимами. Длительность РКИ, обнаруженных при поиске в электронных и прочих источниках, составили не более трех месяцев.
Решение: Воспользуемся формулой (15), в которую подставим следующие числовые значения:
размер популяции n = 9600тыс. человек;
распространенность заболевания P
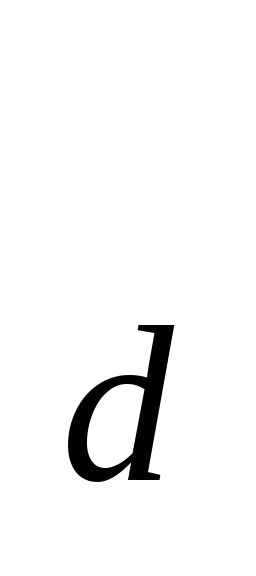 = 1583 на 100тыс. населения;
= 1583 на 100тыс. населения;доля пациентов, имеющих показания к лечению, по данным локального аудита схем лечения интересующего заболевания P
 = 0,98;
= 0,98;доля больных, получающих препарат на регулярной основе P
 = 0,096;
= 0,096;доля пациентов, у которых могут встречаться непереносимость ЛС P
 и (или) побочные эффекты P
и (или) побочные эффекты P составляет 0,095 (по данным рандомизированных
клинических исследований – доля
пациентов в группе лечения выбывших
из исследования в связи с непереносимостью
или побочным действием препарата);
составляет 0,095 (по данным рандомизированных
клинических исследований – доля
пациентов в группе лечения выбывших
из исследования в связи с непереносимостью
или побочным действием препарата);доля пациентов, перенесших, по крайней мере, одно обострение в три месяца, по данным локального аудита r
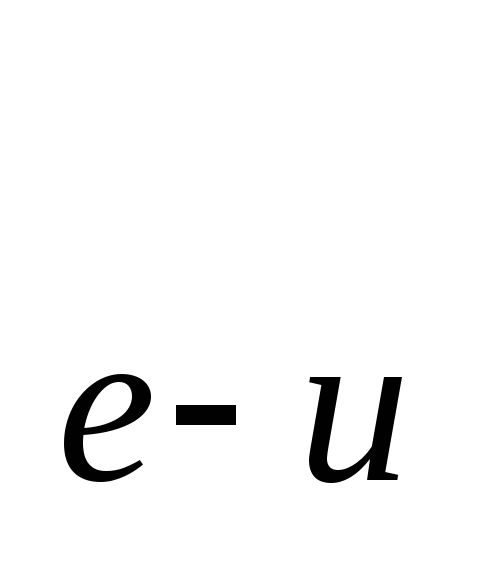 = 0,167;
= 0,167;среднее число обострений на одного пациента в три месяца – 1,15 (оба показателя рассчитаны при проведении ФИ);
снижение относительного риска для числа пациентов, перенесших, по крайней мере, одно обострение в три месяца, по данным рандомизированных клинических исследований RRR = 0,09.
В результате получаем, что NEPP = 1803 чел., или 1,2% от общей популяции избежали бы, по крайней мере, одного обострения в три месяца:
NEPP
= n
![]() P
P![]()
![]() r
r![]()
![]() P
P![]()
![]() RRR
RRR
![]() P
P![]() =
=