ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 06.07.2024
Просмотров: 123
Скачиваний: 0
СОДЕРЖАНИЕ
1.Классификация и номенклатура ферментов
4) Структура белковой молекулы
8)Биосинтез холерестерина и его биологическая роль.
10) .Роль желчных кислот, переваривание липидов
11) Характеристика гормонов поджелудочной железы
15) Характеристика витаминов(в2 и в5)
19)Ферменты биологического окисления
20)Взаимосвязь аминоуглеводов с обменом липидов
23) Факторы, влияющие на скорость ферментативных реакций
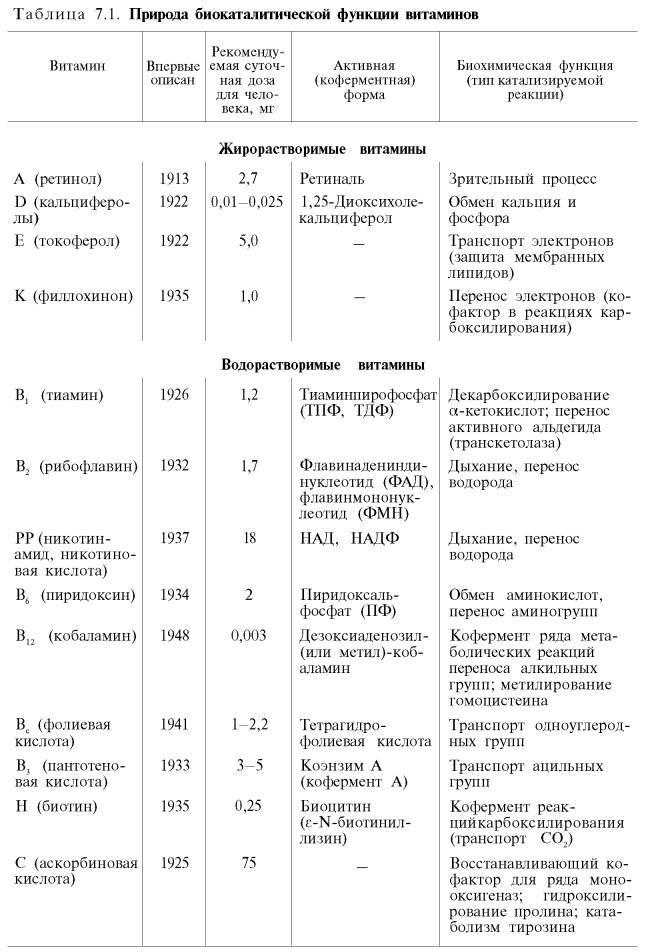
9)Классификация витаминов.
Витамины, растворимые в жирах
1. Витамин А (антиксерофтальмический); ретинол
2. Витамин D (антирахитический); кальциферолы
3. Витамин Е (антистерильный, витамин размножения); токоферолы
4. Витамин К (антигеморрагический); нафтохиноны
Витамины, растворимые в воде
1. Витамин B1(антиневритный); тиамин
2. Витамин В2 (витамин роста); рибофлавин
3. Витамин В6 (антидерматитный, адермин); пиридоксин
4. Витамин B12(антианемический); цианкобаламин; кобаламин
5. Витамин РР (антипеллагрический, ниацин); никотинамид
6. Витамин Вc (антианемический); фолиевая кислота
7. Витамин В3 (антидерматитный); пантотеновая кислота
8. Витамин Н (антисеборейный, фактор роста бактерий, дрожжей и грибков); биотин
9. Витамин С (антискорбутный); аскорбиновая кислота
10. Витамин Р (капилляроукрепляющий, витамин проницаемости); биофлаво-ноиды
Помимо этих двух главных групп витаминов, выделяют группу разнообразных химических веществ, из которых часть синтезируется в организме, но обладает витаминными свойствами. Для человека и ряда животных эти вещества принято объединять в группу витаминоподобных. К ним относят холин, липоевую кислоту, витаминВ15 (пангамовая кислота), оротовую кислоту, инозит, убихинон,парааминобензойную кислоту, кар-нитин, линолевую и линоленовую кислоты, витамин U (противоязвенный фактор) и ряд факторов роста птиц, крыс, цыплят, тканевых культур. Недавно открыт еще один фактор, названный пирролохинолинохиноном. Известны его коферментные и кофакторные свойства, однако пока не раскрыты витаминные свойства (см. далее «Витаминоподобные вещества»). Поскольку типичные проявления авитаминозов встречаются довольно редко, очевидно, нет необходимости в подробном описании клинической картины гипо- и авитаминозов. Более подробно будут представлены сведения о биологической роли тех витаминов, механизм действия которых уже расшифрован.
10) .Роль желчных кислот, переваривание липидов
В ротовой полости и желудке жиры не перевариваются, т.к там не вырабатываются ферменты гидролизующие жиры, нет условий для их эмульгирования .
Переваривание жиров происходит в тонком отделе кишечника под действием липазы, выделяемой поджелудочной железой. В самом начале, перед гидролизом пищ. жиры эмульгируются с помощью желчных кислот. Желудочные кислоты синтезируются в печени на основе холестерина, накапливаются в желудочном пузыре и далее вместе с желчью попадают в тонкий отдел кишечника. Желчные кислоты разбивают жир на мельчайшие капельки, собираются на их поверхности своей гидрофобной частью во внутрь, а гидрофильной снаружи и тем самым способствуют переносу жира в водную фазу с образованием устойчивой водно-жировой эмульсией . Т.к липаза гидролизующие жиры использует только в водной части, поэтому эмульгирование жира необходимо для того чтобы увеличивать площадь соприкосновения жира с липазой.
Желчные кислоты присутствуют в организме в виде натриевых солей парных желчных кислот, т.е они связаны с ам/к-ами глицином и таурином.
NH2-CH2-COOH-глицин
NH2-CH2-CH2-SO3H-таурин
Липаза выделяется поджелудочной железой в неактивной форме, активируется желчными кислотами.
11) Характеристика гормонов поджелудочной железы
Поджелудочная железа состоит из экзокринной и эндокринной (панкреатические островки или островки Лангерганса) частей, которые развиваются из энтодермы первичной кишки. В экзокринной части, которая составляет 98 % всей массы железы у человека, происходит выработка пищеварительного сока, который с пищей поступает в двенадцатиперстную кишку и содержит те ферменты, которые необходимы для расщепления белков, жиров и углеводов. В панкреатических островках происходит синтез гормонов, которые регулируют метаболические процессы, в частности углеводный обмен. Они распределены по всему телу поджелудочной железы и не имеют специальных выводных путей. Секрет этих клеток поступает непосредственно в кровь и доставляется ко всем органам-мишеням.
Основные гормоны поджелудочной железы:
инсулин;
глюкагон; с-пептид.
Бета-клетки, имеющиеся в панкреатических островках, отвечают за синтез инсулина. Инсулин представляет собой белковый гормон, имеющий молекулярную массу около 6000 Да. Состоит он из двух полипептидных цепей, которые соединены двумя дисульфидными мостиками. Инсулин образуется из своего предшественника - проинсулина, под влиянием протеаз. Активность проинсулина составляет 5 % активности инсулина. Преобразование проинсулина в инсулин происходит в тех же бета-клетках.
15) Характеристика витаминов(в2 и в5)
Витамин В2, (или же рибофлавин) является непосредственно предшественником некоторых коферментов, которые участвуют в окислительных процессах. Для взрослого человека суточная норма составляет около 0,03 мг на один килограмм массы тела.
Витамин В5 (или же пантотеновая кислота) прежде всего необходим для преобразования холина в ацетилхолин (главный медиатор нервной системы). Так же есть мнение, что витамин В5 способствует синтезу стероидных гормонов (а именно путем взаимодействия с разнообразными ферментами). Пантотеновая кислота входит в состав кофермента А, который занимает центральное место в метаболизме.
18)Окисление глицерина и бета-окисления жирных кислот(про жирные кислоты не нашла,только глицерин)
Окисление глицерина в тканях тесно связано с ГЛИКОЛИЗОМ, в который вовлекаются метаболиты обмена глицерина по следующей схеме:
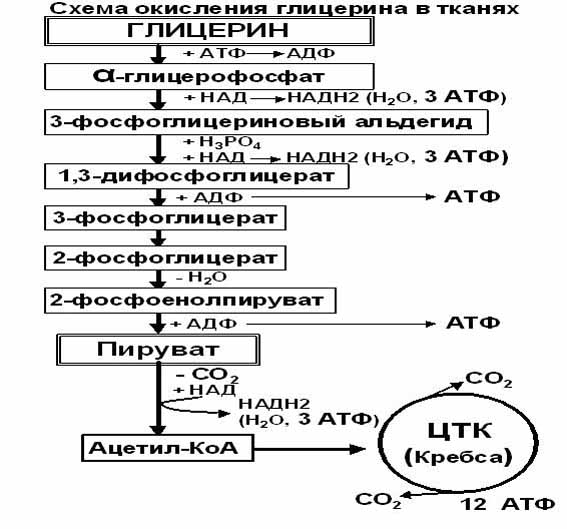
При окислении глицерина образовались конечные продукты:
СО2 на этапе превращения:
1. ПИРУВАТА
2. ИЗОЦИТРАТА
3. Альфа-КЕТОГЛУТАРАТА
Н2О на этапе превращения:
1 . альфа -ГЛИЦЕРОФОСФАТА
2. ГЛИЦЕРАЛЬДЕГИД-3-ФОСФАТА
3. 2-ФОСФОГЛИЦЕРАТА
4. ПИРУВАТА
5. ИЗОЦИТРАТА
6. Альфа-КЕТОГЛУТАРАТА
7. СУКЦИНАТА
8. МАЛАТА
АТФ выделилось за счёт реакций
А) Субстратного фосфорилиования на этапах превращения:
1. 1,3-дифосфоглицерата
2.2-фосфоенолпирувата
3.Сукцинил-КоА
19)Ферменты биологического окисления
Окисление биологическое,совокупность реакций окисления, протекающих во всех живых клетках. Основная функция О. б. — обеспечение организма энергией в доступной для использования форме. Реакции О. б. в клетках катализируют ферменты, объе-диняемые в класс оксидоредуктаз. О. б. в клетках связано с передачей т. н. восстанавливающих эквивалентов (ВЭ) — атомов водорода или электронов — от одного соединения — донора, к другому — акцептору. У аэробов — большинства животных, растений и многих микроорганизмов — конечным акцептором ВЭ служит кислород. Поставщиками ВЭ могут быть как органические, так и неорганические вещества (см. таблицу). Основной путь использования энергии, освобождающейся при О. б., — накопление её в молекулах аденозинтрифосфорной кислоты (АТФ) и др. макроэргических соединений.О. б., со-провождающееся синтезом АТФ из аденозиндифосфорной кислоты (АДФ) и неорганического фосфата, происходит при гликолизе, окислении a-кетоглутаровой кислоты и при переносе ВЭ в цепи окислительных (дыхательных) ферментов, обычно называют окислительным фосфорилированием (см. схему). В процессе дыхания углеводы, жиры и белки подвергаются многоступенчатому окислению, которое приводит к вос-становлению основных поставщиков ВЭ для дыхательных флави-нов, никотинамидадениндинуклеотида (НАД), никотинамидаде-ниндинуклеотидфосфата (НАДФ) и липоевой кислоты. Восстановление этих соединений в значительной мере осуществляется в трикарбоновых кислот цикле, которым завершаются основные пути окислительного расщепления углеводов (оно начинается с гликолиза), жиров и аминокислот. Помимо цикла трикарбоновых кислот, некоторое количество восстановленных коферментов — ФАД (флавинадениндинуклеотида) и НАД — образуется при окислении жирных кислот, а также при окислительном дезаминировании глутаминовой кислоты (НАД) и в пентозофосфатном цикле (восстановленный НАДФ). Одновременно развивалось направление, где в основу классификации ферментов был положен тип реакции, подвергающейся каталитическому воздейсвию. Наряду с ферментами, ускоряющими реакции гидролиза (гидролазы), были изучены ферменты, участвующие в реакциях переноса атомов и атомных групп (феразы), в изомеризации (изомеразы), расщеплении (лиазы), различных синтезах (синтетазы) и т. д. Это направление в классификации ферментов оказалось наибо-лее плодотворным, так как объе-диняло ферменты в группы не по надуманным, формальным признакам, а по типу важнейших биохимических процессов, лежащих в основе жизнедеятельности любого организма. По этому принципу все ферменты делят на 6 классов.1. Оксидоредуктазы — ускоряют реакции окисления — восстанов-ления. 2. Трансферазы — ускоряют реакции переноса функцио-нальных групп и молекулярных остатков. 3. Гидролазы — уско-ряют реакции гидролитического распада. 4. Лиазы — ускоряют негидролитическое отщепление от субстратов определенных групп атомов с образованием двойной связи (или присоединяют группы атомов по двойной связи). 5. Изомеразы — ускоряют пространственные или структурные перестройки в пределах одной молекулы. 6. Лигазы — ускоряют реакции синтеза, сопряженные с распадом богатых энергией связей.