ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 26.10.2023
Просмотров: 152
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Таутомерия. Восстанавливающие дисахариды способны к цикло-оксо-таутомерии во фрагменте, содержащем полуацетальную гидрокси-группу, а также легко окисляются под действием мягких окислителей, например, они дают реакцию «серебряного зеркала»:
Аналогичные превращения возможны для изомальтозы, лактозы и целлобиозы.
Гидролиз – разрушение гликозидной связи, с образованием смеси аномеров.
6 билет
Диссоциация воды. Ионное произведение воды. Водородный показатель (рН).
Вода – очень слабый электролит.Электролитическая диссоциация воды: 2H2O ⇌ H3O+(ион гидроксония) + OH-или в упрощенном виде: H2O ⇌ H+ + OH-
Соответственно, константа диссоциации (Kд) воды будет равна:
Kд =
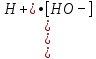 =1,8 * 10-16 (при t=25С)
=1,8 * 10-16 (при t=25С)Где [H+] – концентрация ионов водорода [г/моль], [OH-] – концентрация гидроксид-ионов [г/моль], [H2O] – концентрация воды [г/моль].
Концентрацию воды можно легко вычислить. Плотность воды p=1000г/л, соответственно, в 1л (V) воды 1000г.
n (H2O) = m/M (Н2О) =1000/ 18 = 55,6 моль
[H2O] = n/V = 55,6 / 1 = 55,6 моль/л
Ионное произведение воды – произведение концентраций [H+] и [HO-] при данной температуре – величина постоянная; при 25оС равна 10–14.
[H+] • [HO-] = Kд • [H2O] = 1,8•10-16 • 55,6 моль/л = 10-14 = KW
Величина Kw является константой для всех водных растворов при температуре 25С, при этом неважно какой раствор: 10% раствор NаС1, 0,1М раствор NаОН или раствор концентрированной желчи. Ионное произведение воды равно 10-14.
В растворе с нейтральной средой [H+] = [HO-], получается, что для чистой воды концентрации [H+] = [HO-] = 10-7 моль/л.
Водородный показатель (рН) – показатель кислотности раствора, который равен отрицательному десятичному логарифму концентрации ионов водорода в растворе.
pH = -lg[H+]
обозначение p (pKa, pH, pOH) всегда показывает, что от величины взяли отрицательный десятичный логарифм.
Н-р, надо найти pH в 0,1М растворе соляной кислоты, т.к. кислота сильная, следовательно, диссоциирует в растворе полностью:
[H+] = [HCl] → pH = -lg[HCl] = -lg0,1 = -lg10-1 = 1
В нейтральной среде pH = -lg[H+] = -lg 10-7 = 7
Обратная величина – показатель основности раствора pOH
pOH = -lg[OH-]
Если прологарифмировать ионное произведение воды (KW =10-14), то получим:
pH + pOH = pKw =14
pH = 14 – pOH
pOH = 14 – pH
Реакции нуклеофильного замещения. Моно- и бимолекулярные реакции, их стереохимическая направленность. Аллил- и бензилгалогениды
. Причины повышенной реакционной способности в реакциях нуклеофильного замещения. Винил - и арилгалогениды. Причина низкой подвижности галогена. Особенности реакционной способности.
Реакции нуклеофильного замещения SN – реакции с разрывом сигма-связи, где атакующая частица Nu. Чтобы сказать по какому механизму пойдет реакция моно- или бимолекулярному нужно оценить субстрат, реагент.
1. Оценить возможность образования стабильного карбокатиона (метилхлорид – не будет, а третбутилхлорид – будет).
Эта закономерность бимолекулярной реакции объясняется тем, что увеличение числа алкильных групп у С-атома не создает пространственных затруднений для атаки. В то же время алкильные заместители способствуют стабилизации «+» на углероде.
Аллил- и бензилгалогениды – образуют устойчивые карбокатионы за счет сопряжения р-орбитали sp2-гибридизованного С+ и р-орбиталей двойной связи или бензольного кольца. За счет этого положительный заряд делокализуется по молекуле и получается более устойчивый карбокатион. Из-за этого они обладают повышенной реакционной способностью в реакциях нуклеофильного замещения.
- если образуются карбокатион стабильный механизм SN1
Винил - и арилгалогениды – обладают пониженной реакционной способностью в реакциях нуклеофильного замещения, т.е. низкой подвижности галогена. А все из-за того, что галоген стоит у двойной связи и при попытке его заместить в реакциях нуклеофильного замещения, образующийся карбокатион будет иметь sp-гибридизацию. Такой карбокатион будет очень нестабильный из-за невозможности делокализации положительного заряда и ассиметрии в строении (все остальные в sp2, а он sp).
- если образуется карбокатион не стабильный механизм SN2
2. Также на реакционную способность будут влиять характер уходящей группы (нуклеофуга) и входящей (нуклеофила):
Для осуществления реакции SN необходимо, чтобы уходящая нуклеофильная группа (нуклеофуг) была стабильнее входящей.
Хорошими уходящими группами являются
: Cl-, Br-, I-, N≡N, группы, стабилизированные сопряжением -О– СН=СН, -О–С6Н5, −OSO2R. Эти группы уходят под натиском любых нуклеофилов и сильных оснований без использования каких-либо особых приемов.
Плохими уходящими группами являются: -ОН, -ОR, -NH2, -NHR, -NR2. Их удается вывести из субстратов только при использовании катализаторов (Н+, кислот Льюиса), которые превращают плохие уходящие группы в хорошие. SH, SR группы не удается вытеснить в обычных условиях из-за прочности связи C–S.
- если уходящая группа хорошая и стабильный карбокатион - SN1, плохая - SN2
Билет 16
Изотонические, гипертонические и гипотонические растворы. Тургор, плазмолиз, гемолиз. Закон Рауля и его следствия. Криоскопическая и эбуллиоскопическая константы.
Тоничность – мера градиента осмотического давления
| Раствор | Pосм |
| Оба раствора изотоничны по отношению друг к другу | Росм(А) = Росм(В) |
| Раствор А гипотонический по отношению к В | Росм(А) < Росм(В) |
| Раствор В гипертонический по отношению к А | Росм(А) > Росм(В) |
В медицине изотонические растворы – это растворы, осмотическое давление которых равно осмотическому давлению крови, н-р, 0,9% NaCl и 5% р-р глюкозы:
Росм (р-ра) = Росм (плазмы крови) = 740 – 780 кПа (при 370С).
Тургор – осмотическое давление воды в клетках, которое придает этим клеткам упругость и напряжение.
Плазмолиз эритроцитов – осмос воды из эритроцитов в окружающую плазму (экзоосмос). Это происходит если вводимый в вену раствор гипертоничен по отношению к плазме, в результате эритроциты обезвоживаются и сморщиваются:
Гемолиз эритроцитов - осмос воды внутрь эритроцитов (эндоосмос). Это происходит если вводимый в вену раствор гипотоничен по отношению к плазме. Эритроциты увеличиваются в объеме, что может привести к разрыву оболочки. В результате гемоглобин выходит в плазму.
Давление насыщенного пара растворителя над раствором при любой температуре будет ниже, чем над чистым растворителем.
Первый закон Рауля - относительное понижение давления насыщенного пара растворителя над раствором по сравнению с чистым растворителем при данной температуре равно мольной доле растворенного вещества:
 = iN(х)
= iN(х)Где Ро – давление насыщенного пара над чистым растворителем;
Р – давление насыщенного пара над раствором;
N(х) – мольная доля растворенного вещества x.
i – изотонический коэффициент (используется если раствор электролита)
Можно выразить P насыщенного пара растворителя над раствором: Р = Ро [1 - N(х)] = Р N(р-ля)