ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 06.11.2023
Просмотров: 232
Скачиваний: 4
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
или 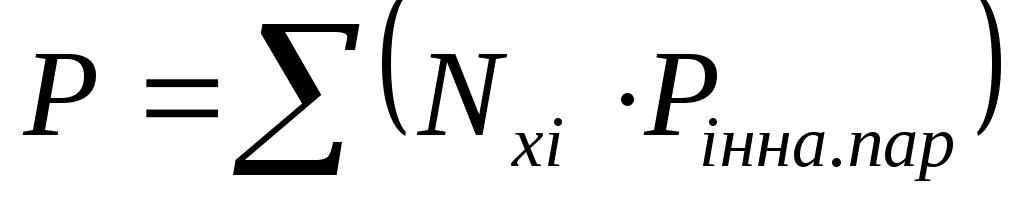 (4.5)
(4.5)
называется уравнением начала однократного (контактного) испарения. Оно характеризует давление, при котором кипит смесь при данной температуре. Температура учитывается в этом уравнении в неявном виде, так как упругости паров (давление насыщенных паров) компонентов зависят от температуры.
Уравнение:
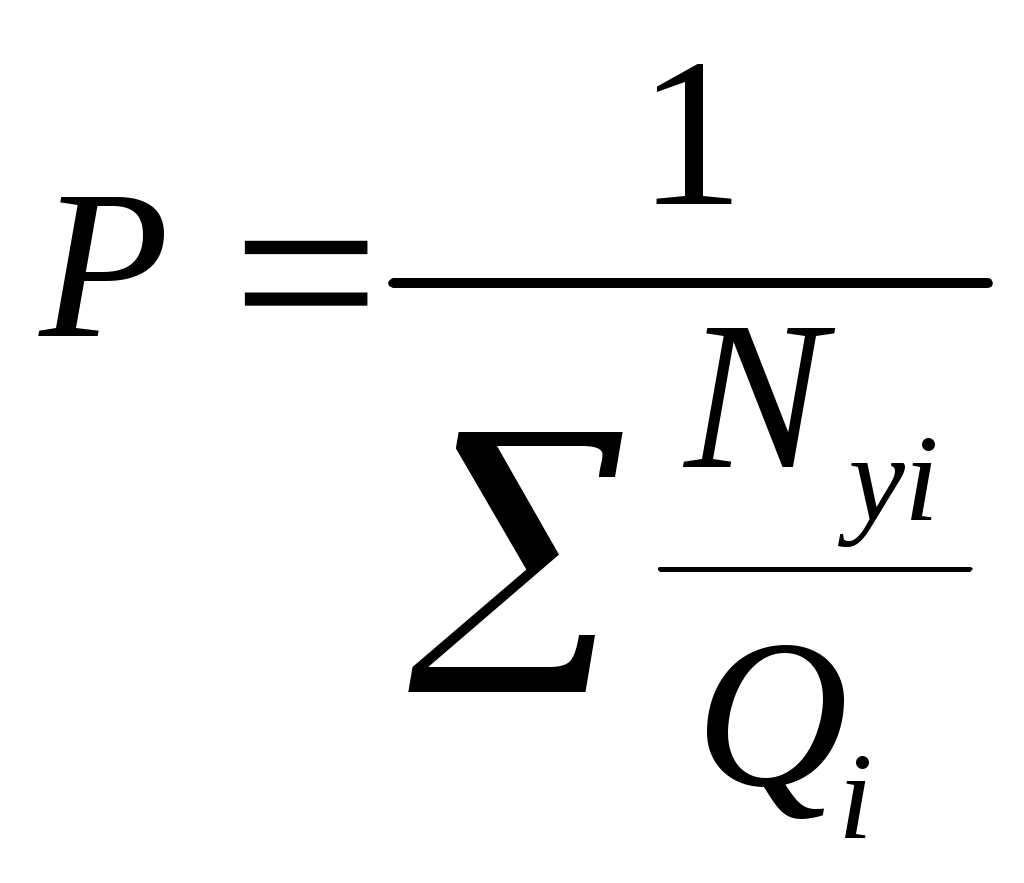 (4.6)
(4.6)
называется уравнением конца однократного испарения или уравнением начала однократной конденсации. Оно характеризует величину упругости паров (давления насыщенных паров) углеводородной смеси при данной температуре, при которой кипит смесь при данной температуре.
Уравнения равновесия (4.4), начала однократного испарения (4.5), начала конденсации (4.6) описывают поведение простых углеводородных смесей при низких давлениях и температурах. Для практических промысловых расчетов использовать их затруднительно, так как они не учитывают влияние давления и состава смеси на величину давления паров углеводородов, находящихся в смеси. Поэтому, для практических расчетов используют не упругости паров углеводородов (давления паров), взятые в чистом виде, а константы равновесия, характеризующие отношение:
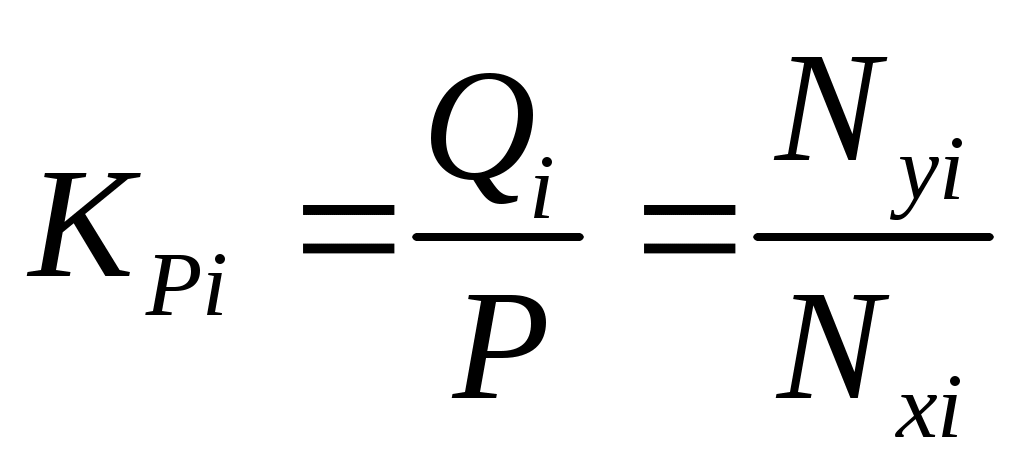 , (4.7)
, (4.7)
где Кi – константа равновесия i-го компонента при данной температуре и давлении смеси.
Оценить состав газовой (Nyi) и жидкой (Nxi) фаз можно на основе уравнения материального баланса, записанного для одного моля нефтегазовой смеси (Nzi):
 , (4.8)
, (4.8)
где L – мольная доля жидкой фазы;
V – мольная доля паровой фазы;
Nzi – мольные доли компонентов в нефтегазовой смеси.
Так как ∑ (Nzi) = 1, то сумма мольной доли жидкой фазы (L) и мольной доли паровой фазы (V) равна: V + L = 1. Отсюда следует:
V=1 – L. (4.9)
Используя уравнения (4.8) и (4.9) получим выражение для оценки мольной доли компонента жидкой фазы:
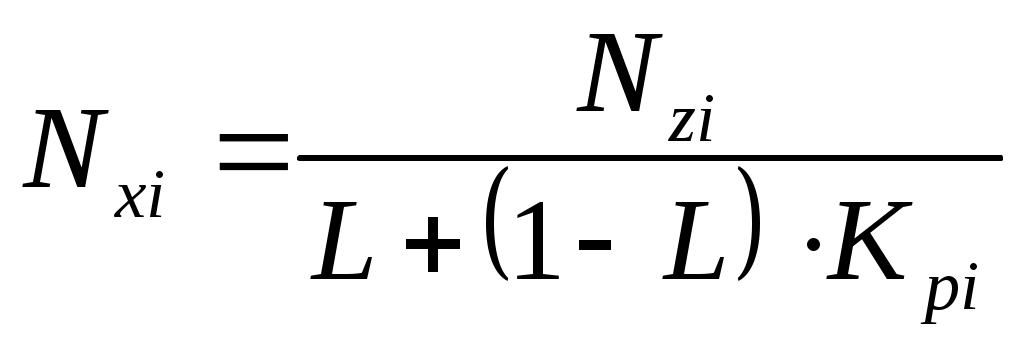 , (4.10)
, (4.10)
или
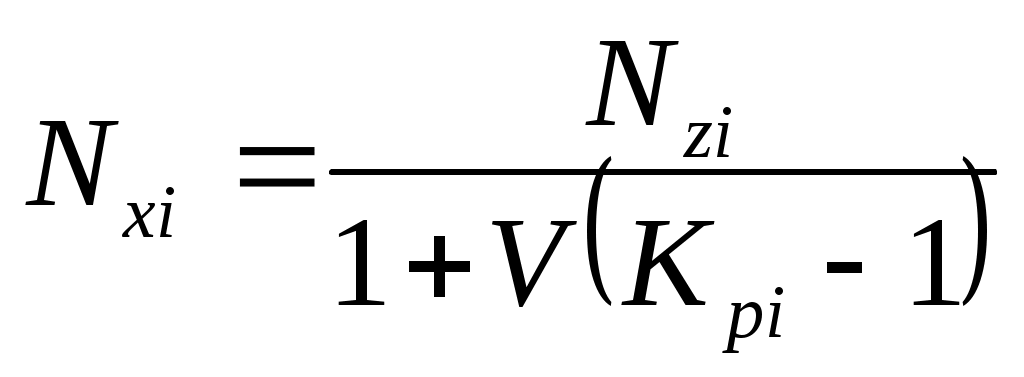 , (4.11)
, (4.11)
и для оценки мольной доли компонента газовой фазы:
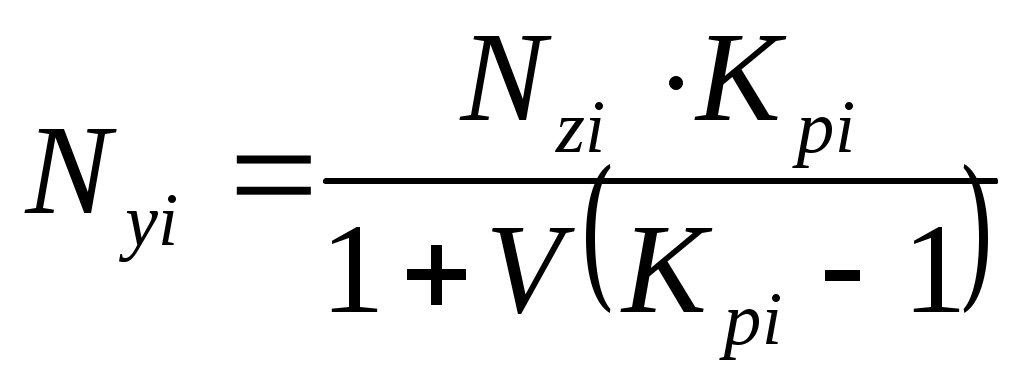
. (4.12)
Величины: V и L оцениваются и уточняются методом последовательных проб и приближений.
Уравнение (4.8) при наличии достоверных данных о константах фазовых равновесий углеводородов при различных условиях существования смесей имеет широкое прикладное значение в практике разработки месторождений, нефтедобычи, подготовки скважинной продукции и в нефтепереработке.
Вода в горных породах находится в сложном взаимодействии со скелетом, обменными ионами и растворенными веществами.
Основываясь на результатах экспериментальных работ, А.Ф.Лебедев разделил все формы влаги, исходя из главных принципов:
1) природы воздействующих на воду сил;
2) агрегатного состояния формы влаги: в форме пара; гигроскопическая вода; пленочная вода, удерживаемая силами молекулярного притяжения; гравитационная вода (капиллярная; подвешенная; собственно гравитационная); в твердом состоянии (в форме льда); кристаллизационная и химически связанная вода.
Недостатком этой схемы является проведение резких границ между отдельными категориями влаги и нехарактерное разграничение естественных форм влаги.
В более поздних классификациях были внесены коррективы в схему А.Ф. Лебедева.
П.А.Ребиндер указывает, что единственно надежным методом оценки форм связи воды с минеральными частицами является энергия связи.
Причины образования каждой из связей различны: для химической валентность; для физико-химической молекулярное силовое поле, осмотическое давление; для физико-механической капиллярное давление и поверхностное натяжение.
Парообразная вода в горной породе (количество влаги составляет 0,0015%) находится в динамическом равновесии с другими видами воды (в частности, с гигроскопической водой) и с парами воды в атмосфере. Фазовые превращения водяного пара ведут к образованию на поверхности частиц горной породы связанной воды: прочно и рыхлосвязанная (удерживается на поверхности частиц молекулярными силами).
Прочносвязанная вода имеет меньшую упругость пара, чем свободная вода, так как в ней ограничена свобода молекулярных движений. Диэлектрическая проницаемость прочносвязанной воды 22,2. Температура замерзания, по Боуюносу, равна 780С.
Максимальное количество прочносвязанной воды в породах соответствует величине максимальной гигроскопичности.
Рыхлосвязанная вода представляет собой слои влаги, окружающие прочносвязанную воду. По своим свойствам она мало отличается от свободной воды: имеет плотность близкую к плотности свободной воды и температуру замерзания 1,5 градусов Цельсия. Рыхлосвязанная вода имеет
меньший уровень энергетической связи, чем прочносвязанная вода.
Образование рыхлосвязанной воды происходит в диффузионном слое ионов, с помощью которого непосредственно связано ее количество. Суммарное содержание прочносвязанной и ориентированной воды полислоев составляет влажность, которая была названа А.Ф. Лебедевым - максимальной молекулярной влагоемкостью, величина которой определяется теми же факторами, что и величина максимальной гигроскопичности породы. Количество рыхлосвязанной воды может в 2 4 раза превышать величину максимальной гигроскопичности.
Капиллярная вода подразделяется на три вида: вода углов пор, подвешенная вода, собственно капиллярная вода. Заполнение пор водой определяется составом и структурой породы. Капиллярная вода, подобно гравитационной, передает гидростатическое давление.
Свободная вода перемещается в порах и пустотах горных пород под действием силы тяжести. Она заполняет трещины, пустоты, крупные поры. Максимально возможное содержание в породе связанной, капиллярной и гравитационной воды при полном заполнении пор называют полной влагоемкостью.
Вода в твердом состоянии (кристаллизационная, химически связанная вода и вода в состоянии льда) детально изучается в минералогии и мерзлотоведении и представляет собой особые формы структуры воды, в которых преобладают молекулярные и ионные связи. Данный вид воды обладает свойствами твердого тела.
Плотность пластовых водвозрастает с увеличением концентрации солей, и в связи с широким изменением минерализации плотность вод может быть различной. Известны рассолы, насыщающие породы, плотность которых достигает 1450 кг/м3 при концентрации солей 642,8 кг/м3.
Тепловое расширение воды характеризуют коэффициентом теплового расширения:
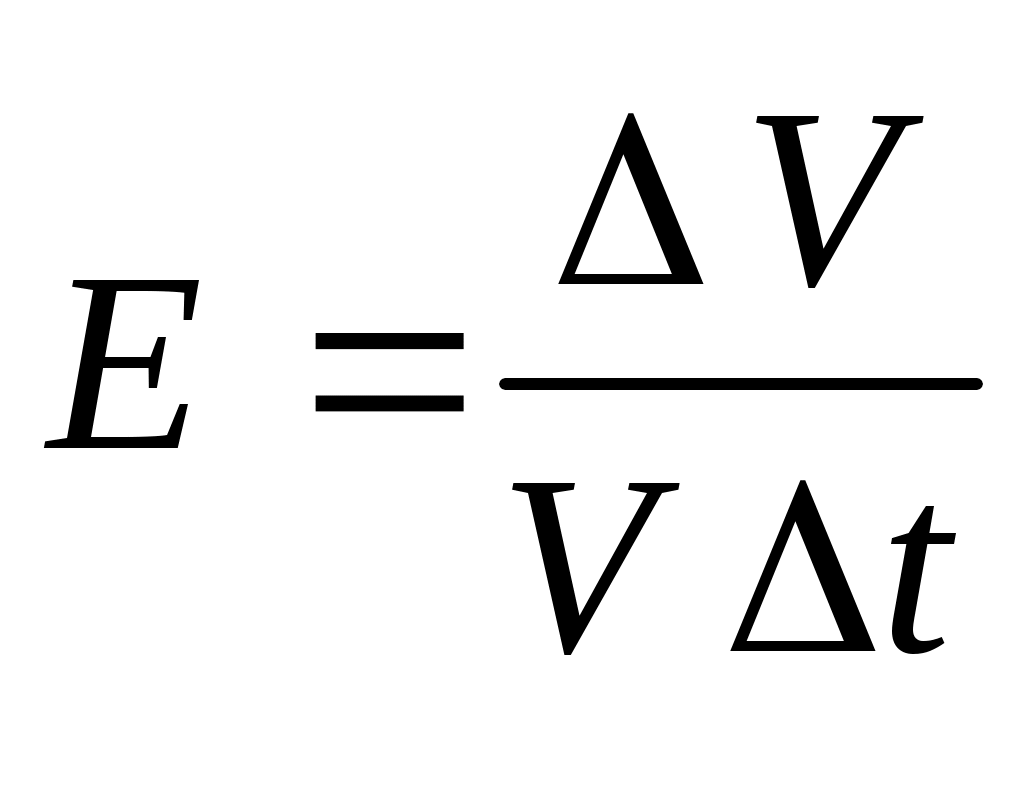 (5.1)
(5.1)
где V изменение объема воды при изменении температуры на t; V – объем воды в нормальных условиях.
Из формулы (5.1) следует, что коэффициент теплового расширения Е воды характеризует изменение единицы объема воды при изменении ее температуры на 10. По экспериментальным данным в пластовых условиях он колеблется в пределах от 18 . 10-5 до 90 . 10-5 1/град, возрастая с увеличением температуры и уменьшаясь с ростом пластового давления.
Сжимаемость пластовой воды. Коэффициент сжимаемости воды:
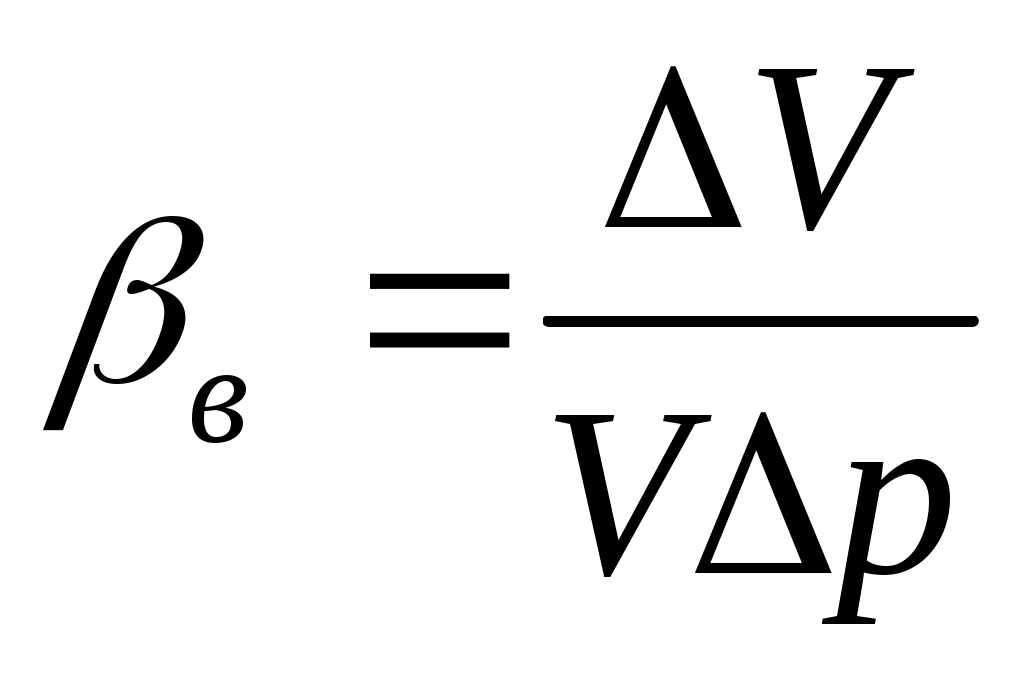 (5.2)
(5.2)
характеризует изменение единицы объема воды при изменении давления на единицу.
Коэффициент сжимаемости воды изменяется в пластовых условиях в пределах (3,7-5,0) 10-10 м2/н. При наличии растворенного газа коэффициент сжимаемости воды увеличивается и может быть приближенно определен по формуле:
вг = в (1 + 0,05 S) (5.3)
в (1 + 0,05 S) (5.3)
где вг – коэффициент сжимаемости воды, содержащий растворенный газ, в м2/н; в – коэффициент сжимаемости чистой воды в м2/н; S – количество газа, растворенного в воде, в м3/м3.
Объемный коэффициент пластовой воды характеризует отношение удельного объема воды в пластовых условиях Vпу к удельному объему ее в стандартных условиях Vн:
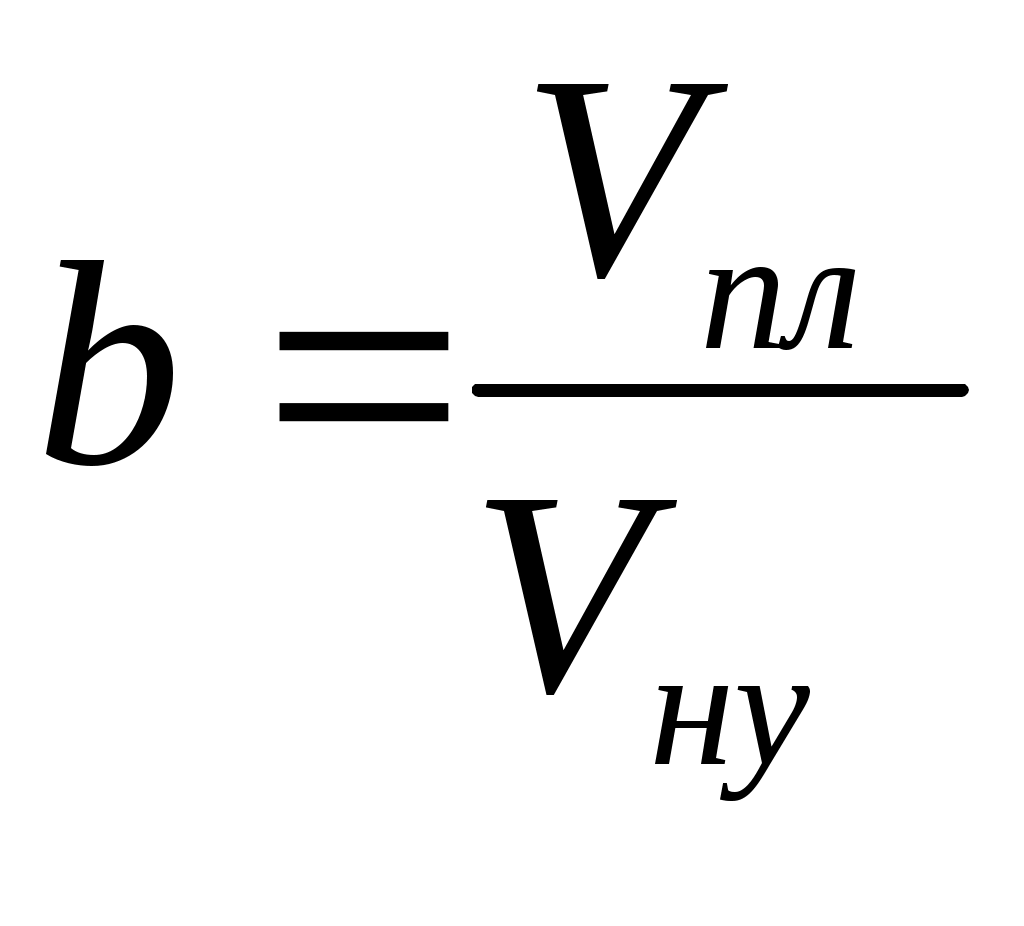 (5.4)
(5.4)
Увеличение пластового давления способствует уменьшению объемного коэффициента, а рост температуры сопровождается его повышением. Поэтому объемный коэффициент воды изменяется в сравнительно узких пределах (0,99-1,06). Правый предел относится к высокой температуре (1210С) и низкому давлению, левый – к низкой температуре (380С) и высокому давлению (32 Мн/м2).
Растворимость углеводородных газов в воде. Растворимость газов в водах возрастает с увеличением давления и уменьшается с ростом температуры. С повышением минерализации ухудшается растворимость газов в воде. Растворимость газа в воде в зависимости от ее минерализации определяют по формуле :
пл = пр (1 – k М), (5.5)
где М – минерализация в кмоль/м3
называется уравнением начала однократного (контактного) испарения. Оно характеризует давление, при котором кипит смесь при данной температуре. Температура учитывается в этом уравнении в неявном виде, так как упругости паров (давление насыщенных паров) компонентов зависят от температуры.
Уравнение:
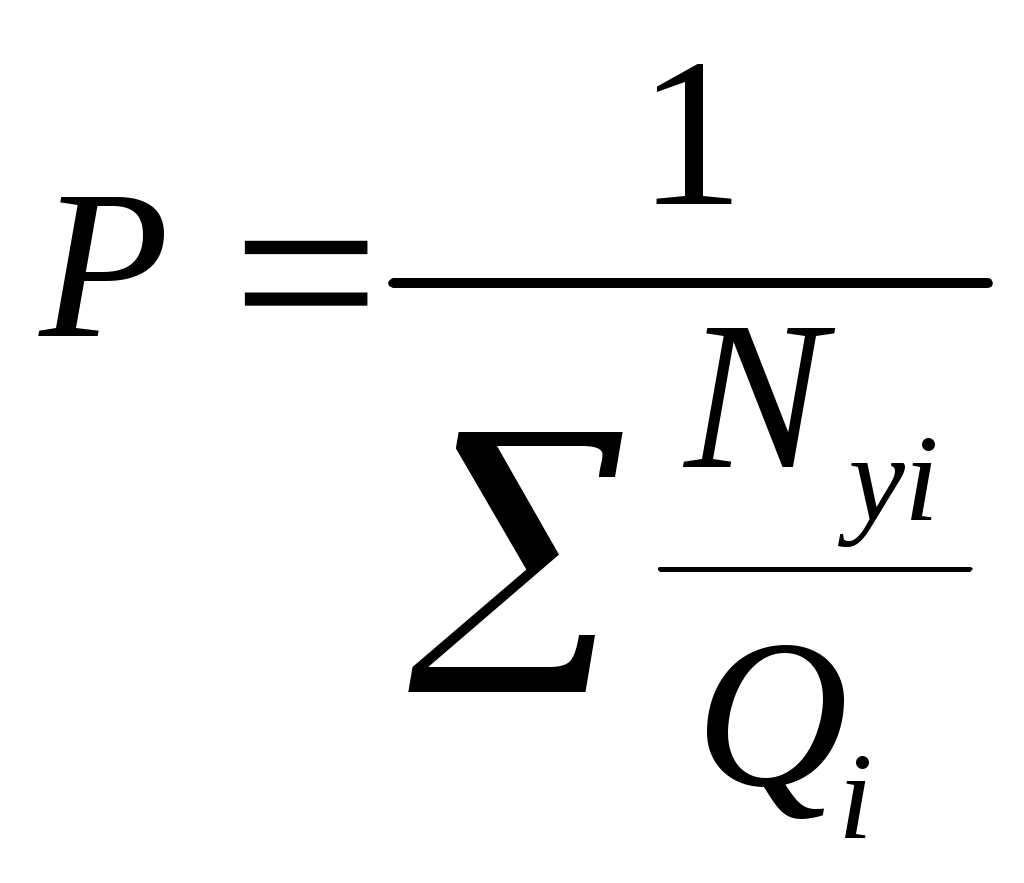 (4.6)
(4.6) называется уравнением конца однократного испарения или уравнением начала однократной конденсации. Оно характеризует величину упругости паров (давления насыщенных паров) углеводородной смеси при данной температуре, при которой кипит смесь при данной температуре.
Уравнения равновесия (4.4), начала однократного испарения (4.5), начала конденсации (4.6) описывают поведение простых углеводородных смесей при низких давлениях и температурах. Для практических промысловых расчетов использовать их затруднительно, так как они не учитывают влияние давления и состава смеси на величину давления паров углеводородов, находящихся в смеси. Поэтому, для практических расчетов используют не упругости паров углеводородов (давления паров), взятые в чистом виде, а константы равновесия, характеризующие отношение:
где Кi – константа равновесия i-го компонента при данной температуре и давлении смеси.
Оценить состав газовой (Nyi) и жидкой (Nxi) фаз можно на основе уравнения материального баланса, записанного для одного моля нефтегазовой смеси (Nzi):
где L – мольная доля жидкой фазы;
V – мольная доля паровой фазы;
Nzi – мольные доли компонентов в нефтегазовой смеси.
Так как ∑ (Nzi) = 1, то сумма мольной доли жидкой фазы (L) и мольной доли паровой фазы (V) равна: V + L = 1. Отсюда следует:
V=1 – L. (4.9)
Используя уравнения (4.8) и (4.9) получим выражение для оценки мольной доли компонента жидкой фазы:
или
и для оценки мольной доли компонента газовой фазы:
. (4.12)
Величины: V и L оцениваются и уточняются методом последовательных проб и приближений.
Уравнение (4.8) при наличии достоверных данных о константах фазовых равновесий углеводородов при различных условиях существования смесей имеет широкое прикладное значение в практике разработки месторождений, нефтедобычи, подготовки скважинной продукции и в нефтепереработке.
5 ПЛАСТОВЫЕ ВОДЫ
5.1. Физическое состояние воды в горных породах
Вода в горных породах находится в сложном взаимодействии со скелетом, обменными ионами и растворенными веществами.
Основываясь на результатах экспериментальных работ, А.Ф.Лебедев разделил все формы влаги, исходя из главных принципов:
1) природы воздействующих на воду сил;
2) агрегатного состояния формы влаги: в форме пара; гигроскопическая вода; пленочная вода, удерживаемая силами молекулярного притяжения; гравитационная вода (капиллярная; подвешенная; собственно гравитационная); в твердом состоянии (в форме льда); кристаллизационная и химически связанная вода.
Недостатком этой схемы является проведение резких границ между отдельными категориями влаги и нехарактерное разграничение естественных форм влаги.
В более поздних классификациях были внесены коррективы в схему А.Ф. Лебедева.
П.А.Ребиндер указывает, что единственно надежным методом оценки форм связи воды с минеральными частицами является энергия связи.
Причины образования каждой из связей различны: для химической валентность; для физико-химической молекулярное силовое поле, осмотическое давление; для физико-механической капиллярное давление и поверхностное натяжение.
Парообразная вода в горной породе (количество влаги составляет 0,0015%) находится в динамическом равновесии с другими видами воды (в частности, с гигроскопической водой) и с парами воды в атмосфере. Фазовые превращения водяного пара ведут к образованию на поверхности частиц горной породы связанной воды: прочно и рыхлосвязанная (удерживается на поверхности частиц молекулярными силами).
Прочносвязанная вода имеет меньшую упругость пара, чем свободная вода, так как в ней ограничена свобода молекулярных движений. Диэлектрическая проницаемость прочносвязанной воды 22,2. Температура замерзания, по Боуюносу, равна 780С.
Максимальное количество прочносвязанной воды в породах соответствует величине максимальной гигроскопичности.
Рыхлосвязанная вода представляет собой слои влаги, окружающие прочносвязанную воду. По своим свойствам она мало отличается от свободной воды: имеет плотность близкую к плотности свободной воды и температуру замерзания 1,5 градусов Цельсия. Рыхлосвязанная вода имеет
меньший уровень энергетической связи, чем прочносвязанная вода.
Образование рыхлосвязанной воды происходит в диффузионном слое ионов, с помощью которого непосредственно связано ее количество. Суммарное содержание прочносвязанной и ориентированной воды полислоев составляет влажность, которая была названа А.Ф. Лебедевым - максимальной молекулярной влагоемкостью, величина которой определяется теми же факторами, что и величина максимальной гигроскопичности породы. Количество рыхлосвязанной воды может в 2 4 раза превышать величину максимальной гигроскопичности.
Капиллярная вода подразделяется на три вида: вода углов пор, подвешенная вода, собственно капиллярная вода. Заполнение пор водой определяется составом и структурой породы. Капиллярная вода, подобно гравитационной, передает гидростатическое давление.
Свободная вода перемещается в порах и пустотах горных пород под действием силы тяжести. Она заполняет трещины, пустоты, крупные поры. Максимально возможное содержание в породе связанной, капиллярной и гравитационной воды при полном заполнении пор называют полной влагоемкостью.
Вода в твердом состоянии (кристаллизационная, химически связанная вода и вода в состоянии льда) детально изучается в минералогии и мерзлотоведении и представляет собой особые формы структуры воды, в которых преобладают молекулярные и ионные связи. Данный вид воды обладает свойствами твердого тела.
5.2 Физические свойства пластовых вод
Плотность пластовых водвозрастает с увеличением концентрации солей, и в связи с широким изменением минерализации плотность вод может быть различной. Известны рассолы, насыщающие породы, плотность которых достигает 1450 кг/м3 при концентрации солей 642,8 кг/м3.
Тепловое расширение воды характеризуют коэффициентом теплового расширения:
где V изменение объема воды при изменении температуры на t; V – объем воды в нормальных условиях.
Из формулы (5.1) следует, что коэффициент теплового расширения Е воды характеризует изменение единицы объема воды при изменении ее температуры на 10. По экспериментальным данным в пластовых условиях он колеблется в пределах от 18 . 10-5 до 90 . 10-5 1/град, возрастая с увеличением температуры и уменьшаясь с ростом пластового давления.
Сжимаемость пластовой воды. Коэффициент сжимаемости воды:
характеризует изменение единицы объема воды при изменении давления на единицу.
Коэффициент сжимаемости воды изменяется в пластовых условиях в пределах (3,7-5,0) 10-10 м2/н. При наличии растворенного газа коэффициент сжимаемости воды увеличивается и может быть приближенно определен по формуле:
вг =
где вг – коэффициент сжимаемости воды, содержащий растворенный газ, в м2/н; в – коэффициент сжимаемости чистой воды в м2/н; S – количество газа, растворенного в воде, в м3/м3.
Объемный коэффициент пластовой воды характеризует отношение удельного объема воды в пластовых условиях Vпу к удельному объему ее в стандартных условиях Vн:
Увеличение пластового давления способствует уменьшению объемного коэффициента, а рост температуры сопровождается его повышением. Поэтому объемный коэффициент воды изменяется в сравнительно узких пределах (0,99-1,06). Правый предел относится к высокой температуре (1210С) и низкому давлению, левый – к низкой температуре (380С) и высокому давлению (32 Мн/м2).
Растворимость углеводородных газов в воде. Растворимость газов в водах возрастает с увеличением давления и уменьшается с ростом температуры. С повышением минерализации ухудшается растворимость газов в воде. Растворимость газа в воде в зависимости от ее минерализации определяют по формуле :
пл = пр (1 – k М), (5.5)
где М – минерализация в кмоль/м3