ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 03.12.2023
Просмотров: 149
Скачиваний: 2
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
СОДЕРЖАНИЕ
Описание для кривой охлаждения II. Отличие кристаллизации этого сплава от кристаллизации сплава I состоит в том, что при перитектической температуре имеется избыток жидкой фазы по сравнению с тем количеством, которое необходимо для образования α-кристаллов концентрации Р. Поэтому перитектическое превращение заканчивается исчерпанием β-твердого раствора, и оставшаяся жидкость в интервале между точками 2'— 3 кристаллизуется в α-фазу. При этом концентрация жидкости изменяется по кривой С—а, а концентрация образующихся α-кристаллов — по Ρ — 3 .
-
Диаграмма состояния сплава с отсутствием растворимости в твердом состоянии и наличием эвтектического превращения
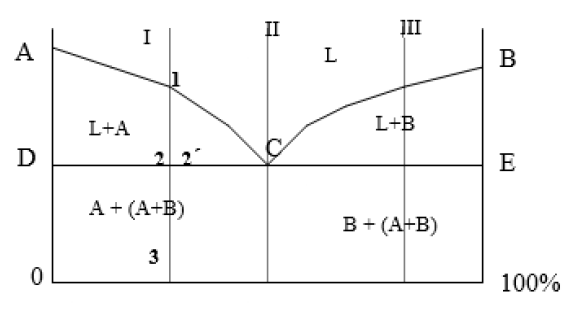
Рисунок 14. Диаграмма состояния сплава с отсутствием растворимости в твердом состоянии и наличием эвтектического превращения
Компоненты: A, B. Фазы: жидкий раствор L, кристаллы A и кристаллы B (максимальное значение фаз – 3).
АСВ – ликвидус. DСЕ – солидус. При охлаждении по АС начинают выделяться кристаллы А, по СВ – кристаллы В. На линии DСЕ из жидкости концентрации С одновременно выделяются кристаллы А и В, образуя эвтектику. DСЕ – линия эвтектических превращений.
Ниже линии АС область двухфазная. Здесь существуют одновременно жидкий раствор L и твердая фаза – кристаллы А.
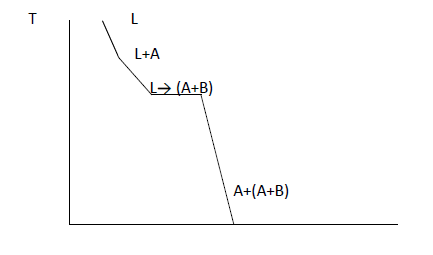
Рисунок 15. Кривая охлаждения
Описание кривой охлаждения: в точке 1 – начало кристаллизации сплава I. На кривой охлаждения наблюдается перегиб. В процессе кристаллизации состав жидкости будет меняться по линии АС. В точке 2 жидкость будет иметь концентрацию точки С. При этой температуре из жидкости одновременно выделяются кристаллы А и В, образуя механическую смесь – эвтектику (А+В), т.е. образуются двухфазные кристаллы. Этот процесс изотермический и происходит по линии DСЕ, которая называется линией эвтектических превращений. С – тройная точка: при данной температуре и данном составе в системе существует 3 фазы: L, А, В.
Сплав 1 – доэвтектический. Структура: А + эвтектика (А+В)
Сплав 2 – эвтектический. Структура: эвтектика (А+В)
Сплав 3 – заэвтектический. Структура В + эвтектика (А + В).
-
Диаграмма состояния для сплавов с промежуточной фазой
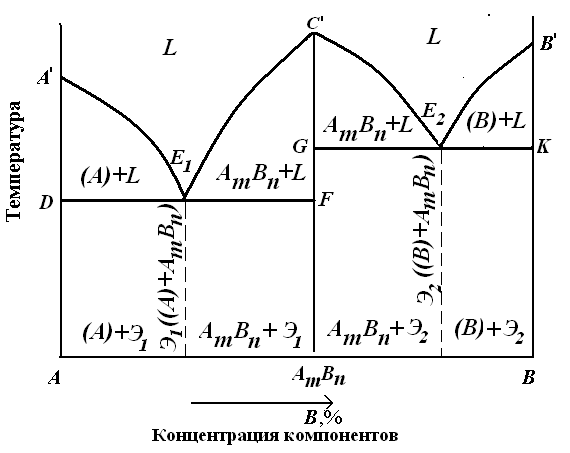
Рисунок 16. Диаграмма состояния сплава с промежуточной фазы
Компоненты: A, B. Фазы: жидкая фаза L, кристаллы A, кристаллы B, кристаллы AmBn.
Точки: А′ – температура плавления и кристаллизации компонента А; В′ – температура плавления и кристаллизации компонента В; С′ – температура плавления и кристаллизации химического соединения АmBn ; Е1 и Е2– точки эвтектики.
Линии: А′Е1С′Е2В′ – ликвидус; А′D Е1F и G Е2K В′ – солидус (не касается осей температур и разрывается на ординате химического соединения). Линии DЕ1F и GЕ2K в то же время являются и эвтектическими линиями.
Эвтектические равновесия для даннойсистемы представляет собой равновесие жидкости эвтектического состава LE1 с кристаллами (А) и АmBn при температуре t E1:
LE1
и равновесие жидкости эвтектического состава LE2 с кристаллами (В) и АmBn при температуре t E2:
LE2
-
Диаграмма состояния сплавов с полиморфным превращением компонентов и эвтектоидным превращением
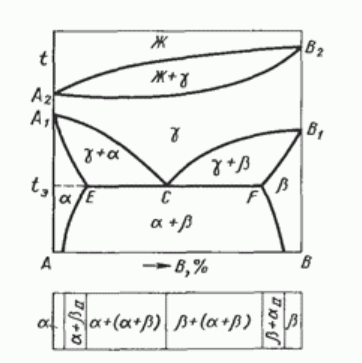
Рисунок 17. Диаграмма состояния сплавов с полиморфным превращениями компонентов и эвтектоидным превращением
Из анализа диаграммы, представленной на рисунке 17, можно заключить, что после кристаллизации всех сплавов данной системы в определенном интервале температур образуется твердый раствор
 , который при понижении температуры ниже tЭ, испытывает эвтектоидное превращение:
, который при понижении температуры ниже tЭ, испытывает эвтектоидное превращение: 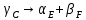
. Образовавшуюся смесь двух твердых фаз принято называть эвтектоидом. В связи с переменной растворимостью компонентов в твердых растворах α и β при дальнейшем охлаждении следуют вторичные выделения твердых растворов. Наблюдаемые в микроскоп вторичные выделения
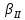 и
и 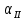 показаны на структурной схеме сплавов, приведенной под диаграммой на рисунке 17.
показаны на структурной схеме сплавов, приведенной под диаграммой на рисунке 17. Правило отрезков. Пользуясь диаграммой состояния, можно для любой температуры определить не только число фаз, но и их состав, а также количественное соотношение по правилу отрезков. Применять его можно для двухфазных областей диаграмм.
-
Определение состава фаз
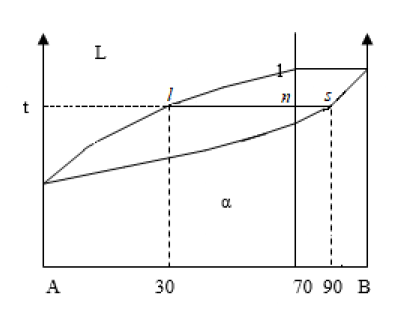
Предположим, что нам нужно определить состав фаз при разных температурах для сплава 1 (сплошная вертикальная линия), который при комнатной температуре состоит из 70% В и 30% А, на пример в точке n. Проведем через точку n – горизонтальную линию –коноду, до пересечения с линиями диаграммы. Точки пересечения l и s проектируем на ось концентраций. Проекция точки l – покажет состав жидкой фазы, проекция т. s – состав твердой фазы. В данном случае при температуре t – состав жидкой фазы: 30% В и 70% А, состав твердой фазы: 90% В, 10% А.
-
Определение количественного соотношения фаз
Для определения количественного соотношения фаз, так же проводят коноду. Правило: количество (масса) фаз обратно пропорционально отрезкам проведенной коноды. Если принять, что отрезок ls – количество всего сплава, то отрезок ln соответствует количеству выпавших кристаллов α, а ns – количеству жидкой фазы. Для определения относительного количества фаз пользуются отношениями:
Ж/С = ns/ ls
Т/С= ln/ ls
где Ж – количество жидкой фазы, С - количество всего сплава, Т – количество твердой фазы.
Если массу всего сплава (C) принять за 100%, то получим:
Ж = ns/ ls · 100%
Т = ln/ ls · 100%
Из диаграммы находим: ls = 60 единиц, ln = 40 ед., ns = 20 ед.
Ж = 20/60 * 100% = 33%
Т = 40/60 ·100% = 67%
Вопрос 5.
Особенности процесса затвердевания в неравновесных условиях. Ликвация в сплавах. Внутрикристаллическая ликвация (ВКЛ). Коэффициент ликвации. Влияние ликвации на структуру и свойства. Факторы, влияющие на развитие ВКЛ. Ее устранение путем термической обработки. Зональная ликвация, прямая и обратная. Ликвация по удельному весу и вследствие расслоения. Меры борьбы.
Диаграмма состояния характеризует равновесное состояние сплава, т.е. они описывают структуры сплавов и процессы превращения в сплавах в условиях очень малых скоростей нагревания и охлаждения, при которых успевает пройти диффузия, позволяющая выровнять переменный состав кристаллов твердой фазы, обусловленный различием в температурах затвердевания.
В реальных условиях нагрева и охлаждения диффузия проходить не успевает. В этом случае структура сплавов будет отличаться от равновесной, а состав в пределах каждого кристалла и тем более в разных кристаллах будет различаться и тем сильнее, чем более значительно реальные условия нагрева и охлаждения отличаются от равновесного состояния. На диаграммах состояния это обстоятельство находит отражение в появлении дополнительных линий, характеризующих неравновесные условия кристаллизации.
В условиях неравновесной кристаллизации сплавы затвердевают ниже равновесной температуры затвердевания.
Ликвация – это химическая неоднородность, возникающая в сплаве в процессе (неравновесной) кристаллизации. Ликвация, проявляющаяся в объеме отдельных зерен (кристаллитов, дендритов), называется внутрикристаллической (ВКЛ) или дендритной ликвацией. Если химическая неоднородность наблюдается в объеме всего слитка или отливки, то такая ликвация называется зональной ликвацией.
Ликвация любого вида является нежелательным процессом, т. к. ухудшает многие свойства (механические, коррозионную стойкость и др.) сплава как в состоянии полуфабриката, так и в готовом изделии.
- 1 2 3 4 5 6 7
Внутрикристаллическая ликвация (ВКЛ)
Внутрикристаллическая или дендритная ликвация (ВКЛ) – ликвация, проявляющаяся в объеме отдельных зерен. Этот вид ликвации обнаруживается в зернах кристаллических фаз переменного состава, т. е. в зернах твердых растворов. Известно, что такие фазы являются наиболее распространенными во многих важных в технике сплавах.
Сплав с внутрикристаллической ликвацией имеет пониженную пластичность и низкую стойкость против коррозии. Микроучастки сплава разного состава при обработке давлением в горячем состоянии (прокатка, прессование и др.) располагаются слоями, отчего возникает строчечная структура, обладающая, как известно, заметной анизотропией свойств.
Факторы, влияющие на возникновение ВКЛ:
-
внутрикристаллическая ликвация будет проявляться тем сильнее, чем больше различаются химические составы жидкой и твердой фаз, т.е. чем больше расстояние до горизонтали между линиями ликвидуса и солидуса диаграммы состояния системы;
-
на степень развития ВКЛ сильно влияет скорость охлаждения. Увеличение скорости охлаждения замедляет диффузионные процессы, следовательно, чем быстрее охлаждается сплав, тем более развита в нем ВКЛ. Однако замечено, что в некоторых сплавах при очень высоких скоростях охлаждения внутрикристаллическая ликвация ослабляется. Это явление объясняется тем, что в этих условиях диффузионный (избирательный) механизм кристаллизации постепенно заменяется бездиффузионным, когда растущие кристаллы присоединяют к себе все атомы компонентов из жидкой фазы, окружающей кристалл. Тогда химический состав кристаллов по всему своему объему оказывается равным химическому составу жидкой фазы и, следовательно, ликвация отсутствует;
-
необходимое условие возникновение ВКЛ – кристаллизация сплава в интервале температур: чем шире в жидкой и твердой фазах.
Для количественной оценки степени ВКЛ и, следовательно, химической неоднородности, возникающей при этом, используют коэффициент ликвации KЛ, численно равный отношению максимальной концентрации растворенного элемента к его минимальной концентрации. Однако с помощью этого коэффициента можно оценить только относительную ширину интервала колебаний концентрации.
Для уменьшения ВКЛ сплавы в виде слитков или отливок подвергают диффузионному отжигу (гомогенизации). Металл нагревают до высокой температуры, при этом не допуская оплавления, и выдерживают длительное время. При этом в неоднородных по химическому составу зернах твердого раствора дополнительно развиваются процессы диффузии, в результате чего выравнивается их химический состав.
-
Зональная ликвация
Зональная ликвация – явление, когда химическая неоднородность наблюдается в объеме всего слитка или отливки. Зональная ликвация встречается в различных формах.
-
Ликвация по поперечному сечению слитка.
Чаще всего она проявляется в том, что наружные слои слитка по сравнению с центральной зоной обогащены компонентом, повышающим температуру кристаллизации сплава. Такая зональная ликвация называется прямой. Установлено, что в крупных слитках, охлаждающихся медленно, прямая зональная ликвация развита сильнее, чем в слитках малого сечения, которые охлаждаются быстрее.
Значительно реже встречается обратная ликвация, когда наружные слои слитка обогащены компонентом, понижающим температуру сплава.
Прямая и обратная зональные ликвации не уничтожаются ни диффузионным отжигом, ни горячей пластической деформацией. Для уменьшения развития зональной ликвации по поперечному сечению слитка применяются специальные меры по созданию нужной формы слитка и условий их охлаждения.
-
Ликвация по высоте слитка.
Этот вид ликвации проявляется в том, что средний химический состав верха слитка отличается от состава низа слитка, что обусловлено различием в структуре верхних и нижних частей слитка. Такая ликвация обычно встречается в сплавах, кристаллизующихся как смеси различных фаз при условии заметной разницы в величине удельного веса у компонентов, и называется ликвацией по удельному весу. В этих сплавах при медленном их охлаждении при кристаллизации создаются условия, когда тяжелые кристаллические образования опускаются к низу слитка, а более легкие – всплывают к верху слитка.
Для предотвращения образования ликвации по удельному весу сплавы следует охлаждать быстро, поскольку данный тип ликвации будет развит тем сильнее, чем медленнее охлаждается сплав. Тем не менее, в случае кристаллизации больших масс сплава практически сделать это трудно. Тогда в целях предотвращения возникновения данного типа ликвации вводят третий компонент в сплав с таким расчетом, чтобы это добавка образовывала с одним из основных компонентов химическое соединение. Будучи более тугоплавким, оно начнет при охлаждении сплава выделяться в первую очередь и своими тонкими, сильно разветвленными осями дендритов воспрепятствует разделению структурных элементов сплава по высоте слитка.
Разновидностью ликвации по удельному весу является расслоение жидкой фазы на две различных по составу жидкости с последующим возникновением различной структуры. Расслоение наблюдается в сплавах с ограниченной растворимостью компонентов в жидком состоянии.
Для предотвращения явления расслоения применяют высокий нагрев сплава для однофазного жидкого состояния и последующее быстрое охлаждение, тщательное перемешивание и встряхивание.
Вопрос 6. Диаграммы состояния системы железо-углерод. Полиморфные превращения в железе. Метастабильная диаграмма состояния системы железо-цементит. Доэвтектоидные и заэвтектоидные стали. Белые доэвтектические и заэвтектические чугуны. Структурные составляющие сталей и белых чугунов, их характеристика и свойства. Стабильная диаграмма системы железо-графит. Фазовые превращения в сталях и чугунах при нагреве и охлаждении.
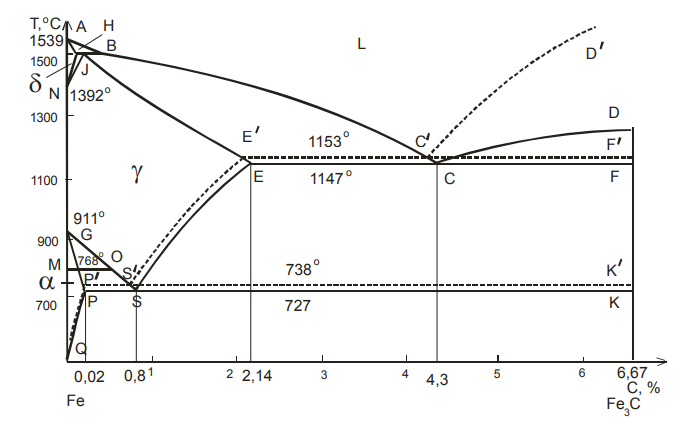
Рисунок 18. Общий вид диаграммы состояния сисмеы железо – углерод
Диаграмма состояния системы железо – углерод является одной из важнейших диаграмм двойных систем, потому что наиболее распространенные в технике сплава, а именно стали и чугуны, представляют собой сплавы железа с углеродом. В состав сталей и чугунов кроме углерода входят кремний, марганец и другие элементы, но углерод является основным компонентом, оказывающим влияние на структуру и свойства железных сплавов.
Диаграмма железо – углерод должна распространяться от железа до углерода. Железо образует с углеродом химическое соединение цементит с формулой Fe3C. Каждое устойчивое химическое соединение можно рассматривать как компонент, а диаграмму – по частям. Так как на практике применяют металлические сплавы с содержанием углерода до 5 %, то рассматриваем часть диаграммы состояния от железа до химического соединения цементита, содержащего 6,67 % углерода.
Поскольку углерод в сплавах с железом встречается в виде цементита и графита, существуют две диаграммы состояния, описывающие условия равновесия фаз в системах: железо – цементит и железо – графит. Первая диаграмма (Fе — Fе3С) называется цементитной (метастабильная), вторая (Fе – С) – графитной (стабильная). Оба варианта диаграммы приводятся вместе в одной системе координат – температура – содержание углерода (рисунок 18): сплошным линиям соответствует диаграмма метастабильная, пунктирным (совместно с некоторыми сплошными) – стабильная.
Компоненты и фазы в системе железо – углерод
Компонентами системы железо – углерод являются железо, углерод и цементит.
Железо – d-переходный металл серебристо-светлого цвета. Температура плавления – 1539 °С. Удельный вес равен 7,86 г/см3.
Одной из существенных особенностей этого металла является его полиморфизм. В твердом состоянии железо может находиться в двух модификациях – α и γ. Полиморфные превращения происходят при температурах 911 и 1392 °С. При температуре ниже 911 и выше 1392 °С существует Feα (или α-Fе) с объемно – центрированной кубической решеткой. В интервале температур 911…1392 °С устойчивым является Feγ (или γ-Fе) с гранецентрированной кубической решеткой. При превращении α→γ наблюдается уменьшение объема, так как решетка γ-Fе имеет более плотную упаковку атомов, чем решетка α-Fе. При охлаждении во время превращения γ→α наблюдается увеличение объема. В интервале температур 1392…1539 °С высокотемпературное Feα называют Feδ. Высокотемпературная модификация Feα не представляет собой новой аллотропической формы.
При температуре ниже 768 °С железо ферромагнитно, а выше – парамагнитно. Точку 768 °С, соответствующую магнитному превращению, т.е. переходу из ферромагнитного состояния в парамагнитное, называют точкой Кюри. Модификация Feγ парамагнитна.
Железо технической чистоты обладает невысокой твердостью и прочностью, высокими характеристиками пластичности. Железо со многими элементами образует растворы: с металлами – растворы замещения, с углеродом, азотом и водородом – растворы внедрения.
Углерод – неметалл, обладает полиморфным превращением: в зависимости от условий образования существует в форме графита с гексагональной кристаллической решеткой (температура плавления – 3500 °С, плотность – 2,5 г/см3) или в форме алмаза со сложной кубической решеткой с координационным числом, равным четырем (температура плавления – 5000 °С). В сплавах железа с углеродом углерод находится в состоянии твердого раствора с железом и в виде химического соединения – цементита (Fe3C), а также в свободном состоянии в виде графита (в серых чугунах).
Цементит (Fe3C) – химическое соединение железа с углеродом (карбид железа), содержит 6,67 % углерода. Кристаллическая решетка цементита ромбическая, удельный вес 7,82 г/см3 (очень близок к удельному весу железа). При высоких температурах цементит диссоциирует, поэтому температура его плавления неясна и проставляется ориентировочно – 1260 °С. Аллотропических превращений не испытывает. При низких температурах цементит слабо ферромагнитен, магнитные свойства теряет при температуре около 210 °С. Цементит имеет высокую твердость (более 800 НВ, легко царапает стекло), но чрезвычайно низкую, практически нулевую, пластичность.
Цементит способен образовывать твердые растворы замещения. Атомы углерода могут замещаться атомами неметаллов, например азотом; атомы железа – металлами, например марганцем, хромом, вольфрамом и др. Такой твердый раствор на базе решетки цементита называется легированным цементитом.
Если графит является стабильной фазой, то цементит – это метастабильная фаза. Цементит – соединение неустойчивое и при определенных условиях распадается с образованием свободного углерода в виде графита. Этот процесс имеет важное практическое значение при структурообразовании чугунов.
В системе железо – углерод существуют следующие фазы: жидкая фаза, феррит, аустенит, цементит, графит.
-
жидкая фаза – в жидком состоянии железо растворяет углерод в любых пропорциях с образованием однородной жидкой фазы;
-
феррит (Ф, α) – твердый раствор внедрения углерода в α-железе. Различают низкотемпературный феррит с предельной растворимостью углерода 0,02 % при температуре 727 °С (точка P) и высокотемпературный δ-феррит (в интервале температур 1392…1539 °С) с предельной растворимостью углерода 0,1 % при температуре 1499 °С (точка J). Свойства феррита близки к свойства железа, феррит мягок и пластичен, магнитен до 768 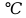 ;
;
-
аустенит (А,  ) – твердый раствор внедрения углерода в γ-железо. Углерод занимает место в центре гранецентрированной кубической ячейки. Предельная растворимость углерода в γ-железе 2,14 % при температуре 1147 °С (точка Е). Аустенит имеет твердость 200…250 НВ, пластичен, парамагнитен. При растворении в аустените других элементов могут изменяться свойства и температурные границы существования;
) – твердый раствор внедрения углерода в γ-железо. Углерод занимает место в центре гранецентрированной кубической ячейки. Предельная растворимость углерода в γ-железе 2,14 % при температуре 1147 °С (точка Е). Аустенит имеет твердость 200…250 НВ, пластичен, парамагнитен. При растворении в аустените других элементов могут изменяться свойства и температурные границы существования;
-
цементит – характеристика дана выше. В железоуглеродистых сплавах присутствуют фазы – цементит первичный, цементит вторичный, цементит третичный. Химические и физические свойства этих фаз одинаковы. Влияние на механические свойства сплавов оказывает различие в размерах, количестве и расположении этих выделений. Цементит первичный выделяется из жидкой фазы в виде крупных пластинчатых кристаллов. Цементит вторичный выделяется из аустенита и располагается в виде сетки вокруг зерен аустенита (при охлаждении – вокруг зерен перлита). Цементит третичный выделяется из феррита и в виде мелких включений располагается у границ ферритных зерен;
-
графит – характеристика дана выше.
Метастабильная диаграмма состояния системы железо – цементит
(Fe – Fe3C)
Рисунок 19. Диаграмма состояния системы железо – цементит
Ликвидус по всей диаграмме проходит по линиям АВ, ВС, СD; солидус – по линиям АН, НJ, JЕ, ЕСF. Сплавы железа с углеродом обычно делят на стали и чугуны. Условной границей для такого деления является 2,14 % С (точка E). Сплавы, содержащие углерода менее 2,14 %, относятся к сталям, более 2,14 % – к чугунам.
Температуры, при которых происходят фазовые и структурные превращения в сплавах системы железо – цементит, т.е. критические точки, обозначаются буквой А. В зависимости от того, при нагреве или при охлаждении определяется критическая точка, к букве А добавляется индекс с (от слова chauffage – нагрев) при нагреве и индекс r (от слова refroidissement – охлаждение) при охлаждении с оставлением цифры, характеризующей данное превращение.
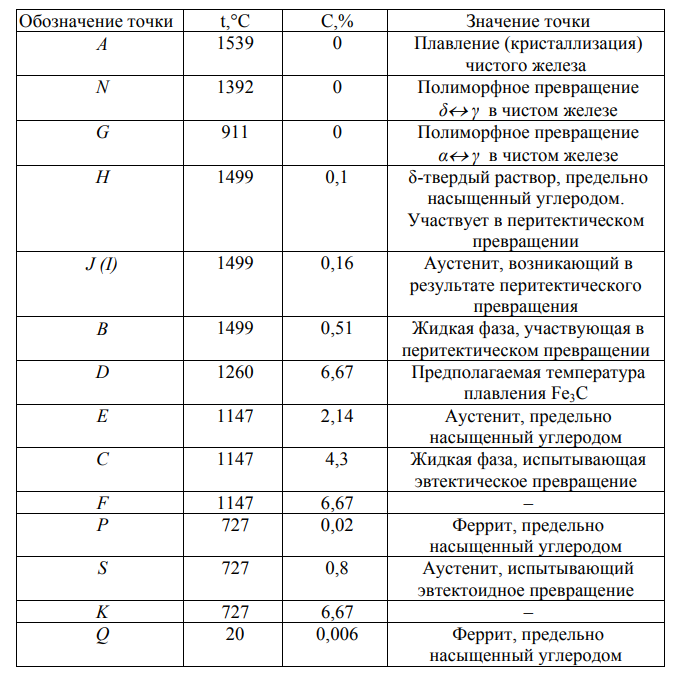
Таблица 2. Узловые точки диаграммы состояния системы Fe – Fe3C
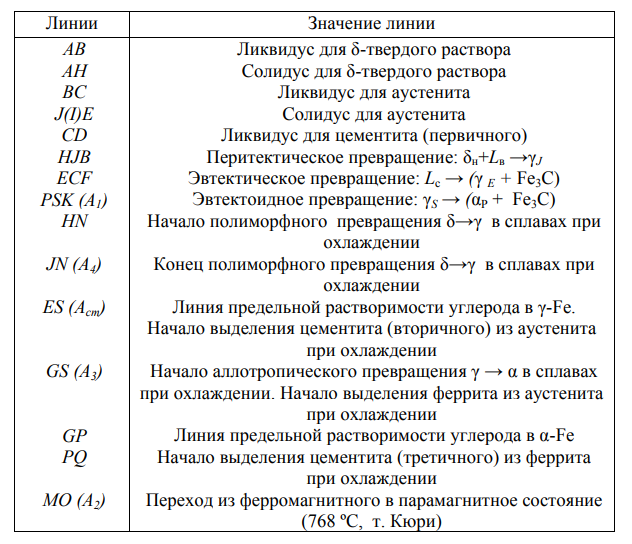
Таблица 3. Значение линий диаграммы состояния системы Fe – Fe3C
Первичная кристаллизация сталей
Рассмотрим первичную кристаллизацию сталей, для чего воспользуемся рисунком 20.
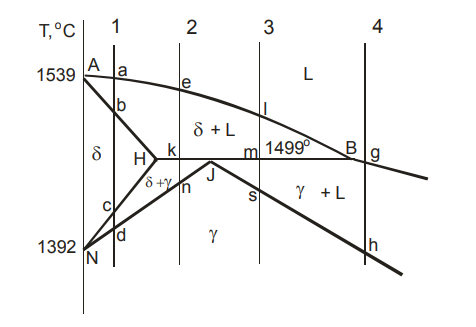
Рисунок 20. Левый верхний угол диаграммы – первичная кристаллизация сталей
Сплав 1 (0,05 % C). Кристаллизация начнется в точке a и закончится в точке b с образованием δ-твердого раствора. Углерод повышает температуру аллотропического превращения железа δ↔γ. Это перестройка решетки твердого раствора идет между точками c и d, когда одновременно существует два разных твердых раствора (состав δ-раствора изменяется по линии НN, γ-раствора – по линии JN). Ниже точки d сплав охлаждается в аустенитном состоянии.
Сплав 2 (0,13 % C). Кристаллизация δ-раствора начнется в точке е и закончится в точке k. При 1499 °C происходит перитектическое превращение:
δH +LB→ γJ
От точки k до точки п идет перестройка решетки δ→γ, и, наконец, ниже точки п сплав охлаждается в аустенитном состоянии.
Сплав 3 (0,25 % C). Кристаллизация δ-раствора начинается в точке l и заканчивается в точке m. При 1499 °C также происходит перитектическое превращение, по окончании которого в избытке оказывается жидкая фаза. От точки m до точки s продолжается кристаллизация аустенита из жидкой фазы. Ниже точки s сплав охлаждается в аустенитном состоянии.
Сплав 4 (0,6 % С). Кристаллизация сплава начинается в точке g с образования аустенита и продолжается до точки h. Ниже этой точки сплав охлаждается в аустенитном состоянии.
Таким образом, первичная кристаллизация сталей заканчивается образованием γ-фазы, т. е. аустенита.
Вторичная кристаллизация сталей
Далее рассмотрим превращения, происходящие в сталях при дальнейшем охлаждении в твердом состоянии, т.е. вторичную кристаллизацию (рисунок 21).
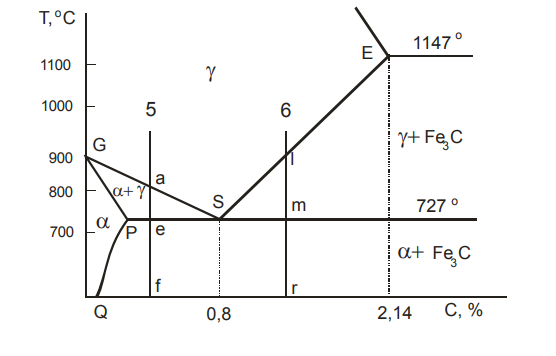
Рисунок 21. Нижний левый угол диаграммы состояния – вторичная кристаллизация сталей
Сплав 5 (0,3 % C). Выше точки a сплав находится в аустенитном состоянии. После окончания первичной кристаллизации аустенит охлаждается без каких-либо изменений. Углерод в сплавах понижает температуру полиморфного превращения γ→α. В сплаве 5 это превращение начнется на линии GS в точке а и будет развиваться далее с понижением температуры до точки е. Так в сплаве появляется феррит. Концентрация углерода в уменьшающемся по количеству аустените будет изменяться по линии GS (к точке S), а концентрация углерода в увеличивающемся по количеству феррите – по линии GP (к точке Р).
В точке е выделение феррита закончится, и сплав будет состоять из двух фаз – αр + γS .
Чуть выше линии PSK:
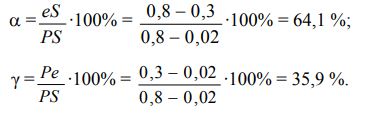
Аустенит с содержанием 0,8 % углерода на линии РSК претерпевает эвтектоидное превращение, состоящее в том, что одновременно выделяются две кристаллические фазы – феррит предельного насыщения (точка Р) и цементит:
γS→ αP + Fe3C
Возникающая при эвтектоидном распаде аустенита смесь феррита и цементита имеет тонкопластинчатое строение (чередующиеся пластинки α и Fе3С) и называется перлитом – по радужной окраске поверхности шлифа после травления, имеющей сходство с перламутром.
Феррит, который выделился из аустенита в интервале температур от точки а до точки е, в эвтектоидном превращении не участвует. Во время эвтектоидного распада аустенита на линии РSК система состоит из трех фаз: αр, γS и Fе3С, поэтому по правилу фаз:
С= К + 1– Ф = 2 + 1– 3 = 0
Устанавливаем, что число степеней свободы системы равно нулю. Следовательно, эвтектоидный распад аустенита происходит при постоянной температуре и при неизменной концентрации углерода во всех трех фазах.
Сразу после перлитного превращения система состоит из фаз α и Fe3C, их относительное количество:
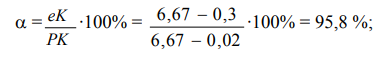
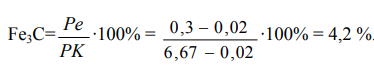
Структурные составляющие – феррит+перлит, т. е. α + (α + Fе3С). Но 95,8 % феррита делится на избыточный феррит, выделившийся в интервале ae из аустенита (64,1 %) и феррит в составе перлита (95,8 %-64,1 %=31,7 %) Цементит же весь находится в составе перлита, т.о. получается: 64,1 % α + (31,7 % α + + 4,2 % Fе3С). Количество перлита (35,9 %) соответствует количеству аустенита перед эвтектоидным превращением.
При дальнейшем охлаждении сплава, состоящего из феррита и цементита, ферритная фаза должна обедняться углеродом (по линии PQ) с выделением цементита, называемого третичным. Это фазовое превращение дает столь незначительные изменения в структуре, составе и количестве фаз, что при рассмотрении превращений в среднеуглеродистых и высокоуглеродистых сталях и чугунах им можно пренебречь. Однако превращение с выделением третичного цементита имеет большое значение для мягких сортов сталей с низким содержанием углерода, так как выделения цементной фазы могут заметно ухудшать вязкость стали.
Таким образом, при комнатной температуре сталь взятого состава (0,3 % С) в точке f состоит из двух фаз: феррита и цементита, а структурные составляющие стали (после медленного охлаждения) будут представлены так:
феррит+перлит, т. е. α + (α + Fе3С)
При этом третичный цементит не учитывается.
В микроструктуре стали с 0,3 % C после медленного охлаждения обнаруживаются зерна феррита и перлита или феррито-карбидной смеси (ФКС). Феррит – светлые зерна, темные – перлит.
Точка S диаграммы (0,8 % С) называется эвтектоидной точкой, а вся линия РSК - линией эвтектоидного или перлитного превращения. По отношению к эвтектоидной точке S стали делятся на:
-
доэвтектоидные (содержащие до 0,8 % углерода);
-
эвтектоидную (0,8 % углерода);
-
заэвтектоидные (содержащие от 0,8 до 2,14 % углерода).
Доэвтектоидные стали при комнатной температуре после медленного охлаждения имеют одни и те же структурные составляющие: избыточный феррит + перлит (количество зависит от содержания углерода).
Вторичная кристаллизация эвтектоидной стали (0,8 %) начинается сразу с эвтектоидного превращения:
γS→ αP + Fe3C
При комнатной температуре фазовые состав – 88,3 % феррита и 11,7 % цементита. В эвтектоидной стали структурная составляющая одна – перлит.
Сплав 6 (1,2 % C). После завершения первичной кристаллизации сталь охлаждается в аустенитном состоянии. Исходя из положения линии ES, можно установить, что аустенит стали с 1,2 % С вплоть до точки l (на линии ES) оказывается ненасыщенным углеродом. По достижении температуры точки l (рисунок 21) аустенит становится предельно насыщенным углеродом, и так как растворимость углерода при охлаждении уменьшается (согласно линии ES), то, начиная с точки l, из аустенита выделяется избыток углерода в виде Fе3С, называемый вторичным (избыточным) цементитом (Fe3C)II.
Чуть выше линии PSK сплав будет состоять из двух фаз – аустенита и вторичного цементита. Применяя правило рычага, можно установить, что весовое количество цементита и аустенита:
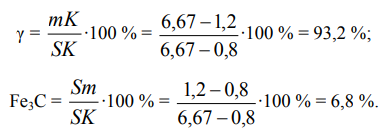
Таким образом, перед превращением сплав состоит из (93,2 % γ + 6,8 % (Fe3C)II). Структурные и фазовые составляющие совпадают.
По достижении точки т аустенит содержит 0,8 % С (точка S) и претерпевает уже известное нам эвтектоидное превращение:
γS→ αP + Fe3C
Вторичный цементит, выделившийся в интервале температур от точки l до точки m, в этом превращении не участвует. Сразу после превращения:
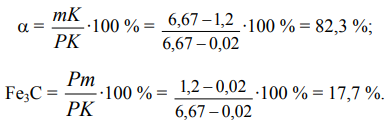
17,7 % – это общее количество цементита в сплаве, он включает в себя и 6,8 % избыточного (Fe3C)II, выделившегося в интервале lm, и цементит перлита: 17,7 %-6,8 %=10,9 %. Таким образом, получаем:
6,8 % (Fe3C)II + (82,3 % α + 10,9 % Fe3C)перлит
При дальнейшем охлаждении вплоть до точки r фазовые и структурные составляющие стали не изменяются (не забывать о поправке, сделанной при разборе сплава 5 в связи с ходом линии PQ). Сплав состоит из двух фаз феррита и цементита, а структурные составляющие стали представлены так:
цементит + перлит, т. е. (Fe3C)II + (α+Fе3С)
Таким образом, заэвтектоидные стали при комнатной температуре после медленного охлаждения имеют одни и те же структурные составляющие: вторичный избыточный цементит + перлит.
Увеличение процентного содержания углерода в структуре стали вызывает увеличение количества цементитной фазы, что приводит к росту твердости и прочности и к снижению и вязкости стали. Однако следует отметить, что прочность повышается при содержании углерода до 1 %, а затем она уменьшается (твердость при этом почти не увеличивается). Это объясняется появлением в структуре заэвтектоидной стали хрупкого вторичного цементита.
Увеличение содержания углерода приводит к повышению порога хладноломкости, также повышается электросопротивление. Углерод оказывает влияние и на технологические свойства: литейные свойства стали ухудшаются (используются стали с содержанием углерода до 0,4 %), ухудшается обрабатываемость давлением и резанием, свариваемость. Стали с низким содержанием углерода также плохо обрабатываются резанием.
Превращения в белых чугунах
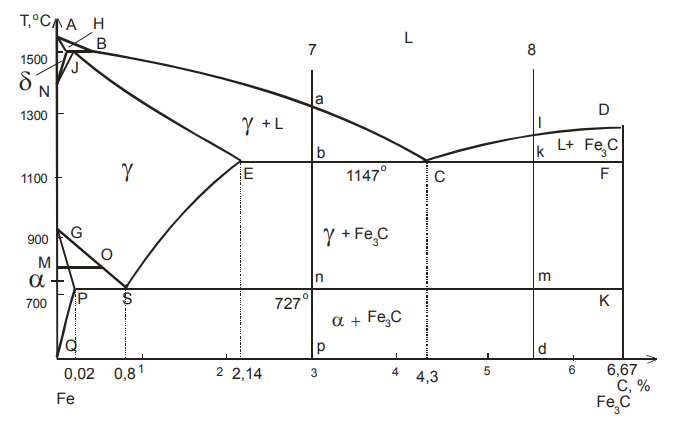
Рисунок 22. Фазовые превращения в чугунах по диаграмме состояния
Fe – Fe3C
Чугуны, кристаллизующиеся в соответствии с диаграммой состояния железо – цементит, отличаются высокой хрупкостью. В них весь углерод находится в связанном состоянии в виде цементита. Цвет их излома – серебристо-белый. Такие чугуны называются белыми чугунами.
Чугуны делятся по отношению к эвтектической точке С на:
-
на доэвтектические (углерода от 2,14 до 4,3 %);
-
эвтектический (4,3 %);
-
заэвтектические (углерода от 4,3 до 6,67 %).
Сплав 7 (3,0 % C). В этом доэвтектическом белом чугуне кристаллизация начнется в точке а с выделения аустенита и закончится в точке b. При подходе к точке b сплав состоит из аустенита предельного насыщения (точки Е) и жидкой фазы эвтектического состава (точки С).
На линии ЕCF жидкая фаза (Lс) испытывает эвтектическое превращение:
LC → γE+ Fe3C
Полученная эвтектическая смесь имеет характерное строение и называется ледебуритом. Таким образом, по окончании первичной кристаллизации (немного ниже точки b) структурные составляющие сплава – первичные зерна аустенита и ледебурит, а фазовые составляющие сплава – аустенит и цементит.
Поскольку аустенит имеет максимальное содержание углерода (2,14 %), при последующем охлаждении сплава из аустенита непрерывно выделяется вторичный цементит. Количество аустенита уменьшается, а количество цементита увеличивается. С понижением температуры концентрация углерода в аустените уменьшается согласно ходу линии ЕS. При подходе к линии РSК (точка n) сплав состоит из аустенита (точка S, рис. 22) – (γS) и Fе3С (фазовый состав). Структурные составляющие – аустенит, вторичный цементит и ледебурит.
На линии PSK (в точке n) в сплаве происходит эвтектоидное превращение с образованием перлита:
γS→ αP + Fe3C
Важно понимать, что перлитное превращение испытали зерна аустенита, выделившегося из жидкой фазы (от а до b), а также зерна аустенита, входившего в эвтектическую смесь (ледебурит). Поэтому структурные составляющие доэвтектического белого чугуна будут представлены так: перлит + вторичный цементит + превращенный ледебурит. Фазовыми составляющими сплава (в точке р) будут феррит и цементит, как и в сталях, но только в других количественных соотношениях.
Эвтектический белый чугун (4,3 % С) на линии ECF кристаллизуется сразу с образование ледебурита:
LC → γE+ Fe3C
При дальнейшем охлаждении сплава из аустенита выделяется вторичный цементит, а на линии PSK происходит перлитное превращение:
γS→ αP + Fe3C
При комнатной температуре в эвтектическом белом чугуне фазовые составляющие – феррит и цементит, структурные составляющие – превращенный ледебурит, вторичный цементит и перлит.
Сплав 8 (5,5 % C). Чугун с 5,5 % C является заэвтектическим. Его кристаллизация начнется на линии ликвидуса DС в точке l с выделения цементита, называемого первичным. Выделение цементита продолжается до точки k, и жидкая фаза, обедняясь углеродом, становится по составу соответствующей эвтектической точке C.
На линии ЕСF происходит образование ледебурита по известной реакции:
LC → γE+ Fe3C
Ниже точки k сплав состоит из двух фаз – γЕ и Fе3С. Структурные составляющие – первичный цементит и ледебурит. Вся аустенитная фаза сплава является составляющей ледебурита. При понижении температуры аустенит, обедняясь углеродом, выделяет вторичный цементит по линии ES.
Структурные составляющие – первичный и вторичные цементит и ледебурит. Наконец, на линии РSК (в точке m) аустенит превращается в перлит:
γS→ αP + Fe3C
Таким образом, структурные составляющие заэвтектического чугуна представлены как цементит первичный, цементит вторичный, превращенный ледебурит и перлит. Фазовыми же составляющими сплава будут (в точке d) те же феррит и цементит.
Стабильная диаграмма системы железо – графит (Fe – Cгр)
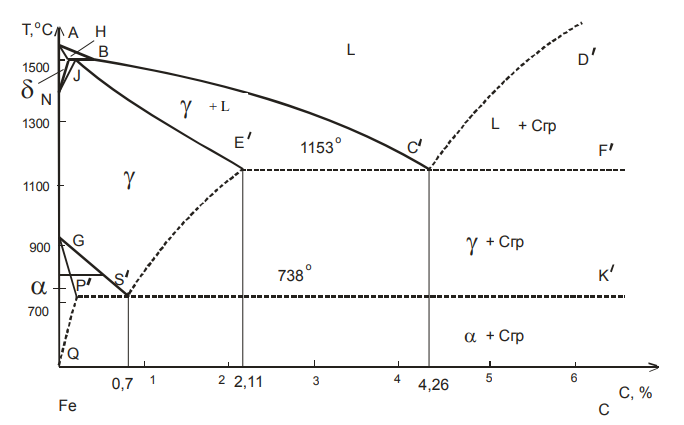
Рисунок 23. Диаграмма состояния системы железо – графит
Необходимо отметить, что фазовые превращения при наличии графита происходят при более высоких температурах, чем аналогичные им превращения при наличии цементита (пунктирные линии диаграммы находятся выше соответствующих сплошных). Критические точки С', Е', S' отвечают меньшему содержанию углерода, чем аналогичные точки С, Е, S цементитной диаграммы (точки С', Е', S' сдвинуты влево). Это объясняется большей стабильностью графита по сравнению с цементитом.
Данные о новом положении некоторых точек приведены в таблице 4, а значения пунктирных линий – в таблице 5.
внутрикристаллическая ликвация будет проявляться тем сильнее, чем больше различаются химические составы жидкой и твердой фаз, т.е. чем больше расстояние до горизонтали между линиями ликвидуса и солидуса диаграммы состояния системы;
на степень развития ВКЛ сильно влияет скорость охлаждения. Увеличение скорости охлаждения замедляет диффузионные процессы, следовательно, чем быстрее охлаждается сплав, тем более развита в нем ВКЛ. Однако замечено, что в некоторых сплавах при очень высоких скоростях охлаждения внутрикристаллическая ликвация ослабляется. Это явление объясняется тем, что в этих условиях диффузионный (избирательный) механизм кристаллизации постепенно заменяется бездиффузионным, когда растущие кристаллы присоединяют к себе все атомы компонентов из жидкой фазы, окружающей кристалл. Тогда химический состав кристаллов по всему своему объему оказывается равным химическому составу жидкой фазы и, следовательно, ликвация отсутствует;
необходимое условие возникновение ВКЛ – кристаллизация сплава в интервале температур: чем шире в жидкой и твердой фазах.
Зональная ликвация
Ликвация по поперечному сечению слитка.
Ликвация по высоте слитка.
жидкая фаза – в жидком состоянии железо растворяет углерод в любых пропорциях с образованием однородной жидкой фазы;
феррит (Ф, α) – твердый раствор внедрения углерода в α-железе. Различают низкотемпературный феррит с предельной растворимостью углерода 0,02 % при температуре 727 °С (точка P) и высокотемпературный δ-феррит (в интервале температур 1392…1539 °С) с предельной растворимостью углерода 0,1 % при температуре 1499 °С (точка J). Свойства феррита близки к свойства железа, феррит мягок и пластичен, магнитен до 768
 ;
;аустенит (А,
 ) – твердый раствор внедрения углерода в γ-железо. Углерод занимает место в центре гранецентрированной кубической ячейки. Предельная растворимость углерода в γ-железе 2,14 % при температуре 1147 °С (точка Е). Аустенит имеет твердость 200…250 НВ, пластичен, парамагнитен. При растворении в аустените других элементов могут изменяться свойства и температурные границы существования;
) – твердый раствор внедрения углерода в γ-железо. Углерод занимает место в центре гранецентрированной кубической ячейки. Предельная растворимость углерода в γ-железе 2,14 % при температуре 1147 °С (точка Е). Аустенит имеет твердость 200…250 НВ, пластичен, парамагнитен. При растворении в аустените других элементов могут изменяться свойства и температурные границы существования;цементит – характеристика дана выше. В железоуглеродистых сплавах присутствуют фазы – цементит первичный, цементит вторичный, цементит третичный. Химические и физические свойства этих фаз одинаковы. Влияние на механические свойства сплавов оказывает различие в размерах, количестве и расположении этих выделений. Цементит первичный выделяется из жидкой фазы в виде крупных пластинчатых кристаллов. Цементит вторичный выделяется из аустенита и располагается в виде сетки вокруг зерен аустенита (при охлаждении – вокруг зерен перлита). Цементит третичный выделяется из феррита и в виде мелких включений располагается у границ ферритных зерен;
графит – характеристика дана выше.
доэвтектоидные (содержащие до 0,8 % углерода);
эвтектоидную (0,8 % углерода);
заэвтектоидные (содержащие от 0,8 до 2,14 % углерода).
на доэвтектические (углерода от 2,14 до 4,3 %);
эвтектический (4,3 %);
заэвтектические (углерода от 4,3 до 6,67 %).
| Точка | Температура, °С | Концентрация углерода, % | Значение точки |
| С’ | 1153 | 4,26 | Жидкая фаза, испытывающая эвтектическое превращение |
| D’ | 3500 | 100 | Плавление (кристаллизация) графита |
| E’ | 1153 | 2,11 | Аустенит, предельно насыщенный углеродом |
| S’ | 738 | 0,7 | Аустенит, испытывающий эвтектоидное превращение |