ВУЗ: Казахский национальный медицинский университет им. С.Д. Асфендиярова
Категория: Шпаргалка
Дисциплина: Химия
Добавлен: 05.02.2019
Просмотров: 12597
Скачиваний: 45

132. физические и химические
свОйства мОнОсахаридОв
физические свойства.
Моносахариды — твердые вещества, способные крис
таллизовываться. Все моносахариды легко раствори
мы в воде. Растворы моносахаридов обладают слад
ким вкусом, оптической активностью, которая обычно
после приготовления раствора некоторое время из
меняется, пока не установится равновесие между та
утомерными формами (мутаротация). В спиртах мо
носахариды растворяются плохо, а в эфире не рас
творяются вообще.
химические свойства.
1. восстановление. При действии восстановите
лей глюкоза превращается в шестиатомный спирт
сорбит.
2. Окисление. Хлорная вода окисляет альдегидную
группу до карбоксильной.
3. реакция с фенилгидразином. При нагревании
глюкозы с избытком фенилгидразина сначала реаги
рует ее альдегидная группа и образуется продукт за
мещения карбонильного кислорода на остаток фенил
гидразина. Вторая молекула фенилгидразина дей
ствует как окислитель, превращая соседний с альде
гидной группой гидроксил в группу С=О, которая
реагирует обычным образом с третьей молекулой фе
нилгидразина.
4. алкилирование. При действии алкилирующих
средств (диметилсульфатом и щелочью или йодис
тым метилом и оксидом серебра) на глюкозу можно
получить ее простые эфиры — пентаОметилaD
глюкоза (Ирвин, Хеуорс).

5. ацилирование. При действии ацилирующих
средств (уксусный ангидрид) гидроксильные группы
глюкозы легко превращаются в сложноэфирные.
6. действие оснований. При действии слабых ос
нований происходит эпимеризация моносахари
дов — процесс обращения конфигурации при асим
метрическом атоме углерода, ближайшем к альде
гидному концу молекулы. Одновременно происходит
взаимное превращение альдоз и кетоз.
7. действие кислот. При нагревании с минераль
ными кислотами пентоз от них отщепляется вода и
образуется фурфурол.
Гексозы дают сначала неустойчивый оксиметил
фурфурол, который далее разлагается с образовани
ем левулиновой и муравьиной кислот.
8. брожение — это процесс расщепления моноса
харидов под влиянием различных микроорганизмов,
приводящий к образованию спирта, молочной кисло
ты и т.д.
9. реакция «серебряного зеркала»: реакция с
аммиачным раствором оксида серебра (реактив
Толленса) по альдегидной группе; при этом выделя
ется металлическое серебро и образуется глюконо
вая кислота.
10. глюкоза восстанавливает фелингову жид-
кость, из раствора выделяется оксид меди (I) в виде
красного осадка. Фелингова жидкость — растворимый в
воде яркосинего цвета комплекс гидроксида меди (II) с
двойной солью винной кислоты — тартрат калиянатрия
(сегнетова соль).

133. ОлигОсахариды
В зависимости от числа молекул моносахаридов,
входящих в состав олигосахарида, выделяют дисаха
риды, трисахариды и т.д.
строение дисахаридов и их свойства. Дисахари
ды построены по типу гликозидов: все они представ
ляют собой производные циклической формы моно
сахарида, у которого атом водорода в полуацеталь
ном гидроксиле замещен остатком другой молекулы
моносахарида. Остатки двух молекул моносахарида
могут быть одинаковыми и разными. В создании свя
зи могут участвовать оба гликозидных гидроксила
или один гликозидный и один спиртовой.
Различают невосстанавливающие и восстанав-
ливающие дисахариды. У невосстанавливающих
дисахаридов (трегалозы, сахарозы) нет свободных
гликозидных гидроксилов, они не способны перехо
дить в таутомерную альдегидную форму, а следова
тельно, не могут вступать в свойственные этой форме
реакции («серебряного зеркала»), не восстанавлива
ют фелингову жидкость. Они могут вступать лишь в
реакции, обусловленные присутствием гидроксиль
ных групп (алкилирование, ацилирование).
У восстанавливающих дисахаридов [целлобиоза
(2 молекулы глюкозы, соединенные βгликозидной свя
зью), мальтоза (2 молекулы глюкозы, соединенные
aгликозидной связью), лактоза (глюкоза + галакто
за)] имеется свободный гликозидный гидроксил, сле
довательно, они могут переходить в альдегидную
форму, т.е. проявлять восстановительные свойства.
Восстанавливающие дисахариды вступают в те же хи
мические реакции, что и моносахариды, т.е. образу
ют алкильные и ацильные производные за счет своих

гидроксильных групп, окисляются до монокарбоно
вых кислот, дают реакцию «серебряного зеркала»,
восстанавливают фелингову жидкость.
Фенилгидразин и подобные ему ароматические
производные гидразина реагируют с альдозами и ке
тозами с образованием гидразонов, которые превра
щаются в фенилозазоны. Озазоны — кристаллизую
щиеся вещества желтого цвета, растворимые в воде,
используются для выделения и идентификации саха
ров.
При кислотном или ферментативном гидролизе
дисахариды гидролизуются до моносахаридов, при
этом изменяется знак оптического вращения: право
вращающая сахароза превращается в левовращаю
щую смесь глюкозы и фруктозы. Этот процесс назы
вают инверсией.
134. пОлисахариды (крахмал)
Полисахариды — продукты конденсации большого
числа молекул моносахаридов друг с другом. Состав
их выражается формулой (С
6
Н
10
О
5
)
n
, где n достигает
величины сотен и тысяч.
крахмал.
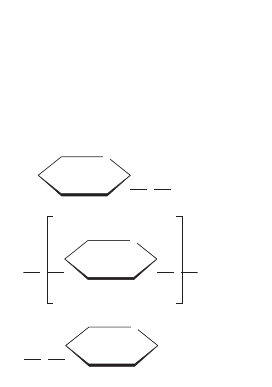
строение. Крахмал — смесь полисахаридов амино
пектина и амилозы. И амилоза, и амилопектин состоят
из остатков глюкозы, связанных aгликозидными связя
ми, однако они различаются формой молекул. Амило
за — линейный полисахарид, амилопектин имеет раз
ветвленное строение:
H
|
OH
H
|
OH
|
H
H
|
OH
CH
2
OH
|
H
O
(S)
(R)
O
H
|
CH
2
OH
|
H
OH
|
H
O
H
|
OH
(S)
O
H
|
(R)
O
n
OH
|
H
(R)
H
|
CH
2
OH
|
H
OH
|
H
O
H
|
OH
(S)
O