Файл: Изучение молекулярных предикторов сосудистого риска опосредованного эндотелиальной дисфункцией у людей с сахарным диабетом 2 типа.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 05.12.2023
Просмотров: 111
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
СОДЕРЖАНИЕ
КЛИНИЧЕСКАЯ ДИАГНОСТИКА ИНСУЛИНОВОЙ РЕЗИСТЕНТНОСТИ
МОЛЕКУЛЯРНЫЕ МАРКЕРЫ ИНСУЛИНОВОЙ РЕЗИСТЕНТНОСТИ
ШАПЕРОНЫ И МАЛЫЕ БЕЛКИ ТЕПЛОВОГО ШОКА
ИНСУЛИНОВАЯ РЕЗИСТЕНТНОСТЬ, КАРБОНИЛЬНЫЙ СТРЕСС И ДИСФУНКЦИЯ ЭНДОТЕЛИЯ
ИНСУЛИНОВАЯ РЕЗИСТЕНТНОСТЬ, АДИПОГЕННАЯ ДИФФЕРЕНЦИРОВКА И ТРАНСКРИПЦИОННЫЙ ФАКТОР PREP1
ИНСУЛИНОВАЯ РЕЗИСТЕНТНОСТЬ, ЛИПОДИСТРОФИЯ И МУТАЦИИ ГЕНОВ
[22, 44]. Гликозилирование коллагена вызывает изменение его физико-химических свойств, которые проявляются меньшей растворимостью и большей устойчивостью к действию коллагеназы [21].
Конечные продукты гликирования оказывают выраженное влияние на состояние сосудистой стенки несколькими механизмами, которые могут быть разделены на рецепторные и нерецепторные. Первая группа связана со взаимодействием конечных продуктов гликирования с рецепторами эндотелиоцитов, вторая группа механизмов осуществляется за счет изменения конформации и активности ферментов, неспецифического связывания рецепторов и изменения их аффинитета и внутренней активности. Конечные продукты гликирования вызывают нарушение барьерной функции сосудистой стенки, повышают экспрессию адгезивных молекул, индуцируют образование активных форм кислорода, выработку провоспалительных цитокинов, повышают экспрессию индуцибельной NOS, что блокирует активность эндотелиальной NOS и снижает биодоступность NO, то есть в конечном итоге приводят к эндотелиальной дисфункции [47−49]. При этом показано, что конечные продукты гликирования оказывают непосредственное ингибирующее влияние на антиоксидантные ферменты, в частности PON2, что способствует развитию оксидативного стресса [50]. Кроме того, воздействие конечных продуктов гликирования на КПГ-рецепторы моноцитов и макрофагов вызывает их активацию и запускает экспрессию ими провоспалительных цитокинов, которые являются важным патогенетическим звеном в возникновении и развитии сосудистого воспаления и атерогенеза [14, 16].
Накопление конечных продуктов гликирования при прогрессировании диабета способствует структурному ремоделированию сосудистой стенки, что проявляется, в частности, увеличением толщины интимы и медии сонных артерий [51].
Таким образом, накопление конечных продуктов гликирования является одним из пусковых механизмов в возникновении эндотелиальной дисфункции при сахарном диабете. Эндотелиальная дисфункция, в свою очередь, играет инициирующую роль в каскаде последовательных процессов, происходящих в сосудистой стенке и приводящих к ее морфологическим изменениям.
ВЫВОДЫ
Эндотелиальная функция играет важную роль в поддержании гомеостаза организма, и на сегодняшний день сформулирована концепция, согласно которой эндотелиальная дисфункция является центральным звеном в патогенезе многих заболеваний, включая сахарный диабет. Проведенный анализ литературы свидетельствует, что развитие эндотелиальной дисфункции при сахарном диабете складывается из нескольких ключевых аспектов, которые могут быть представлены в виде схемы (рис.) Так, представленные данные позволяют выделить среди основных факторов, инициирующих альтерацию эндотелиальных клеток, гипергликемию и накопление конечных продуктов гликирования. Гипергликемия, обусловливающая активацию полиолового и гексозаминового путей, а также накопление продуктов гликолиза в совокупности с рецепторным и нерецепторным воздействием конечных продуктов гликирования нарушают метаболизм и функционирование сигнальных систем эндотелиоцитов как за счет изменения активности ферментов, в частности протеинкиназы С, эндотелиальной NOS, так и за счет изменения экспрессии ряда генов, в том числе гиперэкспрессии генов NADPH-оксидаз, PAI-1, VEGF, индуцибельной NOS, провоспалительных цитокинов.
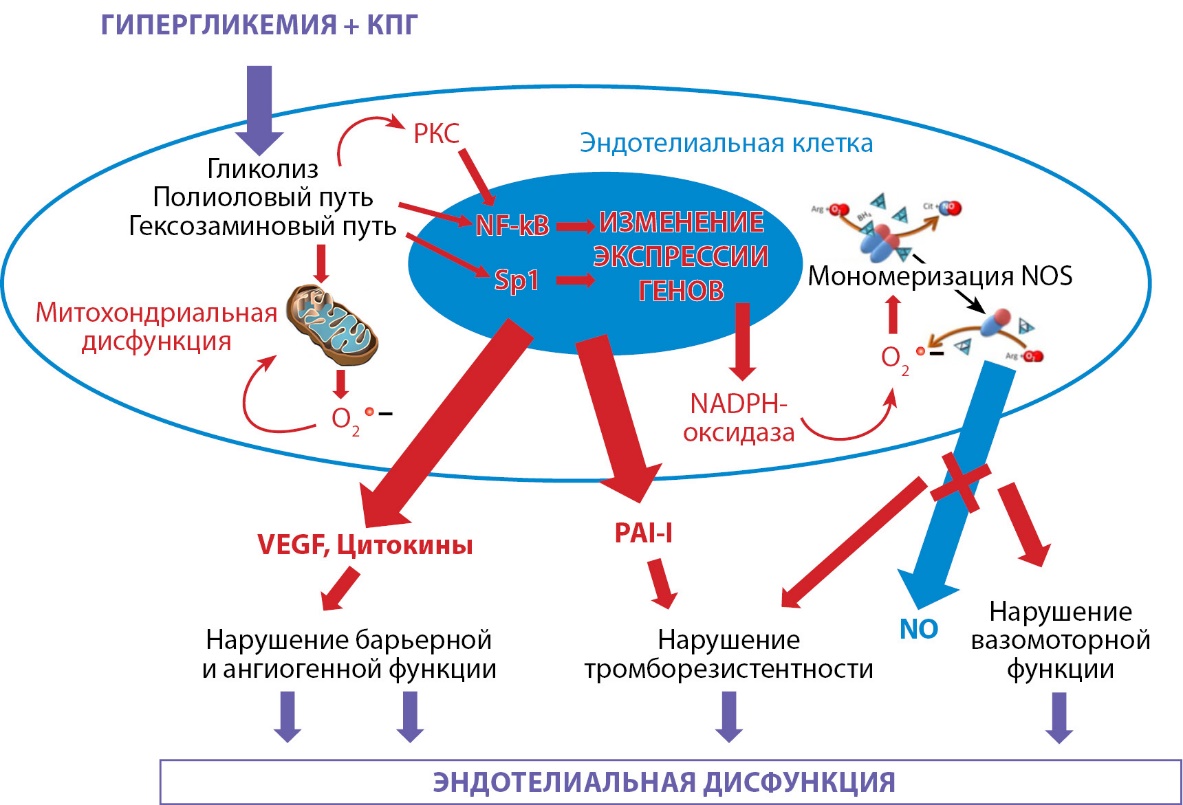
Рис. Схема патогенеза эндотелиальной дисфункции при сахарном диабете
Примечания. КПГ — конечные продукты гликирования; РКС — протеинкиназа С; NOS — NO-синтаза; O2 — супероксидный анион; VEGF — фактор роста эндотелия сосудов; PAI-I — ингибитор активатора плазминогена; NO — оксид азота.
Наиболее значимыми проявлениями дисметаболизма эндотелиоцитов при сахарном диабете следует считать оксидативный стресс и нарушения цикла оксида азота. Оксидативный стресс эндотелиоцитов при сахарном диабете сопряжен с формированием патогенетических порочных кругов, включая митохондриальную дисфункцию и мономеризацию эндотелиальной NOS, приводящих к стойкой гиперпродукции активных форм кислорода, которая при функциональной недостаточности антиоксидантных систем обеспечивает прогрессирующее повреждение и дисфункцию эндотелия. Следовательно, патогенетическая коррекция эндотелиальной дисфункции при сахарном диабете должна быть направлена не только на обеспечение адекватного гликемического контроля, но и на устранение явлений оксидативного стресса. В этой связи в качестве мишени таргетной терапии и профилактики ангиопатий может выступать система неферментных и ферментных антиоксидантов.
Результатом оксидативного стресса эндотелиальных клеток являются ингибирование эндотелиальной NOS, уменьшение продукции и биодоступности NO, что обусловливает снижение его способности эффективно оказывать паракринные дилататорные эффекты на гладкомышечные клетки, обусловливая нарушение вазомоторной функции, а следовательно, сосудистого тонуса и артериального давления. Кроме того, снижение биодоступности NO, в том числе изменение паракринных взаимодействий с тромбоцитами и лейкоцитами, а также гиперэкспрессия PAI-1 нарушают тромборезистентность эндотелия, что может вызывать внутрисосудистые нарушения микроциркуляции, которые неизбежно приводят к гипоксии, еще больше усугубляющей эндотелиальную дисфункцию. Нарушение аутокринных регуляторных эффектов NO в сочетании с гиперэкспрессией VEGF и провоспалительных цитокинов вызывает изменения барьерной и ангиогенной функций эндотелиоцитов, что обусловливает структурное ремоделирование сосудистого русла
, приводящее к развитию ангиопатий. Следовательно, эндотелиальная дисфункция при сахарном диабете проявляется нарушением всех основных функций эндотелия, включая барьерную, вазомоторную, ангиогенную и тромборезистентность. Ряд эффективных терапевтических стратегий, используемых в настоящее время для лечения пациентов с диабетическими ангиопатиями, направлены на коррекцию отдельных функций эндотелиальных клеток (лечение вазодилататорами, антиагрегантами, антикоагулянтами; антиангиогенная терапия). Для повышения эффективности подобных схем лечения необходимы дальнейшие исследования сложных взаимосвязей указанных нарушений при развитии эндотелиальной дисфункции у пациентов с сахарным диабетом.
ЗАКЛЮЧЕНИЕ
Таким образом, патогенез эндотелиальной дисфункции при сахарном диабете многокомпонентный и многие его аспекты нуждаются в уточнении. Для эффективной профилактики и лечения диабетических ангиопатий требуется разработка комплексных патогенетически обоснованных лечебных схем, включающих адекватный гликемический контроль, подавление оксидативного стресса и коррекцию нарушенных функций эндотелиальных клеток.
ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ
Источник финансирования. Работа выполнена в рамках государственного задания ФГБОУ ВО «Саратовский государственный медицинский университет им. В.И. Разумовского» Минздрава России «Разработка технологий медикаментозной и немедикаментозной коррекции микроциркуляторных нарушений при сахарном диабете, сопровождающемся абсолютной недостаточностью инсулина, в условиях эксперимента» (регистрационный номер АААА-А19-119021190053-0).
Конфликт интересов. Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с публикацией настоящей статьи.
Участие авторов: Э.Б. Попыхова — анализ источников литературы, написание текста статьи; Т.В. Степанова — подбор источников литературы, оформление статьи; Д.Д. Лагутина — подбор источников литературы, подготовка иллюстрации; Т.С. Кириязи — подбор и анализ источников литературы; А.Н. Иванов — разработка концепции, редактирование текста статьи. Все авторы внесли значимый вклад в проведение поисково-аналитической работы и подготовку статьи, прочли и одобрили финальную версию до публикации.
СПИСОК ЛИТЕРАТУРЫ
↑1. Куликов Д.А., Глазков А.А., Ковалева Ю.А., и др. Перспективы использования лазерной допплеровской флоуметрии в оценке кожной микроциркуляции крови при сахарном диабете // Сахарный диабет - 2017. - Т.20. - №4. - С. 279−285. [Kulikov DA, Glazkov AA, Kovaleva YuA, et al. Prospects of laser doppler flowmetry application in assessment of skin microcirculation in diabetes. Diabetes Mellitus. 2017;20(4):279−285. (In Russ).] https://doi.org/10.14341/DM8014
↑2. Гоженко А.И., Кузнецова А.С., Кузнецова Е.С., и др. Эндотелиальная дисфункция в патогенезе осложнений сахарного диабета. Сообщение I. Эндотелиальная дисфункция: этиология, патогенез и методы диагностики // Ендокринологія’. - 2017. - Т.22. - №2. - С. 171−181. [Gozhenko AI, Kuznetsova HS, Kuznetsova KS, et al. Endothelial dysfunction in the pathogenesis of diabetes complications. The message I. Endothelial dysfunction: etiology, pathogenesis and diagnostic methods. Endokrinologiia. 2017;22(2):171−181. (In Russ).]
↑3. Васина Л.В., Петрищев Н.Н., Власов Т.Д. Эндотелиальная дисфункция и ее основные маркеры // Регионарное кровообращение и микроциркуляция. - 2017. - Т.16. - №1. - С. 4-15. [Vasina LV, Petrishchev NN, Vlasov TD. Markers of endothelial dysfunction. Regional blood circulation and microcirculation. 2017;16(1):4-15. (In Russ).] https://doi.org/10.24884/1682-6655-2017-16-1-4-15
↑4. Васина Л.В., Власов Т.Д., Петрищев Н.Н. Функциональная гетерогенность эндотелия (обзор) // Артериальная гипертензия. - 2017. - Т.23. - №2. - С. 88-102. [Vasina LV, Vlasov TD, Petrishchev NN. Functional heterogeneity of the endothelium (the review). Arterial hypertension. 2017;23(2):88-102. (In Russ).] https://doi.org/10.18705/1607-419X-2017-23-2-88-102
↑5. Мельникова Ю.С., Макарова Т.П. Эндотелиальная дисфункция как центральное звено патогенеза хронических болезней // Казанский медицинский журнал. - 2015. - Т.96. - №4. - C. 659-665. [Mel’nikova JuS, Makarova TP. Endothelial dysfunction as the key link of chronic diseases pathogenesis. Kazan Medical Journal. 2015;96(4):659-665. (In Russ).] https://doi.org/10.17750/KMJ2015-659
↑6. Власов Т.Д., Нестерович И.И., Шиманьски Д.А. Эндотелиальная дисфункция: от частного к общему. Возврат к «старой парадигме»? // Регионарное кровообращение и микроциркуляция. - 2019. - Т.18. - №2. - С. 19-27. [Vlasov TD, Nesterovich II, Shimanski DA. Endothelial dysfunction: from the particular to the general. Return to the «Old Paradigm»? Regional hemodynamics and microcirculation. 2019;18(2):19-27. (In Russ).] https://doi.org/10.24884/1682-6655-2019-18-2-19-27
↑7. Степанова Т.В., Иванов А.Н., Терешкина Н.Е., и др. Маркеры эндотелиальной дисфункции: патогенетическая роль и диагностическое значение (обзор литературы) // Клиническая лабораторная диагностика. - 2019. - Т.64. - №1. - С. 34−41. [Stepanova TV, Ivanov AN, Tereshkina NE, et al. Markers of endothelial dysfunction: pathogenetic role and diagnostic significance. Klinicheskaia laboratornaia diagnostika. 2019;64(1):34−41. (In Russ).]
↑8. Torimoto K, Okada Y, Tanaka Y. Type 2 diabetes and vascular endothelial dysfunction. J Uoeh. 2018;40(1):65-75. https://doi.org/10.7888/juoeh.40.65
↑9. Sena CM, Pereira AM, Seiça R. Endothelial dysfunction - a major mediator of diabetic vascular disease. Biochimica Biophysica Acta. 2013;1832:2216-2231.
Конечные продукты гликирования оказывают выраженное влияние на состояние сосудистой стенки несколькими механизмами, которые могут быть разделены на рецепторные и нерецепторные. Первая группа связана со взаимодействием конечных продуктов гликирования с рецепторами эндотелиоцитов, вторая группа механизмов осуществляется за счет изменения конформации и активности ферментов, неспецифического связывания рецепторов и изменения их аффинитета и внутренней активности. Конечные продукты гликирования вызывают нарушение барьерной функции сосудистой стенки, повышают экспрессию адгезивных молекул, индуцируют образование активных форм кислорода, выработку провоспалительных цитокинов, повышают экспрессию индуцибельной NOS, что блокирует активность эндотелиальной NOS и снижает биодоступность NO, то есть в конечном итоге приводят к эндотелиальной дисфункции [47−49]. При этом показано, что конечные продукты гликирования оказывают непосредственное ингибирующее влияние на антиоксидантные ферменты, в частности PON2, что способствует развитию оксидативного стресса [50]. Кроме того, воздействие конечных продуктов гликирования на КПГ-рецепторы моноцитов и макрофагов вызывает их активацию и запускает экспрессию ими провоспалительных цитокинов, которые являются важным патогенетическим звеном в возникновении и развитии сосудистого воспаления и атерогенеза [14, 16].
Накопление конечных продуктов гликирования при прогрессировании диабета способствует структурному ремоделированию сосудистой стенки, что проявляется, в частности, увеличением толщины интимы и медии сонных артерий [51].
Таким образом, накопление конечных продуктов гликирования является одним из пусковых механизмов в возникновении эндотелиальной дисфункции при сахарном диабете. Эндотелиальная дисфункция, в свою очередь, играет инициирующую роль в каскаде последовательных процессов, происходящих в сосудистой стенке и приводящих к ее морфологическим изменениям.
ВЫВОДЫ
Эндотелиальная функция играет важную роль в поддержании гомеостаза организма, и на сегодняшний день сформулирована концепция, согласно которой эндотелиальная дисфункция является центральным звеном в патогенезе многих заболеваний, включая сахарный диабет. Проведенный анализ литературы свидетельствует, что развитие эндотелиальной дисфункции при сахарном диабете складывается из нескольких ключевых аспектов, которые могут быть представлены в виде схемы (рис.) Так, представленные данные позволяют выделить среди основных факторов, инициирующих альтерацию эндотелиальных клеток, гипергликемию и накопление конечных продуктов гликирования. Гипергликемия, обусловливающая активацию полиолового и гексозаминового путей, а также накопление продуктов гликолиза в совокупности с рецепторным и нерецепторным воздействием конечных продуктов гликирования нарушают метаболизм и функционирование сигнальных систем эндотелиоцитов как за счет изменения активности ферментов, в частности протеинкиназы С, эндотелиальной NOS, так и за счет изменения экспрессии ряда генов, в том числе гиперэкспрессии генов NADPH-оксидаз, PAI-1, VEGF, индуцибельной NOS, провоспалительных цитокинов.

Рис. Схема патогенеза эндотелиальной дисфункции при сахарном диабете
Примечания. КПГ — конечные продукты гликирования; РКС — протеинкиназа С; NOS — NO-синтаза; O2 — супероксидный анион; VEGF — фактор роста эндотелия сосудов; PAI-I — ингибитор активатора плазминогена; NO — оксид азота.
Наиболее значимыми проявлениями дисметаболизма эндотелиоцитов при сахарном диабете следует считать оксидативный стресс и нарушения цикла оксида азота. Оксидативный стресс эндотелиоцитов при сахарном диабете сопряжен с формированием патогенетических порочных кругов, включая митохондриальную дисфункцию и мономеризацию эндотелиальной NOS, приводящих к стойкой гиперпродукции активных форм кислорода, которая при функциональной недостаточности антиоксидантных систем обеспечивает прогрессирующее повреждение и дисфункцию эндотелия. Следовательно, патогенетическая коррекция эндотелиальной дисфункции при сахарном диабете должна быть направлена не только на обеспечение адекватного гликемического контроля, но и на устранение явлений оксидативного стресса. В этой связи в качестве мишени таргетной терапии и профилактики ангиопатий может выступать система неферментных и ферментных антиоксидантов.
Результатом оксидативного стресса эндотелиальных клеток являются ингибирование эндотелиальной NOS, уменьшение продукции и биодоступности NO, что обусловливает снижение его способности эффективно оказывать паракринные дилататорные эффекты на гладкомышечные клетки, обусловливая нарушение вазомоторной функции, а следовательно, сосудистого тонуса и артериального давления. Кроме того, снижение биодоступности NO, в том числе изменение паракринных взаимодействий с тромбоцитами и лейкоцитами, а также гиперэкспрессия PAI-1 нарушают тромборезистентность эндотелия, что может вызывать внутрисосудистые нарушения микроциркуляции, которые неизбежно приводят к гипоксии, еще больше усугубляющей эндотелиальную дисфункцию. Нарушение аутокринных регуляторных эффектов NO в сочетании с гиперэкспрессией VEGF и провоспалительных цитокинов вызывает изменения барьерной и ангиогенной функций эндотелиоцитов, что обусловливает структурное ремоделирование сосудистого русла
, приводящее к развитию ангиопатий. Следовательно, эндотелиальная дисфункция при сахарном диабете проявляется нарушением всех основных функций эндотелия, включая барьерную, вазомоторную, ангиогенную и тромборезистентность. Ряд эффективных терапевтических стратегий, используемых в настоящее время для лечения пациентов с диабетическими ангиопатиями, направлены на коррекцию отдельных функций эндотелиальных клеток (лечение вазодилататорами, антиагрегантами, антикоагулянтами; антиангиогенная терапия). Для повышения эффективности подобных схем лечения необходимы дальнейшие исследования сложных взаимосвязей указанных нарушений при развитии эндотелиальной дисфункции у пациентов с сахарным диабетом.
ЗАКЛЮЧЕНИЕ
Таким образом, патогенез эндотелиальной дисфункции при сахарном диабете многокомпонентный и многие его аспекты нуждаются в уточнении. Для эффективной профилактики и лечения диабетических ангиопатий требуется разработка комплексных патогенетически обоснованных лечебных схем, включающих адекватный гликемический контроль, подавление оксидативного стресса и коррекцию нарушенных функций эндотелиальных клеток.
ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ
Источник финансирования. Работа выполнена в рамках государственного задания ФГБОУ ВО «Саратовский государственный медицинский университет им. В.И. Разумовского» Минздрава России «Разработка технологий медикаментозной и немедикаментозной коррекции микроциркуляторных нарушений при сахарном диабете, сопровождающемся абсолютной недостаточностью инсулина, в условиях эксперимента» (регистрационный номер АААА-А19-119021190053-0).
Конфликт интересов. Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с публикацией настоящей статьи.
Участие авторов: Э.Б. Попыхова — анализ источников литературы, написание текста статьи; Т.В. Степанова — подбор источников литературы, оформление статьи; Д.Д. Лагутина — подбор источников литературы, подготовка иллюстрации; Т.С. Кириязи — подбор и анализ источников литературы; А.Н. Иванов — разработка концепции, редактирование текста статьи. Все авторы внесли значимый вклад в проведение поисково-аналитической работы и подготовку статьи, прочли и одобрили финальную версию до публикации.
СПИСОК ЛИТЕРАТУРЫ
↑1. Куликов Д.А., Глазков А.А., Ковалева Ю.А., и др. Перспективы использования лазерной допплеровской флоуметрии в оценке кожной микроциркуляции крови при сахарном диабете // Сахарный диабет - 2017. - Т.20. - №4. - С. 279−285. [Kulikov DA, Glazkov AA, Kovaleva YuA, et al. Prospects of laser doppler flowmetry application in assessment of skin microcirculation in diabetes. Diabetes Mellitus. 2017;20(4):279−285. (In Russ).] https://doi.org/10.14341/DM8014
↑2. Гоженко А.И., Кузнецова А.С., Кузнецова Е.С., и др. Эндотелиальная дисфункция в патогенезе осложнений сахарного диабета. Сообщение I. Эндотелиальная дисфункция: этиология, патогенез и методы диагностики // Ендокринологія’. - 2017. - Т.22. - №2. - С. 171−181. [Gozhenko AI, Kuznetsova HS, Kuznetsova KS, et al. Endothelial dysfunction in the pathogenesis of diabetes complications. The message I. Endothelial dysfunction: etiology, pathogenesis and diagnostic methods. Endokrinologiia. 2017;22(2):171−181. (In Russ).]
↑3. Васина Л.В., Петрищев Н.Н., Власов Т.Д. Эндотелиальная дисфункция и ее основные маркеры // Регионарное кровообращение и микроциркуляция. - 2017. - Т.16. - №1. - С. 4-15. [Vasina LV, Petrishchev NN, Vlasov TD. Markers of endothelial dysfunction. Regional blood circulation and microcirculation. 2017;16(1):4-15. (In Russ).] https://doi.org/10.24884/1682-6655-2017-16-1-4-15
↑4. Васина Л.В., Власов Т.Д., Петрищев Н.Н. Функциональная гетерогенность эндотелия (обзор) // Артериальная гипертензия. - 2017. - Т.23. - №2. - С. 88-102. [Vasina LV, Vlasov TD, Petrishchev NN. Functional heterogeneity of the endothelium (the review). Arterial hypertension. 2017;23(2):88-102. (In Russ).] https://doi.org/10.18705/1607-419X-2017-23-2-88-102
↑5. Мельникова Ю.С., Макарова Т.П. Эндотелиальная дисфункция как центральное звено патогенеза хронических болезней // Казанский медицинский журнал. - 2015. - Т.96. - №4. - C. 659-665. [Mel’nikova JuS, Makarova TP. Endothelial dysfunction as the key link of chronic diseases pathogenesis. Kazan Medical Journal. 2015;96(4):659-665. (In Russ).] https://doi.org/10.17750/KMJ2015-659
↑6. Власов Т.Д., Нестерович И.И., Шиманьски Д.А. Эндотелиальная дисфункция: от частного к общему. Возврат к «старой парадигме»? // Регионарное кровообращение и микроциркуляция. - 2019. - Т.18. - №2. - С. 19-27. [Vlasov TD, Nesterovich II, Shimanski DA. Endothelial dysfunction: from the particular to the general. Return to the «Old Paradigm»? Regional hemodynamics and microcirculation. 2019;18(2):19-27. (In Russ).] https://doi.org/10.24884/1682-6655-2019-18-2-19-27
↑7. Степанова Т.В., Иванов А.Н., Терешкина Н.Е., и др. Маркеры эндотелиальной дисфункции: патогенетическая роль и диагностическое значение (обзор литературы) // Клиническая лабораторная диагностика. - 2019. - Т.64. - №1. - С. 34−41. [Stepanova TV, Ivanov AN, Tereshkina NE, et al. Markers of endothelial dysfunction: pathogenetic role and diagnostic significance. Klinicheskaia laboratornaia diagnostika. 2019;64(1):34−41. (In Russ).]
↑8. Torimoto K, Okada Y, Tanaka Y. Type 2 diabetes and vascular endothelial dysfunction. J Uoeh. 2018;40(1):65-75. https://doi.org/10.7888/juoeh.40.65
↑9. Sena CM, Pereira AM, Seiça R. Endothelial dysfunction - a major mediator of diabetic vascular disease. Biochimica Biophysica Acta. 2013;1832:2216-2231.