ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 06.12.2023
Просмотров: 467
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.

228
КирикЛ. А. · «Усі уроки фізики. 9 клас»
-
Бета-розпад не змінює масового числа, а зарядове число збільшує на 1, тобто зміщує елемент на одну клітинку ближче до кінця періодичної системи. -
Сума зарядів (масових чисел) продуктів розпаду дорівнює заряду (масовому числу) вихідного ядра.
Домашнє завдання
-
Підр.: § 33. -
Зб.:
ріві — № 17.8; 17.9; 17.13; 17.14.
рів2 — № 17.19; 17.21; 17.23; 17.25, 17.26.
рівЗ — № 17.30, 17.31; 17.32; 17.33; 17.34.
-
Д.: підготуватися до самостійної роботи № 15.
Задачі із самостійної роботи № 15 «Будова атома. Атомне ядро»
Середній рівень
-
У ядрі атома Цинку 65 частинок, з них 30 протонів. Скільки нейтронів у ядрі й скільки електронів обертається навколо ядра цього атома? -
Який склад ядра атома Алюмінію ? Достатній рівень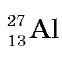
-
Ядро атома й електрони мають різні знаки зарядів, отже, притягуються один до одного. Чому ж електрони не падають на ядра атомів? -
Розташуйте перераховані нижче атомні ядра: а) по мірі збільшення масового числа; б) по мірі збільшення заряду ядра; в) по мірі збільшення числа нейтронів у них.
54Mn, 192Ir, 35S, 59Fe, 134Cs, 152Eu.
Високий рівень
-
Яким числом — зарядовим чи масовим — визначаються хімічні властивості елемента? Чим це пояснюється? -
З огляду на співвідношення розмірів ядра й електронної оболонки, атом часто називають «ажурним». Що більш ажурне — Сонячна система чи атом?

ВИВЧЕННЯ НОВОГО МАТЕРІАЛУ
-
Причини радіоактивного розпаду
Було встановлено, що під час радіоактивного випромінювання реалізується мрія алхіміків: випромінювання супроводжується перетворенням одних хімічних елементів на інші.
Намагаючись пояснити явища, що спостерігаються, Е. Резерфорд і його співробітник Ф. Содді висунули гіпотезу, відповідно до якої причиною радіоактивного випромінювання є мимовільний розпад атомів.
З гіпотези Резерфорда й Содді випливало, що кожен атом радіоактивної речовини — це «сховище» енергії. Під час розпаду атома частина енергії зі «сховища» несеться α- і β
-частками і γ-променями, а енергія, що залишилася, зберігається в новому атомі, що утворився в результаті розпаду. Стало очевидним, що енергія, що вивільнюється під час радіоактивного розпаду, міститься не просто в атомах, а в атомних ядрах.
-
Період напіврозпаду
Резерфорд, досліджуючи перетворення радіоактивних речовин, установив дослідним шляхом, що їхня активність зменшується з часом. Так, активність радону зменшується вдвічі вже за 1 хв.
Для кожної радіоактивної речовини існує визначений інтервал часу, протягом якого активність зменшується вдвічі.

КирикЛ. А. · «Усі уроки фізики. 9 клас»
^ Період напіврозпаду Т — це час, протягом якого розпадається половина наявного числа радіоактивних атомів. Наприклад, для ядра
ко 1600 років. Отже, якщо взяти 1 г радію, то через 1600 років його буде 0,5 г, а через 3200 років — 0,25 г. Таким чином, вихідна кількість радію повинна перетворитися на нуль через нескінченний проміжок часу.
У різних речовин період напіврозпаду дуже різний: від мільйонних часток секунди до мільярдів років. Чим менше період напіврозпаду, тим активніше протікає розпад.
| Радіоактивна речовина | Період напіврозпаду | Радіоактивна речовина | Період напіврозпаду |
| Полоній | 3 · 10-7 с | Стронцій | 27 років |
| Радон | 52 с | Радій | 1622 роки |
| Каліфорній | 55 діб | Уран | 4,5 · 109 років |
| Кобальт | 5,26 року | Торій | 1,4 · 1010 років |
З таблиці видно, що активність полонію зменшується вдвічі майже миттєво, стронцію — за 27 років, а активність радію, урану і торію не змінюється протягом людського життя.
3. Закон радіоактивного розпаду
Нехай число радіоактивних атомів у початковий момент часу (t =0) дорівнює N0. Через час t1= Т число ядер, що не розпалися,
дорівнює
ких ядер виявиться
ку часу t = nT ядер, що не розпалися, залишиться

Ядерна фізика. Атомне ядро. Ядерна енергетика
За цією формулою знаходять число атомів, що не розпалися, у будь-який момент часу. Період напіврозпаду — стала величина, що не може бути змінена такими доступними впливами, як охолодження, нагрівання, тиск тощо.
Закон розпаду атомів не є законом, що керує розпадом одного атома, тому що не можна вгадати, коли відбудеться цей розпад.
Розпад атома не залежить від його віку, тобто атоми «не старіють».
Розпад будь-якого атомного ядра — це, так би мовити, не «смерть від старості», а «нещасливий випадок» у його житті. Для радіоактивних атомів не існує поняття віку. Можна визначити лише середню тривалість життя τ.
Середня тривалість життя — це просто середнє арифметичне тривалості життя досить великої кількості атомів даного виду. Передбачити, коли відбудеться розпад даного атома, неможливо. Закон радіоактивного розпаду визначає середнє число атомів, що розпадаються за певний інтервал часу. Закон радіоактивного розпаду є статистичним законом.
Питання до учнів у ході викладу нового матеріалу
? Чим відрізняються радіоактивні атоми від нерадіоактив-них?
? Яка причина радіоактивного розпаду? ? Що розуміють під періодом напіврозпаду? ? Чи існує вік у радіоактивних атомів?
ЗАКРІПЛЕННЯ ВИВЧЕНОГО МАТЕРІАЛУ
1. Якісні питання
-
Чому не визначають час повного розпаду всіх ядер? -
Чи правильним є твердження, що чим довше існує атом, тим більше ймовірність його розпаду? -
Лічильник реєструє β-частки радіоактивного препарату. Чи спрацьовує лічильник через однакові інтервали часу?

232
КирикЛ. А. · «Усі уроки фізики. 9 клас»
2. Навчаємося розв'язувати задачі
-
Дві різні речовини містять однакове число N радіоактивних атомів. Період напіврозпаду першої з них 1 рік, другої — 4 роки. Яка з речовин більш активна? -
Існує певна кількість радіоактивного ізотопу срібла. Маса радіоактивного срібла зменшилася у 8 разів за 810 діб. Визначте період напіврозпаду радіоактивного срібла.
Розв'язання:
Тоді
-
Скільки за масою радіоактивної речовини залишиться через три доби, якщо спочатку її було 100 г? Період напіврозпаду речовини дорівнює дві доби. (Відповідь: 35,4 г.)
Що ми дізналися на уроці
? Період напіврозпаду Т — це час, протягом якого розпадається
половина наявного числа радіоактивних атомів. ? Закон радіоактивного розпаду:
? Розпад атома не залежить від його віку, тобто атоми «не старіють».
Домашнє завдання
-
Підр.: § 33, конспект уроку. -
Зб.:
ріві — № 17.20; 17.21; 17.22; 17.23; 17.24. рів2 — № 17.25; 17.35; 17.36; 17.37, 17.38. рівЗ — № 17.40, 17.41; 17.42; 17.44; 17.45.
Урок 5/52
Тема. Експериментальне вивчення структури атома
Мета уроку: дати учням знання про будову атома, ознайомити їх із
планетарною моделлю атома по Резерфорду. Тип уроку: урок вивчення нового матеріалу.
План уроку
| Контроль знань | 5 хв | 1. Яка причина радіоактивного розпаду? 2. Що розуміють під періодом напіврозпаду? 3. Закон радіоактивного розпаду |
| Демонстрації | 6 хв | 1. Таблиці зі схемою досліду Резерфорда і схе- мою планетарної моделі атома. 2. Відеофільм «Дослід Резерфорда» |
| Вивчення нового матеріалу | 28 хв | 1. Модель атома Томсона. 2. Досліди Резерфорда. 3. Ядерна модель атома Резерфорда. 4. Ядерні перетворення |
| Закріплення вивченого матеріалу | 6 хв | 1. Контрольні питання. 2. Навчаємося розв'язувати задачі |
ВИВЧЕННЯ НОВОГО МАТЕРІАЛУ
1. Модель атома Томсона
До 1902 р. було проведено достатньо експериментів, що переконливо довели, що електрон є однією з основних складових частин будь-якої речовини.
Джозеф Джон Томсон показав на основі класичної електромагнітної теорії, що розміри електрона повинні бути порядка 10-15 м. Крім того, було відомо, що розміри атомів дорівнюють кільком ангстремам (один ангстрем дорівнює 10-10 м). На цій підставі Томсон 1903 р. запропонував модель атома, відповідно до якої атоми являють собою однорідні кулі з позитивно зарядженої речовини, у якій знаходяться електрони. Сумарний заряд електронів дорівнює позитивному заряду атома. Тому атом у цілому електрично нейтральний.
Ця модель одержала назву «пудинг», тому що електрони були вкраплені в позитивно заряджене середовище, як родзинки в пудингу.
Відхилення електрона в атомі від положення рівноваги призводить до виникнення повертальної сили. Тому електрон, виведений певним чином з положення рівноваги, здійснює коливання, а тому є джерелом електромагнітного випромінювання.