ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 09.12.2023
Просмотров: 309
Скачиваний: 4
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Проводниковый аппарат боли
Нервные проводники, подкорковые образования и кора головного мозга являются главными элементами, которые вовлечены в передачу болевых импульсов и формирование ощущения боли. Нейроны трёх уровней вовлечены в проведение болевой чувствительности. Нейрон 1-го уровня лежит в спинномозговых ганглиях (узлах), 2-го уровня – в задних рогах спинного мозга, 3-го уровня – в таламусе (зрительных буграх).
В спинном мозге принято выделять 9 слоёв или пластин. I пластина носит название маргинальной, II и III пластины образуют желатинозную субстанцию или студенистое вещество (SG), IV-VI – собственное ядро, VII-VIII – промежуточное ядро, IX пластина представлена двигательной частью с моторными клетками переднего рога спинного мозга.
Ноцицептивная информация поступает в задние рога спинного мозга, а затем передаётся в ЦНС по лемнисковой и экстралемнисковой восходящим афферентным системам. В пределах спинного мозга одна из них располагается в дорсальной и дорсолатеральной зоне белого вещества, другая – в его вентролатеральной части.
Вентролатеральная система представлена спиноталамическим, спиноретикулярным и спиномезенцефалическим трактами. Спиноталамический тракт является важным восходящим путем, существующим для передачи широкого спектра информации о свойствах болевого стимула, и обозначается как неоспиноталамический. Два других тракта объединяются в палеоспиноталамический тракт, нейроны которого представлены в маргинальной зоне и более глубоких пластинах заднего рога, а также в промежуточной области и вентральном роге всех сегментов спинного мозга.
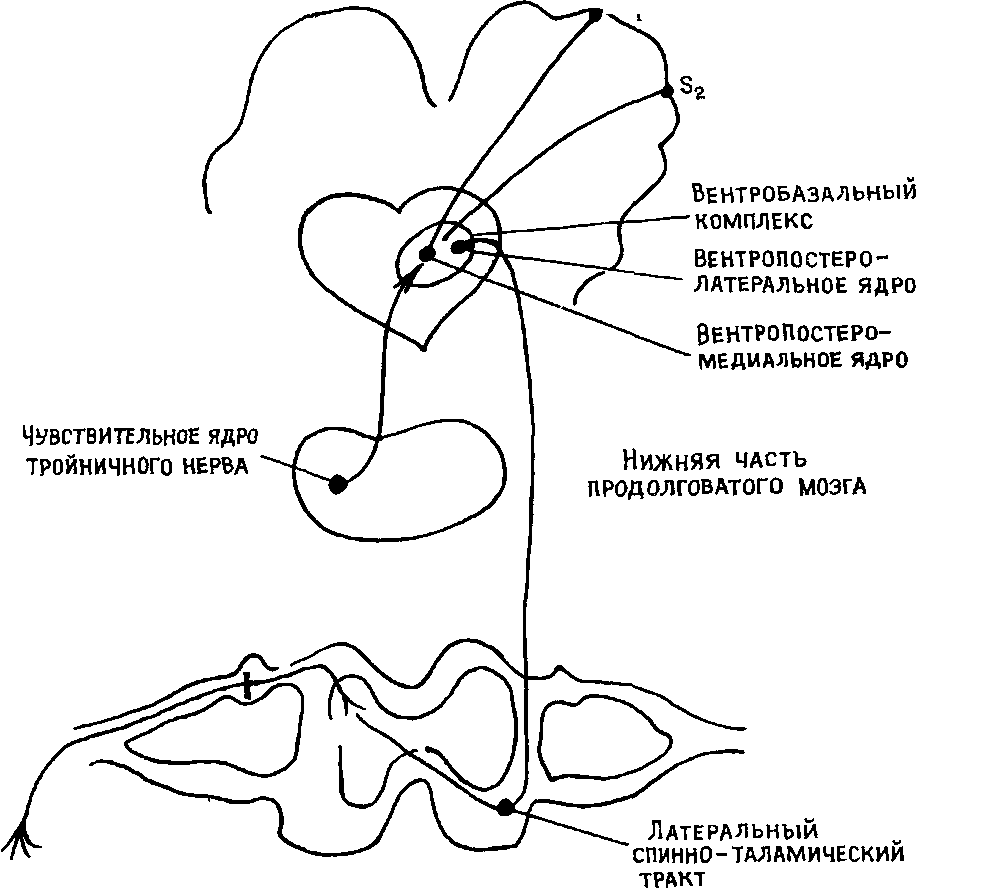
Рис. 5. Неоспиноталамический тракт (Овсянников В.Г., 1990).
Нейроны спиноталамического тракта подразделяются на четыре группы: первая – нейроны широкого динамического диапазона (мультирецептивные); вторая – высокопороговые нейроны (ноцицептивно-специфические); третья – низкопороговые; четвертая – глубокие нейроны, активирующиеся различными проприорецептивными раздражениями. Терминали нейронов спиноталамического тракта оканчиваются в специфических (релейных) ядрах таламуса (вентропостериолатеральное ядро – VPL), а также в диффузно-ассоциативных (медиальная часть заднего комплекса) и неспецифических ядрах (интраламинарный комплекс – субмедиальное ядро). Большинство нейронов, оканчивающихся в специфических ядрах, сконцентрированы в I и IV пластинах. При этом, нейроны, чьи терминали оканчиваются в неспецифических ядрах, в частности в центролатеральном ядре (CL), сконцентрированы преимущественно в VI-VIII пластинах. Кроме того, определенное число аксонов, направляющихся в VPL из I и V пластин, отдает коллатерали в CL, а также к нейронам медиальной ретикулярной формации и центрального серого околоводопроводного вещества (ЦСОВ).
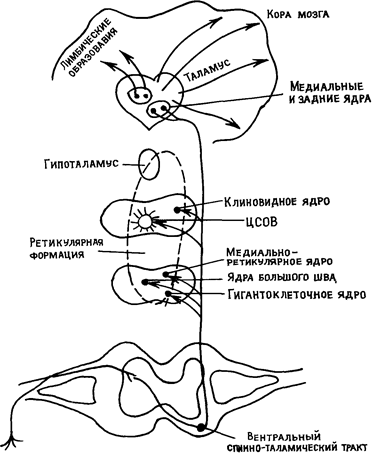
Рис. 6. Палеоспиноталамический тракт (Овсянников В.Г., 1990).
Большинство терминалей висцеральных ноцицептивных афферентных волокон оканчивается на мультирецепторных нейронах спиноталамического тракта, получающих также информацию от соматических ноцицептивных афферентов, что позволяет рассматривать их как важную афферентную ноцицептивную систему, способную передавать сигналы, вызванные действием механических стимулов с широким диапазоном энергии.
Значительный объем ноцицептивной информации поступает в ствол мозга через те аксоны спиноретикулярного тракта, нейроны которых лежат в VII-VIII пластинах и терминали которых распределены в медиальной ретикулярной формации продолговатого мозга, а также в релейных ядрах таламуса.
Аксоны и тела нейронов, лежащие вместе с нейронами спиноталамического тракта и сопровождающие их до перешейка среднего мозга, образуют спиномезенцефалический тракт. Важно отметить, что терминали спиномезенцефалического тракта распределяются среди интегративных структур ЦНС, которые формируют рефлексы ориентации (верхние бугорки крыши среднего мозга, ретикулярное клиноформное ядро) и управляют вегетативными реакциями (ядра Даркшевича и Эдингера-Вестфаля), а также структур ЦНС, таких как латеральная область ЦСОВ, участвующих в появлении аверсивных (вызывающих неприязнь) ответов. Коллатерали аксонов спиномезенцефалического тракта также оканчиваются на вентробазальных и медиальных ядрах таламуса. Считается, что таким способом могут быть инициированы сложные соматические и висцеральные антиноцицептивные рефлексы.
Спиноцервикоталамический тракт образован преимущественно низкопороговыми и мультирецептивными нейронами, которые сконцентрированы в III, IV и V пластинах серого вещества. Стимуляция этих нейронов, переключаясь на нейроны латерального цервикального ядра, затем в составе медиального лемниска достигает VPL и несет информацию о действии механических неболевых и термических стимулах. Миелинизированные афферентные волокна задних корешков, несущие информацию от кожи, сухожилий, мышц и внутренних органов формируют дорсальные тракты. Эти волокна без перерыва в сером веществе спинного мозга в задних столбах достигают нижнего и клиновидного ядер. Вторичные проекции от задних ядер столбов через медиальную петлю оканчиваются в задневентральном ядре тадамуса, а оттуда проецируются в соматосенсорные зоны коры. Вместе с тем, порция коллатералей волокон задних корешков оканчивается на нейронах III-IV пластин заднего рога спинного мозга. Двигательные волокна этих нейронов формируют так называемый постсинаптический дорсальный тракт, который также оканчивается в нижнем и клиновидном ядрах.
Тактильные низкопороговые миелинизированные волокна оканчиваются на уровне IV-V пластин заднего рога и дают большое количество коллатералей к желатинозной субстанции. Это обстоятельство объясняет уменьшение болевых ощущений при механическом растирании, электрораздражении кожи, акупунктуре и др. Такие импульсы тормозят выделение вещества Р (одного из медиаторов боли) и усиливают образование антиноцицептивных эндогенных опиатов (энкефалинов). Это явление легло в основу теории «воротного контроля» боли.
Соматический нерв состоит из преимущественно миелинизированных и немиелинизированных волокон. Толстые миелинизированные волокна относятся к группе А, тонкие немиелинизированные – к группе С. Быстро способны проводить импульсы тактильной и глубокой чувствительности волокна группы А, которые подразделяются на α (альфа), β (бета), γ (гамма) и δ (дельта). При этом, не вызывает сомнений, что болевые импульсы проводятся только по тонким миелинизированным Аδ и безмиелиновым С-волокнам.
В задних (дорсальных) рогах серого вещества спинного мозга находятся клетки размером 5-25 мкм, на которых оканчиваются эти проводники болевых импульсов. Таким образом, волокна нейронов спинальных ганглиев подразделяются на:
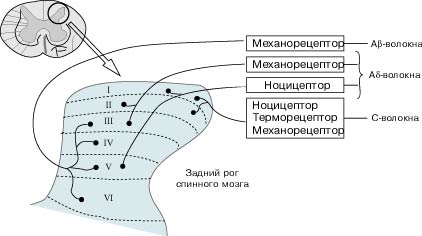
Рис. 7. Локализация окончаний чувствительных волокон в столбах заднего рога спинного мозга (Ивашкин В.Т., Шульпекова Ю.О., 2002).
1) тонкие миелинизированные А-дельта (Аδ) волокна – диаметр 1-4 мкм, скорость проведения возбуждения 5-30 м/с;
2) безмиелиновые С-волокна – диаметр менее 1 мкм, скорость проведения возбуждения – 0,5-2 м/с.
Большинство афферентных импульсов поступает по задним корешкам спинного мозга и по чувствительным черепным нервам. При этом в заднем корешке число немиелинизированных волокон в 2 раза превышает количество миелинизированных афферентов. Через передний корешок в спинной мозг входит около 20-30% болевых волокон, также в основном являющихся безмиелиновыми.
Центральный аппарат системы боли
Одной из главных супрасегментарных зон восприятия афферентного притока и его переработки является ретикулярная формация головного мозга. Эта область продолговатого мозга, получающая афферентную информацию по спиноретикулярному тракту, в свою очередь посылает диффузные восходящие проекции в ростральные отделы мозга, в частности, проекции от нейронов бульбарной ретикулярной формации к ядрам медиального таламуса. Эти проекции носят название бульботаламический тракт. Помимо проекции к ядрам медиального таламуса ретикулярная формация посылает свои проекции к ЦСОВ, к верхним буграм четверохолмия, к гипоталамусу и другим структурам. ЦСОВ представляет собой образование, в котором происходит интеграция ответов на многие повреждающие стимулы. Известно, что гипоталамус участвует в организации сенсорных защитных реакций, большое значение в которых играют его тесные связи, установленные с ЦСОВ. Ноцицептивные нейроны встречаются также в гипоталамусе, ядрах шва, синем пятне, черной субстанции и других подкорковых образованиях.
Таким образом, ноцицептивная информация поступает по диффузным восходящим проекциям в различные образования мозга, которые обеспечивают самые разнообразные функции чувствительного, двигательного и вегетативного обеспечения защитных реакций.
В таламусе принято выделять три основных комплекса ядер, которые самым непосредственным образом вовлечены в восприятие и интерпретацию боли: вентробазальный комплекс, задняя группа ядер, медиальные и интраламинарные ядра.
Вентробазальный комплекс является главной структурой соматосенсорной системы. Восходящие лемнисковые проекции оканчиваются на нейронах этого комплекса, а неоспиноталамический тракт – в ограниченных зонах VPL. Нейроны вентробазального комплекса проецируются в соматосенсорные зоны коры (S2–S1) и частично – в орбитальную кору. Мультисенсорная конвергенция на нейронах вентробазального комплекса обеспечивает точную соматотопическую информацию о локализации боли, ее пространственную соотнесенность и сенсорно-дискриминативный анализ.
Задняя группа ядер таламуса характеризуется наличием на них конвергенции полисенсорных входов из спиноталамических, спиноцервикальных и лемнискового трактов. Кроме того, на нейронах этих ядер оканчиваются спиноретикулярные и спиномезенцефалоталамические проекции. Задняя группа таламических ядер имеет многоканальные проекции в кору, и в том числе в заднюю часть ее соматосенсорной области (S1, S2). Задняя группа ядер вместе с вентробазальным комплексом участвуют в передаче и интерпретации информации о локализации болевого воздействия и частично – в формировании мотивационно-аффективных компонентов боли. Общие анестетики способны сильно подавлять нейрональную активность этих ядер.
Волокна спиноталамического тракта и все ноцицептивные восходящие тракты оканчиваются на медиальных и интраламинарных ядрах, к которым относят ассоциативное медиодорсальное ядро и неспецифические интраламинарные ядра (центральное медиальное, центральное латеральное, парацентральное, парафасцикулярное и срединный центр). Нейроны этих ядер способны отвечать на соматические, висцеральные, слуховые, зрительные и болевые стимулы. Медиальные и интраламинарные ядра таламуса играют решающую роль в формировании восприятия «вторичной», поздней, протопатической боли. Эти ядра получают кроме ноцицептивной информации также обширные афферентные входы из гипоталамуса, лимбической, стриопаллидарной систем, ЦСОВ, и широко представлены в субкортикальных и корковых проекциях. Кроме того, медиальные и интраламинарные ядра формируют сложные вегетомоторные высокоинтегрированные защитные реакции на болевое воздействие, а также мотивационно-поведенческие ноцицептивные проявления и их аффективное, дискомфортное восприятие.
Конечный этап анализа болевых ощущений происходит в коре головного мозга, которая принимает участие, как в восприятии (перцепции) боли, так и в механизмах её формирования.
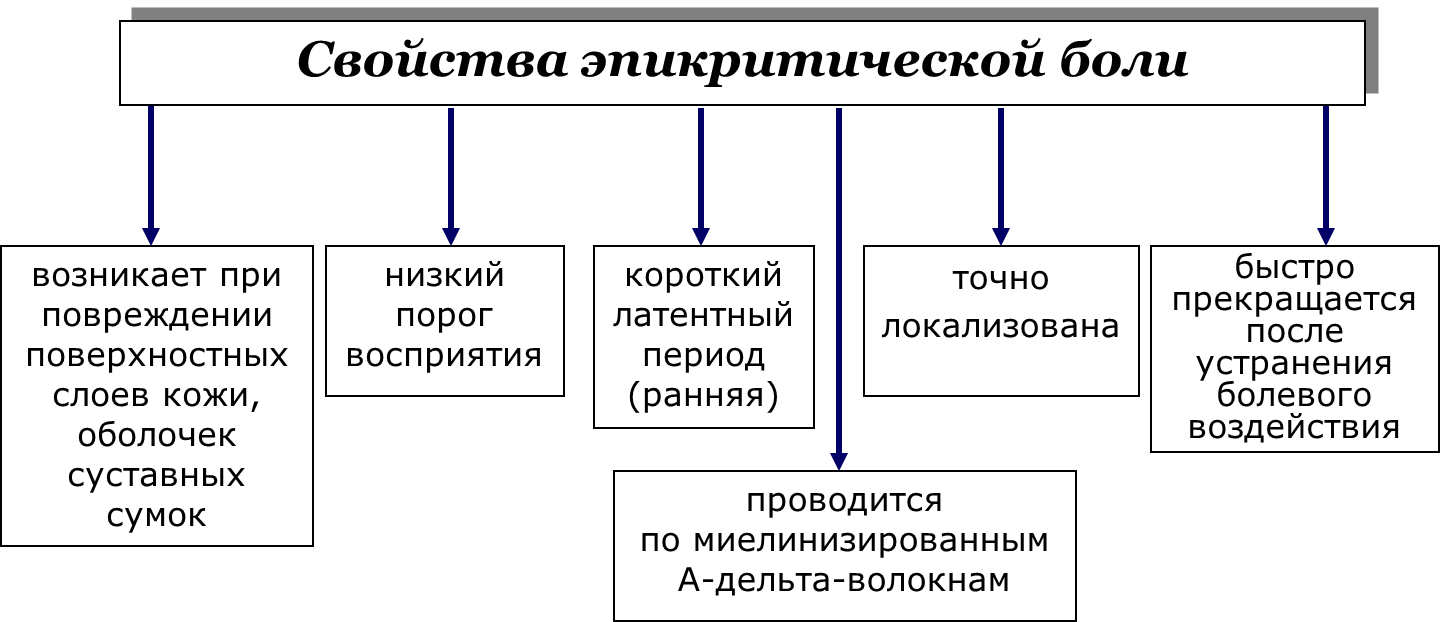
Рис. 8. Характеристики поверхностной эпикритической (ранней) боли.
Непосредственное участие в патогенезе перцептуально-дискриминативного компонента системной ноцицептивной реакции принимает первая соматосенсорная зона коры (S1). Экспериментально доказано, что её удаление может способствовать повышению порогов восприятия боли.
Ведущую роль в механизмах формирования адекватных защитных реакций организма в ответ на болевое раздражение играет вторая соматосенсорная область коры, ее удаление, напротив, приводит к снижению порогов восприятия. Орбитофронтальная область коры также непосредственно участвует в механизмах формирования эмоционально-аффективного компонента системной болевой реакции организма, ее удаление не изменяет порогов восприятия перцептуально-дискриминативного компонента и значительно повышает пороги восприятия эмоционально-аффективного компонента боли.
Таким образом, данные литературы свидетельствуют о разделении болевой чувствительности на эпикритическую и протопатическую. Следует отметить, что эпикритическая боль – это, в большинстве случаев, соматическая, а протопатическая – висцеральная.
Эпикритическая боль возникает при стимуляции преимущественно быстропроводящих миелинизированных тонких Аδ-волокон. Ноцицептивная информация в этом случае передается в основном по неоспиноталамическому тракту и частично – по системе дорсолатеральных и дорсальных лемнисковых проекций. Через вентролатеральный отдел таламуса она достигает в основном соматосенсорной коры. Благодаря быстрой передаче информации через эту систему обеспечивается точная локализация боли, ее сенсорная дискриминация, оценка длительности и интенсивности ноцицептивного стимула.
Протопатическая боль, как правило, вторична. Она в значительной степени обусловлена проведением по медленным немиелинизированным ноцицептивным С-афферентам информации, которая затем передается по палеоспиноталамическим восходящим системам (спиноретикулоталамическому, спиномезенцефалоталамическому трактам и по другим подразделениям этих диффузных проекций), а также по проприоспинальной системе. Ноцицептивные сигналы по мере их рострального проведения активируют целый ряд супрасегментарных структур – ретикулярную формацию, гипоталамус, лимбическую и стриопаллидарную системы. Ноцицептивный поток преимущественно через медиальные, интраламинарные и задние ядра таламуса достигает различных областей коры головного мозга. Вся эта сложноорганизованная иерархия восходящих проекций и структур головного мозга обусловливает труднодифференцируемое по качеству и локализации ноцицептивное ощущение, его многокомпонентные висцеромоторные и эмоционально-аффективные проявления, а также психическое переживание боли.
Нервные проводники, подкорковые образования и кора головного мозга являются главными элементами, которые вовлечены в передачу болевых импульсов и формирование ощущения боли. Нейроны трёх уровней вовлечены в проведение болевой чувствительности. Нейрон 1-го уровня лежит в спинномозговых ганглиях (узлах), 2-го уровня – в задних рогах спинного мозга, 3-го уровня – в таламусе (зрительных буграх).
В спинном мозге принято выделять 9 слоёв или пластин. I пластина носит название маргинальной, II и III пластины образуют желатинозную субстанцию или студенистое вещество (SG), IV-VI – собственное ядро, VII-VIII – промежуточное ядро, IX пластина представлена двигательной частью с моторными клетками переднего рога спинного мозга.
Ноцицептивная информация поступает в задние рога спинного мозга, а затем передаётся в ЦНС по лемнисковой и экстралемнисковой восходящим афферентным системам. В пределах спинного мозга одна из них располагается в дорсальной и дорсолатеральной зоне белого вещества, другая – в его вентролатеральной части.
Вентролатеральная система представлена спиноталамическим, спиноретикулярным и спиномезенцефалическим трактами. Спиноталамический тракт является важным восходящим путем, существующим для передачи широкого спектра информации о свойствах болевого стимула, и обозначается как неоспиноталамический. Два других тракта объединяются в палеоспиноталамический тракт, нейроны которого представлены в маргинальной зоне и более глубоких пластинах заднего рога, а также в промежуточной области и вентральном роге всех сегментов спинного мозга.

Рис. 5. Неоспиноталамический тракт (Овсянников В.Г., 1990).
Нейроны спиноталамического тракта подразделяются на четыре группы: первая – нейроны широкого динамического диапазона (мультирецептивные); вторая – высокопороговые нейроны (ноцицептивно-специфические); третья – низкопороговые; четвертая – глубокие нейроны, активирующиеся различными проприорецептивными раздражениями. Терминали нейронов спиноталамического тракта оканчиваются в специфических (релейных) ядрах таламуса (вентропостериолатеральное ядро – VPL), а также в диффузно-ассоциативных (медиальная часть заднего комплекса) и неспецифических ядрах (интраламинарный комплекс – субмедиальное ядро). Большинство нейронов, оканчивающихся в специфических ядрах, сконцентрированы в I и IV пластинах. При этом, нейроны, чьи терминали оканчиваются в неспецифических ядрах, в частности в центролатеральном ядре (CL), сконцентрированы преимущественно в VI-VIII пластинах. Кроме того, определенное число аксонов, направляющихся в VPL из I и V пластин, отдает коллатерали в CL, а также к нейронам медиальной ретикулярной формации и центрального серого околоводопроводного вещества (ЦСОВ).

Рис. 6. Палеоспиноталамический тракт (Овсянников В.Г., 1990).
Большинство терминалей висцеральных ноцицептивных афферентных волокон оканчивается на мультирецепторных нейронах спиноталамического тракта, получающих также информацию от соматических ноцицептивных афферентов, что позволяет рассматривать их как важную афферентную ноцицептивную систему, способную передавать сигналы, вызванные действием механических стимулов с широким диапазоном энергии.
Значительный объем ноцицептивной информации поступает в ствол мозга через те аксоны спиноретикулярного тракта, нейроны которых лежат в VII-VIII пластинах и терминали которых распределены в медиальной ретикулярной формации продолговатого мозга, а также в релейных ядрах таламуса.
Аксоны и тела нейронов, лежащие вместе с нейронами спиноталамического тракта и сопровождающие их до перешейка среднего мозга, образуют спиномезенцефалический тракт. Важно отметить, что терминали спиномезенцефалического тракта распределяются среди интегративных структур ЦНС, которые формируют рефлексы ориентации (верхние бугорки крыши среднего мозга, ретикулярное клиноформное ядро) и управляют вегетативными реакциями (ядра Даркшевича и Эдингера-Вестфаля), а также структур ЦНС, таких как латеральная область ЦСОВ, участвующих в появлении аверсивных (вызывающих неприязнь) ответов. Коллатерали аксонов спиномезенцефалического тракта также оканчиваются на вентробазальных и медиальных ядрах таламуса. Считается, что таким способом могут быть инициированы сложные соматические и висцеральные антиноцицептивные рефлексы.
Спиноцервикоталамический тракт образован преимущественно низкопороговыми и мультирецептивными нейронами, которые сконцентрированы в III, IV и V пластинах серого вещества. Стимуляция этих нейронов, переключаясь на нейроны латерального цервикального ядра, затем в составе медиального лемниска достигает VPL и несет информацию о действии механических неболевых и термических стимулах. Миелинизированные афферентные волокна задних корешков, несущие информацию от кожи, сухожилий, мышц и внутренних органов формируют дорсальные тракты. Эти волокна без перерыва в сером веществе спинного мозга в задних столбах достигают нижнего и клиновидного ядер. Вторичные проекции от задних ядер столбов через медиальную петлю оканчиваются в задневентральном ядре тадамуса, а оттуда проецируются в соматосенсорные зоны коры. Вместе с тем, порция коллатералей волокон задних корешков оканчивается на нейронах III-IV пластин заднего рога спинного мозга. Двигательные волокна этих нейронов формируют так называемый постсинаптический дорсальный тракт, который также оканчивается в нижнем и клиновидном ядрах.
Тактильные низкопороговые миелинизированные волокна оканчиваются на уровне IV-V пластин заднего рога и дают большое количество коллатералей к желатинозной субстанции. Это обстоятельство объясняет уменьшение болевых ощущений при механическом растирании, электрораздражении кожи, акупунктуре и др. Такие импульсы тормозят выделение вещества Р (одного из медиаторов боли) и усиливают образование антиноцицептивных эндогенных опиатов (энкефалинов). Это явление легло в основу теории «воротного контроля» боли.
Соматический нерв состоит из преимущественно миелинизированных и немиелинизированных волокон. Толстые миелинизированные волокна относятся к группе А, тонкие немиелинизированные – к группе С. Быстро способны проводить импульсы тактильной и глубокой чувствительности волокна группы А, которые подразделяются на α (альфа), β (бета), γ (гамма) и δ (дельта). При этом, не вызывает сомнений, что болевые импульсы проводятся только по тонким миелинизированным Аδ и безмиелиновым С-волокнам.
В задних (дорсальных) рогах серого вещества спинного мозга находятся клетки размером 5-25 мкм, на которых оканчиваются эти проводники болевых импульсов. Таким образом, волокна нейронов спинальных ганглиев подразделяются на:

Рис. 7. Локализация окончаний чувствительных волокон в столбах заднего рога спинного мозга (Ивашкин В.Т., Шульпекова Ю.О., 2002).
1) тонкие миелинизированные А-дельта (Аδ) волокна – диаметр 1-4 мкм, скорость проведения возбуждения 5-30 м/с;
2) безмиелиновые С-волокна – диаметр менее 1 мкм, скорость проведения возбуждения – 0,5-2 м/с.
Большинство афферентных импульсов поступает по задним корешкам спинного мозга и по чувствительным черепным нервам. При этом в заднем корешке число немиелинизированных волокон в 2 раза превышает количество миелинизированных афферентов. Через передний корешок в спинной мозг входит около 20-30% болевых волокон, также в основном являющихся безмиелиновыми.
Центральный аппарат системы боли
Одной из главных супрасегментарных зон восприятия афферентного притока и его переработки является ретикулярная формация головного мозга. Эта область продолговатого мозга, получающая афферентную информацию по спиноретикулярному тракту, в свою очередь посылает диффузные восходящие проекции в ростральные отделы мозга, в частности, проекции от нейронов бульбарной ретикулярной формации к ядрам медиального таламуса. Эти проекции носят название бульботаламический тракт. Помимо проекции к ядрам медиального таламуса ретикулярная формация посылает свои проекции к ЦСОВ, к верхним буграм четверохолмия, к гипоталамусу и другим структурам. ЦСОВ представляет собой образование, в котором происходит интеграция ответов на многие повреждающие стимулы. Известно, что гипоталамус участвует в организации сенсорных защитных реакций, большое значение в которых играют его тесные связи, установленные с ЦСОВ. Ноцицептивные нейроны встречаются также в гипоталамусе, ядрах шва, синем пятне, черной субстанции и других подкорковых образованиях.
Таким образом, ноцицептивная информация поступает по диффузным восходящим проекциям в различные образования мозга, которые обеспечивают самые разнообразные функции чувствительного, двигательного и вегетативного обеспечения защитных реакций.
В таламусе принято выделять три основных комплекса ядер, которые самым непосредственным образом вовлечены в восприятие и интерпретацию боли: вентробазальный комплекс, задняя группа ядер, медиальные и интраламинарные ядра.
Вентробазальный комплекс является главной структурой соматосенсорной системы. Восходящие лемнисковые проекции оканчиваются на нейронах этого комплекса, а неоспиноталамический тракт – в ограниченных зонах VPL. Нейроны вентробазального комплекса проецируются в соматосенсорные зоны коры (S2–S1) и частично – в орбитальную кору. Мультисенсорная конвергенция на нейронах вентробазального комплекса обеспечивает точную соматотопическую информацию о локализации боли, ее пространственную соотнесенность и сенсорно-дискриминативный анализ.
Задняя группа ядер таламуса характеризуется наличием на них конвергенции полисенсорных входов из спиноталамических, спиноцервикальных и лемнискового трактов. Кроме того, на нейронах этих ядер оканчиваются спиноретикулярные и спиномезенцефалоталамические проекции. Задняя группа таламических ядер имеет многоканальные проекции в кору, и в том числе в заднюю часть ее соматосенсорной области (S1, S2). Задняя группа ядер вместе с вентробазальным комплексом участвуют в передаче и интерпретации информации о локализации болевого воздействия и частично – в формировании мотивационно-аффективных компонентов боли. Общие анестетики способны сильно подавлять нейрональную активность этих ядер.
Волокна спиноталамического тракта и все ноцицептивные восходящие тракты оканчиваются на медиальных и интраламинарных ядрах, к которым относят ассоциативное медиодорсальное ядро и неспецифические интраламинарные ядра (центральное медиальное, центральное латеральное, парацентральное, парафасцикулярное и срединный центр). Нейроны этих ядер способны отвечать на соматические, висцеральные, слуховые, зрительные и болевые стимулы. Медиальные и интраламинарные ядра таламуса играют решающую роль в формировании восприятия «вторичной», поздней, протопатической боли. Эти ядра получают кроме ноцицептивной информации также обширные афферентные входы из гипоталамуса, лимбической, стриопаллидарной систем, ЦСОВ, и широко представлены в субкортикальных и корковых проекциях. Кроме того, медиальные и интраламинарные ядра формируют сложные вегетомоторные высокоинтегрированные защитные реакции на болевое воздействие, а также мотивационно-поведенческие ноцицептивные проявления и их аффективное, дискомфортное восприятие.
Конечный этап анализа болевых ощущений происходит в коре головного мозга, которая принимает участие, как в восприятии (перцепции) боли, так и в механизмах её формирования.

Рис. 8. Характеристики поверхностной эпикритической (ранней) боли.
Непосредственное участие в патогенезе перцептуально-дискриминативного компонента системной ноцицептивной реакции принимает первая соматосенсорная зона коры (S1). Экспериментально доказано, что её удаление может способствовать повышению порогов восприятия боли.
Ведущую роль в механизмах формирования адекватных защитных реакций организма в ответ на болевое раздражение играет вторая соматосенсорная область коры, ее удаление, напротив, приводит к снижению порогов восприятия. Орбитофронтальная область коры также непосредственно участвует в механизмах формирования эмоционально-аффективного компонента системной болевой реакции организма, ее удаление не изменяет порогов восприятия перцептуально-дискриминативного компонента и значительно повышает пороги восприятия эмоционально-аффективного компонента боли.
Таким образом, данные литературы свидетельствуют о разделении болевой чувствительности на эпикритическую и протопатическую. Следует отметить, что эпикритическая боль – это, в большинстве случаев, соматическая, а протопатическая – висцеральная.
Эпикритическая боль возникает при стимуляции преимущественно быстропроводящих миелинизированных тонких Аδ-волокон. Ноцицептивная информация в этом случае передается в основном по неоспиноталамическому тракту и частично – по системе дорсолатеральных и дорсальных лемнисковых проекций. Через вентролатеральный отдел таламуса она достигает в основном соматосенсорной коры. Благодаря быстрой передаче информации через эту систему обеспечивается точная локализация боли, ее сенсорная дискриминация, оценка длительности и интенсивности ноцицептивного стимула.
Протопатическая боль, как правило, вторична. Она в значительной степени обусловлена проведением по медленным немиелинизированным ноцицептивным С-афферентам информации, которая затем передается по палеоспиноталамическим восходящим системам (спиноретикулоталамическому, спиномезенцефалоталамическому трактам и по другим подразделениям этих диффузных проекций), а также по проприоспинальной системе. Ноцицептивные сигналы по мере их рострального проведения активируют целый ряд супрасегментарных структур – ретикулярную формацию, гипоталамус, лимбическую и стриопаллидарную системы. Ноцицептивный поток преимущественно через медиальные, интраламинарные и задние ядра таламуса достигает различных областей коры головного мозга. Вся эта сложноорганизованная иерархия восходящих проекций и структур головного мозга обусловливает труднодифференцируемое по качеству и локализации ноцицептивное ощущение, его многокомпонентные висцеромоторные и эмоционально-аффективные проявления, а также психическое переживание боли.