ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 07.03.2019
Просмотров: 755
Скачиваний: 1
БОЛЕЗНИ ЖЕЛЕЗ ВНУТРЕННЕЙ СЕКРЕЦИИ.
Составила доцент Матвеенко М.Е.
Эндокринным заболеванием можно назвать такое, при котором
патология
эндокринной
железы
составляет
сущность
болезни.
Эндокринные заболевания обладают рядом особенностей:
1. Для них характерно плюригландулярное поражение, т.е. при
заболевании любой эндокринной железы к этому процессу
присоединяются патологические изменения в других эндокринных
железах, так как все органы эндокринной системы связаны между собой
функционально, и между ними существуют тесные заместительные
связи.
2. Эндокринные заболевания не бывают только эндокринными. Это
нейро-эндокринно-иммунные заболевания, т.к. синтез и секреция
гормонов регулируются нервной системой, либо непосредственно, либо
через выделение других гормонов и гуморальных факторов. В
гипоталамусе концентрируются нейроны, выделяющие в кровь
портальной системы гипофиза в ответ на приходящие извне импульсы
особые рилизинг-гормоны, стимулируя или тормозя выделение
гипофизарных гормонов. С иммунной системой эндокринная связана
через вилочковую железу. С другой стороны изменения иммунного
статуса, например, наличие аутоантител ведет в некоторых случаях к
недостаточности эндокринных желез.
3. Эндокринная система путем гормональной регуляции поддерживает
гомеостаз организма, поэтому при эндокринных заболеваниях
нарушается взаимосвязь между жировым, белковым, минеральным и
водным обменами. При этом в различных органах и тканях появляются
морфологические изменения, выражающиеся в дистрофических,
атрофических, гиперпластических, склеротических, диспластических и
неопластических
процессах.
В
самой
эндокринной
системе
преобладают
две
группы
патологических
процессов:
гиперпластические, которые выражаются, как правило, гиперфункцией,
и дистрофические, атрофические и склеротические, которые
выражаются гипофункцией желез внутренней секреции.
Болезни гипоталамуса и гипофиза.
Гипоталамус – высший вегетативный центр, координирующий
функции различных систем. Он представляет собой скопление нервных
клеток, которые трансформируют разнообразные нервные сигналы,
поступающие извне, в гуморальные путем выработки рилизинг-гормонов.
Гипоталамические гормоны могут активировать или угнетать выделение
тропных гормонов. При появлении в гипоталамусе патологических
процессов, таких как травматические повреждения, воспаление или
2
гамартом, нарушаются связи, регулирующие функцию гипофиза и других
эндокринных желез.
Гипофиз состоит из двух долей: передней (аденогипофиз) и задней
(нейрогипофиз).
Аденогипофиз
вырабатывает
тропные
гормоны,
воздействующие на эндокринные железы-мишени (щитовидную железу,
надпочечники, половые железы), а также гормоны, контролирующие рост
и лактацию. Врожденные пороки развития, такие как выраженная
гипоплазия или аплазия гипофиза, несовместимы с жизнью. Описанные в
литературе удвоения гипофиза сочетаются с тяжелыми пороками ЦНС.
Встречаются гипофизарные кисты, которые располагаются между
передней долей и средней частью гипофиза. При их значительном
увеличении гипофиз атрофируется, что сопровождается хронической
гипофизарной недостаточностью.
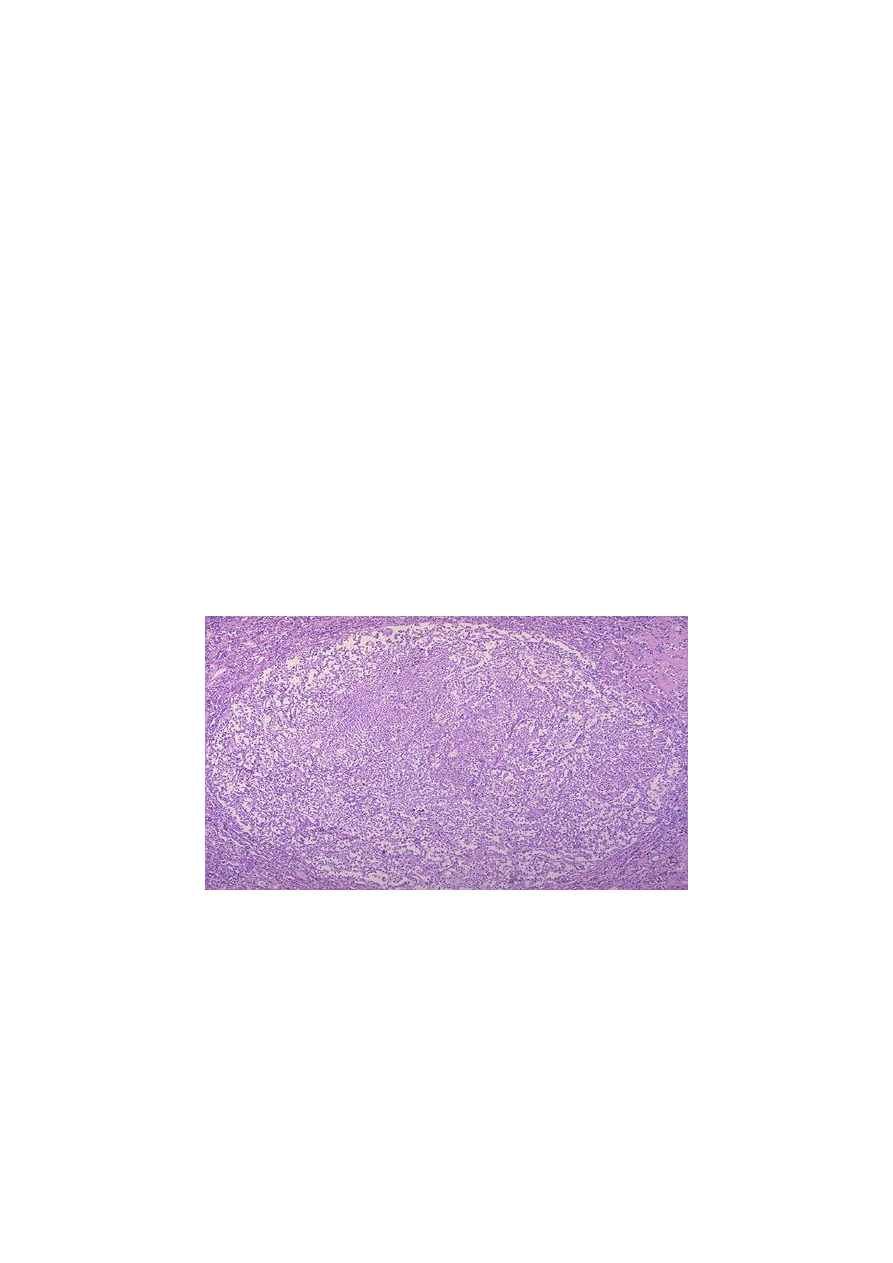
Из опухолей гипофиза наиболее важное место занимают аденомы,
которые часто встречаются у пожилых людей (рис.1). Аденомы почти
всегда вызывают гиперсекрецию тропных гормонов, т.е. являются
гормонально активными (соматотропная – из эозинофильных клеток
гипофиза, пролактинотропная – из хромофобных или эозинофильных
клеток и др.)(рис.2). Однако аденомы могут быть и гормонально
неактивными (мелкоклеточная недифференцированная и оксифильная
онкоцитома).
Рис.1 Микроаденома передней доли гипофиза: такая аденома встречается у
взрослых пациентов в 5% случаев. Редко бывает гормонально активной.
Аденомы могут озлокачествляться, приобретая инвазивный рост,
прорастая капсулу органа. Опухоли гипофиза, в том числе
доброкачественные, в случае значительного увеличения оказывают
давление на перекрест зрительных нервов, вызывая вначале сужение полей
зрения, а затем потерю зрения. Чаще всего аденомы вырабатывают
несколько гормонов одновременно, но возможна преимущественная
продукция одного гормона.
3
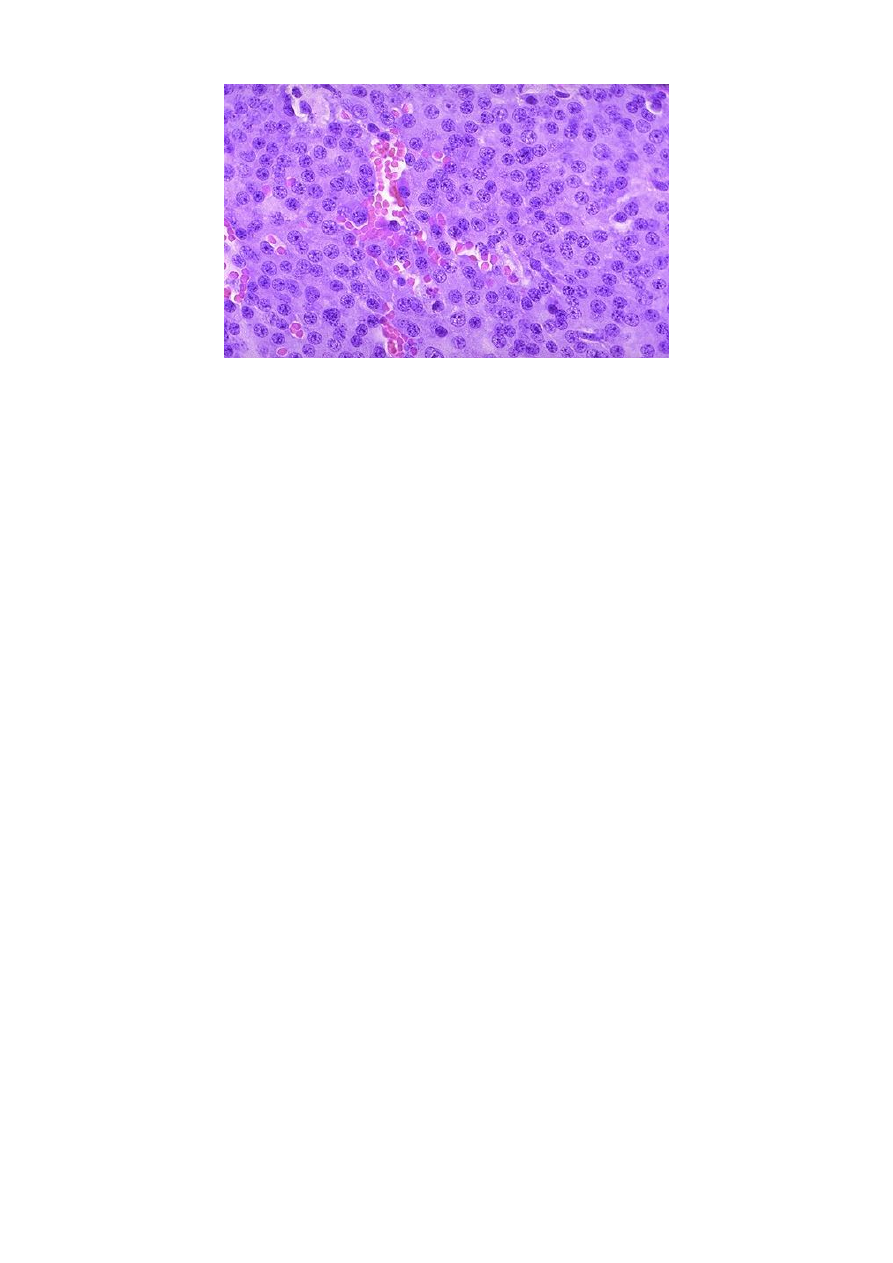
Рис.2 Аденома гипофиза состоит из небольших круглых клеток с четкими ядрами и
умеренно базофильной цитоплазмой. В центре видны сосуды.
С гиперфункцией гормона роста связаны три синдрома: гигантизм,
акромегалия и сахарный диабет. Гигантизм (свыше 190 см у девушек и 200
см у мужчин) возникает у детей и подростков с незакончившимся
физиологическим ростом. Рост костей и патологические изменения в них,
по мнению одних исследователей, связаны с высокой функциональной
активностью остеобластов, по мнению других, с особой реактивностью
эпифизарных хрящей к СТГ. После окостенения эпифизарных хрящей
гигантизм переходит в акромегалию. Ведущим признаком акромегалии
является рост тела в ширину за счет периостального увеличения костей
скелета и размеров внутренних органов, что сочетается с нарушением
обмена веществ. Заболевание развивается у взрослых. У больных
гигантизмом
и
акромегалией
обнаруживается
спланхномегалия
(увеличение размеров внутренних органов в 2–4 раза), обусловленная
гипертрофией паренхиматозных структур и избыточным ростом
фиброзной ткани. Так как гормон роста оказывает влияние на
толерантность к глюкозе, у больных с гиперпродукцией гормона роста
развивается сахарный диабет. Как правило, у них снижена половая
функция, и они быстро стареют.
При повышении уровня в сыворотке крови другого гормона
гипофиза – пролактина возникает синдром аменореи – галактореи, для
которого характерно бесплодие, вторичная аменореи и галакторея. Этот
синдром может появляться у молодых женщин после приема оральных
контрацептивов. При гиперпролактинемии в гипофизе обнаруживаются
аденомы.
Гипофункция аденогипофиза (пангипопитуитаризм) ведет к
снижению продукции тропных гормонов, что вызывает различные
сочетания эндокринных и обменных нарушений. При абсолютном или
относительном дефиците СТГ, развивается гипофизарный нанизм
(карликовость), проявляющийся малым ростом при сохранении
пропорциональности телосложения.
4
Большинство
форм
гипофизарного
нанизма
относится
к
генетическим заболеваниям. Другую группу больных нанизмом
(приобретенным)
составляют
пациенты
с
различными
видами
органической патологии ЦНС, которые возникли внутриутробно или в
раннем детском возрасте. Морфологическими причинами, вызывающими
эту патологию, являются гипоплазия гипофиза, дистрофические изменения
в нем, кистозная дегенерация, атрофия вследствие сдавления опухолью,
травматические
повреждения
гипоталамо-гипофизарной
области,
инфекционные заболевания и токсические повреждения.
При рождении гипофизарные карлики имеют нормальные размеры и
массу тела, но с второго-третьего года жизни рост замедляется. Взрослые
карлики сохраняют детские пропорции тела. У них отмечается
предрасположенность к гипогликемии (преобладание инсулинового
эффекта при отсутствии ингибирующего действия СТГ), есть признаки
гипогонадизма (дефицит гонадотропинов), гипотиреоидизма (при
подавлении секреции ТТГ), гипокортицизма (выпадение АКТГ),
утомляемость,
гипотония,
плохая
переносимость
стресса,
гиперхолестеринемия и т.д.
При морфологических исследованиях находят, что у таких больных
щитовидная железа и половые железы гипоплазированы, в надпочечниках
– гипоплазия пучковой и сетчатой зон при относительной сохранности
клубочковой. У мальчиков отмечается крипторхизм, отстают в развитии
наружные половые органы, не развивается половое оволосение в
пубертатном периоде. У девочек не развиты матка и придатки, не
развиваются молочные железы, отсутствует менструация.
Нейрогипофиз накапливает и выделяет два гормона: окситоцин,
который стимулирует сокращение матки и вызывает лактацию, и
вазопрессин (антидиуретический гормон), поддерживающий нормальную
осмолярность сыворотки крови путем резорбции воды в дистальных
канальцах почечного нефрона. Дефицит вазопрессина снижает
реабсорбцию жидкости в дистальном отделе почечного нефрона и
способствует
выделению
большого
количества
гипоосмолярной
неконцентрированной мочи. Это характерно для центрального несахарного
диабета в отличие от периферического, при котором синтезируется
достаточное количество вазопрессина, но снижена или отсутствует
чувствительность к гормону рецепторов почечных канальцев.
Причиной центрального несахарного диабета могут быть
воспалительные, дегенеративные, травматические, опухолевые и другие
поражения различных участков гипоталамо-нейрогипофизарной системы.
Среди острых и хронических инфекций, вызывающих перечисленные
морфологические изменения наиболее часто встречается грипп с его
нейротропным действием. Заболевание может возникать после черепно-
мозговой и психической травм. Причиной несахарного диабета у детей
может быть родовая травма. Симптоматический несахарный диабет
вызывается первичными и метастатическими опухолями гипоталамуса и
5
гипофиза. Метастазируют в гипофиз чаще всего рак молочной и
щитовидной желез и бронхов.
Вместе с тем у значительно числа больных (60–70%) этиология
заболевания остается неизвестной – идиопатический несахарный диабет.
По данным последних лет идиопатический несахарный диабет часто
связан с аутоиммунными заболеваниями и органоспецифическими
антителами
к
вазопрессинсекретирующим
и
реже
окситоцинсекретирующим клеткам. При этом в нейросекреторных органах
обнаруживается
лимфоидная
инфильтрация
с
формированием
лимфоидных фолликулов и замещением паренхимы этих органов
лимфоидной тканью.
Сахарный диабет.
Сахарный диабет имеет наибольший удельный вес среди
заболеваний эндокринной системы. В настоящее время около 2%
населения земного шара больны сахарным диабетом, что связано с
относительной или абсолютной недостаточностью инсулина.
Сахарный диабет может быть спонтанный (спонтанный –
возникающий без внешнего воздействия), вторичный (при заболеваниях
поджелудочной железы, эндокринных органов, генетических синдромах),
диабет беременных, латентный. Как самостоятельное заболевание
рассматривают
лишь
спонтанный
диабет,
который
делят
на
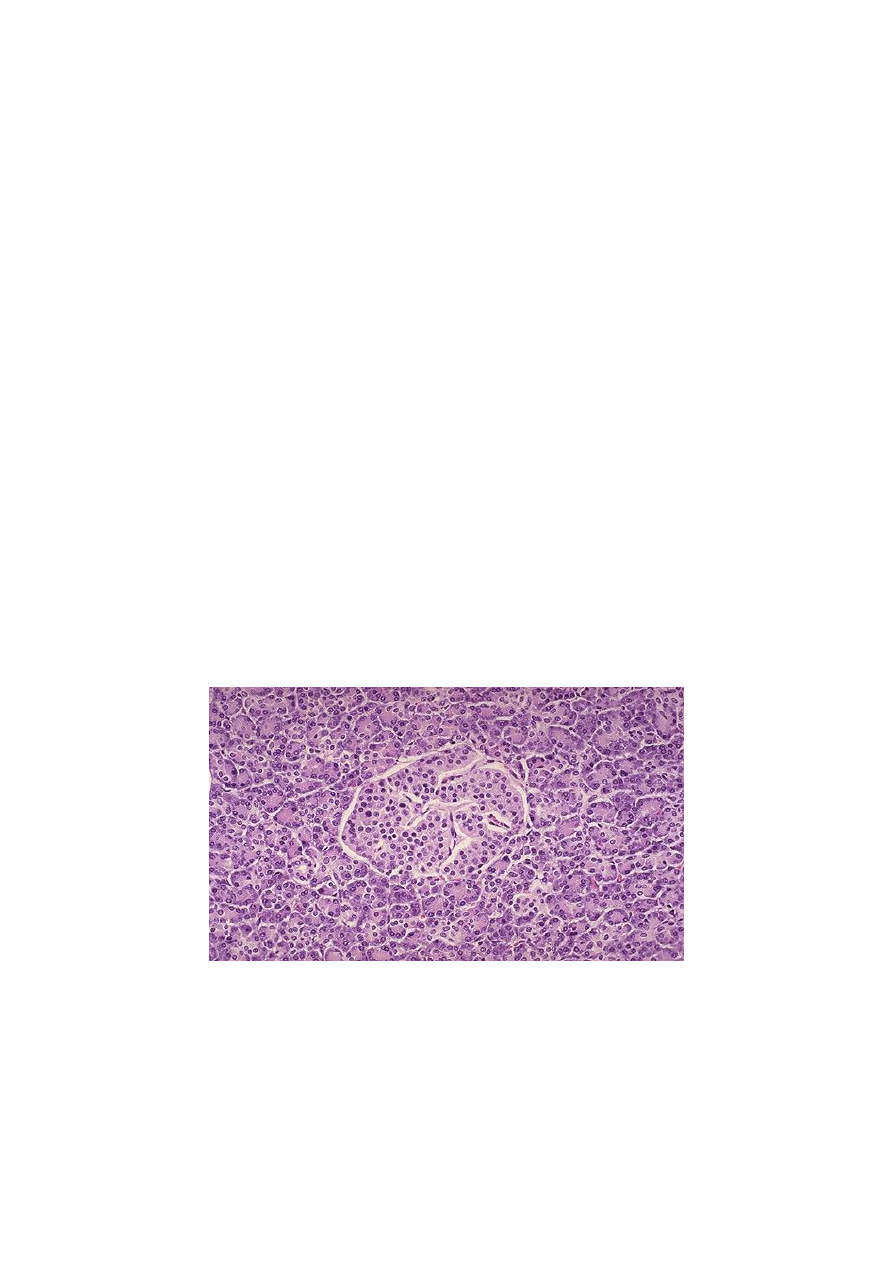
инсулинзависимый (I тип)(рис.3, 4) и инсулиннезависимый диабет (II
тип)(рис.5).
Рис.3 Нормальный островок Лангерганса: содержит альфа-клетки, секретирующие
глюкагон, бетта-клетки, выделяющие инсулин и дельта-клетки – соматостатин.
Этиологические факторы:
1. Генетически обусловленное изменение количества и функции бета-
клеток, ведущее к снижению синтеза инсулина, продукции аномального
инсулина, к нарушению превращения проинсулина в инсулин.