ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 02.11.2019
Просмотров: 3116
Скачиваний: 2

11
сти проницаемости сосудистой стенки. Автор отмечает параллелизм в проницаемости ГЭБ и ге-
мато-ликворного барьера, хотя, по другим данным (Reichardt, 1959), последний может оставаться
интактным при нарушении ГЭБ.
Для уяснения морфологического субстрата ГЭБ большое значение имеют многочисленные
работы, посвященные электронной микроскопии церебральных кровеносных сосудов.
В конечном итоге, принимая во внимание точку зрения большинства исследователей, под ГЭБ
следует понимать термин, обозначающий совокупность определенных физиологических меха-
низмов и эндотелио-глиальных образований, отделяющих от крови субстрат центральной нервной
системы, а также цереброспинальный ликвор, располагающийся между структурными элементами
в субмикроскопических щелях.
Следуя приведенной установке, удается заключить, что ГЭБ обладает определенным мор-
фологическим субстратом, изменения которого могут оказаться характерными для нарушений
проницаемости внутримозговых кровеносных сосудов. А это особенно важно учитывать при изу-
чении проблемы отека-набухания мозга.
Касаясь затронутого вопро-
са, необходимо отметить суще-
ствование двух возможностей. В
некоторых случаях переход крас-
ки в вещество мозга происходит
без гистологически заметных из-
менений капилляров мозга. Од-
нако Вölönуі и Földes (1957), по-
вышавшие проницаемость ГЭБ
введением гистамина и ацетил-
холина, установили сохранность
эндотелия, но обнаружили быстро
наступающие изменения аргиро-
фильных сосудистых мембран.
При этом была дана рекомендация
считать поражение аргирофиль-
ной системы мозговых сосудов
(утолщение, склеивание, разжи-
жение) основным гистопатологи-
ческим тестом при выявлении
нарушений ГЭБ.
Вышеприведенные данные
отвечают действительности, од-
нако возможны разнообразные
варианты гистологического отоб-
ражения нарушений структуры
церебральных сосудов в связи с
представлениями о ГЭБ.
Прежде всего для гистопа-
тологической картины отека-набухания мозга характерна деструкция стенок церебральных сосудов
(подробно об этом мы говорим в VI главе). В ряде других случаев (не связанных с оте-
ком-набуханием) — при наличии тех или иных поражений головного мозга — иногда удается ви-
деть достаточно сохранные аргирофильные мембраны мелких сосудов (что говорит о благополучии
в смысле проницаемости) внутри патологических очагов, например в толще небольших опухолевых
узелков (рис. 1,
а
). В других наблюдениях резкое уплотнение и разжижение аргирофильного ве-
щества сосудистых стенок не сочетается с разрыхлением прилежащей мозговой ткани и, таким
образом, основной гистологический признак, свидетельствующий о том, что проницаемость по-
высилась, отсутствует (рис. 1,
б
). В равной мере в условиях выраженного застойного полнокровия,
сочетающегося с явной деструкцией сосудистой стенки, нам приходилось наблюдать полную
компактность окружающего мозгового вещества (рис. 1,
в
). В некоторых случаях резко деструк-
туированные внутримозговые кровеносные сосуды (вокруг которых определялись признаки ло-
кально повысившейся проницаемости) имели лишь несколько уплотненные, но четко контуриро-
Рис. 1. Гистологическая картина внутримозговых кровеносных сосудов
при различных церебральных поражениях (не сопровождавшихся оте-
ком-набуханием);
а
— обычный аргирофильный остов мелкого сосуда в скоплении опухолевых
клеток (саркоматоз мягких мозговых оболочек с прорастанием в кору);
б
—
резкое уплотнение и разжижение аргирофильного каркаса сосуда белого ве-
щества сдавливаемого полушария большого мозга собаки — без соответству-
ющего разрыхления прилежащей ткани;
в
— переполненный кровью сосуд в
компактном белом веществе полушария, сдавленного менингиомой (стенка
сосуда дистрофически изменена);
г
— аргирофильный каркас сосуда с резко
деструктуированной стенкой и местно повышенной проницаемостью (белое
вещество височной доли). Целлоидин (
в
), парафин (
г
), замороженные срезы (
а
,
б
). Импрегнация азотнокислым серебром по Пердро (
а
) и Гомори (
б
,
г
); ге-
матоксилин-пикрофуксин (
в
). Об. 40, ок. 10 (
а
,
б
,
г
), об 10, ок. 10 (
в
).
12
ванные аргирофильные волокна (рис. 1,
г
). При различных экзогенных интоксикациях (экспери-
мент), не сопровождавшихся распространенным повышением проницаемости цереброваскулярной
системы, иногда отмечались разрастания аргирофильных волокон сосудистых стенок — аргиро-
фиброз (явление защитного характера).
Все эти данные свидетельствуют о том, что гистопатологическое отображение нарушенной
проницаемости ГЭБ не является строго постоянным. При наличии существенных изменений
структуры стенок внутримозговых кровеносных сосудов в светомикроскопической картине моз-
гового вещества могут отсутствовать четкие указания на повысившуюся проницаемость. С другой
стороны, несмотря на предпосылки (поражение головного мозга патологическим процессом),
строение церебральных сосудов может оставаться неизмененным или хотя бы не адекватным тому
состоянию, в котором находится мозговая паренхима.
Мы полагаем, что детальная расшифровка природы вышеприведенных явлений станет воз-
можной в итоге углубленного изучения функций ГЭБ не только с преимущественным освещением
механизма «кровь — мозг» (как это практикуется в настоящее время), но и с учетом обратного
соотношения. В этом плане заслуживает особого внимания точка зрения Б.Н. Клосовского (1965),
считающего, что степень проницаемости ГЭБ (эндотелия капилляров) зависит в первую очередь от
функционального состояния нервных клеток, регулирующих проницаемость и просвет мозговых
сосудов как гуморальным путем, так и посылкой к ним нервных импульсов.
В литературе имеются и некоторые другие указания в аналогичном направлении. Так,
например, Н.Н. Зайко (1955, 1962, 1964) сообщает, что разница в сорбционных свойствах нервной
ткани зависит и от увеличения проницаемости церебральных сосудов, и от изменения функцио-
нальных свойств самих нервных клеток; он также считает, что ГЭБ достаточно устойчив (в отличие
от ряда авторов, говорящих о лабильности ГЭБ).
При обсуждении проблемы ГЭБ (применительно к основам учения об отеке-набухании мозга)
необходимо исходить из представлений, согласно которым
нарушения проницаемости внутри-
мозговых кровеносных сосудов определяются не только собственно сосудистыми обстоятель-
ствами
(деструкция стенок, гемостаз, «прорыв» барьера принесенными кровью вредностями),
но и
особенностями состояния самого мозгового вещества
. В этом отношении цереброваскулярная
система не отличается от кровоснабжающих приспособлений других органов и проницаемость ГЭБ
на этой основе должна расцениваться как подчиняющаяся всем тем закономерностям, о которых мы
говорили выше.
В неврологической литературе содержится множество указаний на повышение проницаемо-
сти ГЭБ при различных воздействиях на организм, патологических состояниях и заболеваниях.
Особенно важным является признание возможности медикаментозного изменения проницаемости
сосудов головного мозга. С помощью различных индикаторных методик (витальное окрашивание,
радиоактивные изотопы) и других методов показано повышение проницаемости ГЭБ при череп-
но-мозговых травмах, электро- и кардиазоловом шоке, воздушной эмболии, искусственном кро-
вообращении, умеренной гипотермии, воздействии гистамина и др. Некоторые авторы подчерки-
вают топографические особенности нарушенной проницаемости ГЭБ, объясняемые не только
местными изменениями обменных процессов, но и различиями в организации барьерных образо-
ваний в разных отделах головного мозга.
Исходя из изложенного, при рассмотрении проблемы отека-набухания мозга мы не видим
оснований для окончательного отказа от сосудистой теории ГЭБ, локализующей барьер на уровне
сосудистой стенки. Состояние последней принимается нами в качестве достаточно важного пока-
зателя при оценке нарушений водно-солевого обмена центральной нервной системы и церебраль-
ной гемодинамики.
О ПЕРИВАСКУЛЯРНЫХ ПРОСТРАНСТВАХ
ГОЛОВНОГО МОЗГА
Опираясь на некоторые представления о субмикроскопических межклеточных щелях мозго-
вого вещества и морфологическом субстрате гемато-энцефалического барьера, следует обсудить
понятие «периваскулярное пространство» головного мозга, так как оно имеет прямое отношение к
расшифровке одного из ведущих гистологических признаков церебрального отека-набухания.

13
Для современного состояния рассматриваемого вопроса характерно отсутствие единства
мнений: здесь четко наметились три точки зрения. Согласно первой и самой ранней из них, пери-
васкулярные пространства представляют собой непременные образования в веществе головного
мозга высших животных и
человека и играют важную
роль в его жизнедеятельности
(трансцеребральный ток це-
реброспинального
ликвора,
циркуляция тканевой жидко-
сти мозга). Вторая группа
авторов рассматривают про-
странства в качестве предсу-
ществующих и появляющих-
ся только в условиях патоло-
гии. Представители третьей
группы,
основывающиеся
главным образом на эле-
кронномикроскопических
данных, объявляют перивас-
кулярные пространства арте-
фактом во всех без исключе-
ния случаях и отрицают их прижизненное существование.
Определенный интерес должно представить систематизированное изучение микроскопиче-
ской картины периваскулярных пространств головного мозга в разнообразных условиях, с осве-
щением таких вопросов, как особенности локализации пространств, соотношение между ними и
уровнем кровенаполнения внутримозговых кровеносных сосудов, зависимость между простран-
ствами и состоянием структур сосудистой стенки.
В объеме изученного материала — при строгом единообразии метода обработки — выявля-
лась четкая зависимость степени выраженности и распространения пространств от исходных осо-
бенностей наблюдений. При очаговых процессах пространства, например, всегда преобладали в
окружности очага. Уже один этот факт говорит о том, что появление хорошо очерченных про-
странств зависит не только от технических причин.
В условиях световой микроскопии изредка удается видеть пространства, возникшие за счет
глиальной мембраны — путем увеличения камер Гельда (рис. 2,
а
). При остром повышении про-
ницаемости отдельных внутримозговых сосудов оптически пустое (заполненное прозрачной жид-
костью) пространство может возникать в неповрежденной мозговой ткани (рис. 2,
б
). В то же время
в сильно отечном разрыхленном мозговом веществе иногда не обнаруживается щелевидных цир-
кулярных околососудистых пространств, несмотря на гемостаз, деструкцию стенок сосудов и вы-
ход за пределы сосудистого русла богатой белком жидкости (рис. 2,
в
).
О прижизненном возникновении и функциональной значимости периваскулярных про-
странств головного мозга косвенно свидетельствует отсутствие закономерной зависимости между
их выраженностью и уровнем кровенаполнения мозговых сосудов. Здесь мы выделили ряд вари-
антов: переполнение мозговых сосудов кровью сопровождается образованием периваскулярного
пространства (рис. 3,
а
); на фоне резкого переполнения пространство отсутствует (рис. 3,
б
); про-
странство образуется в связи со спадением сосуда и дистонией его стенки (рис. 3,
в
); при всех вы-
шеуказанных обстоятельствах пространство отсутствует или имеет минимальную выраженность
(рис. 3,
г
). Нами не найдено постоянной связи между особенностями периваскулярных пространств
и состоянием структур сосудистой стенки: пространство иногда возникает в окружности совер-
шенно сохранных сосудов и не выражено там, где стенка сосуда заметно изменена (рис. 2,
в
, 3,
б
).
Первый из этих вариантов, в частности, нередко выявляется в коре мозга контрольных (не под-
вергшихся каким-либо манипуляциям) животных. Это явление скорее всего объясняется неболь-
шими чисто функциональными сдвигами сосудистой проницаемости и водного баланса мозга
(возможно, они связаны с особенностями забоя животных), перераспределением минимальной
свободной жидкости (без увеличения ее количества). Кроме того, остается вероятной и небольшая
артефициальность.
Рис. 2. Соотношение кровеносных сосудов и мозговой паренхимы,
а
— периваскулярное пространство, образованное за счет глиальной мембраны;
б
—
пространство в неповрежденном мозговом веществе;
в
— кровеносный сосуд в
отечной зоне, не имеющий четкого циркулярного периваскулярного пространства.
Целлоидин. Гематоксилин-эозин. Об. 40, ок. 5.
14
Как показали наши наблю-
дения, ряд особенностей перивас-
кулярных пространств головного
мозга зависит от исходных пред-
посылок в каждой отдельной
группе случаев. Пространства мо-
гут быть более или менее объем-
ными, концентрическими или ха-
рактеризоваться
пристеночным
расположением сосуда; оптически
пустыми или заполненными жид-
костью, богатой белком, а также
глиально-адвентициальной
во-
локнистостью или форменными
элементами крови. Пространства
наиболее типичны для серого ве-
щества, но могут наблюдаться и в
белом веществе полушарий, под-
корковых
формациях,
стволе,
мозжечке. Соотношение перивас-
кулярных пространств и окружа-
ющей их паренхимы представля-
ется разнообразным (последняя может быть компактной или полностью или частично разрыхлен-
ной). Края отдельных периваскулярных пространств интенсивно закрашиваются гематоксилином
(вследствие пропитывания их белком). В некоторых случаях при наличии разрыхления мозговой
ткани и значительного фиброза сосудистой стенки не удается установить ни малейших следов пе-
риваскулярной щели (рис. 4,
а
),
хотя иногда фиброзно изме-
ненные сосуды бывают окру-
жены широким пространством
(рис. 4,
б
). Не всегда способ-
ствуют возникновению пери-
васкулярных
пространств и
околососудистые
кровоизлия-
ния. На рис. 4, в вблизи крупной
артерии располагается значи-
тельное количество излившейся
крови (мозг собаки, получившей
черепно-мозговую
травму);
кровь прилежит к сосуду с одной
стороны, занимая участок па-
ренхимы, подвергшейся неко-
торому разрыхлению. Однако
никаких намеков на периваску-
лярное пространство нет. Не
исключено,
что
форменные
элементы крови, скопившиеся
вблизи данного сосуда, вышли
из других, мелких сосудов и
впоследствии сюда перемести-
лись, но не периваскулярным, а
транспаренхимальным
путем.
Однажды (при опухолевом поражении мозга) мы даже наблюдали весьма своеобразный феномен
образования мощного «вала» из глиальных волокон в окружности дистрофически измененных
внутримозговых сосудов, препятствовавшего образованию периваскулярного пространства (рис. 4,
г
).
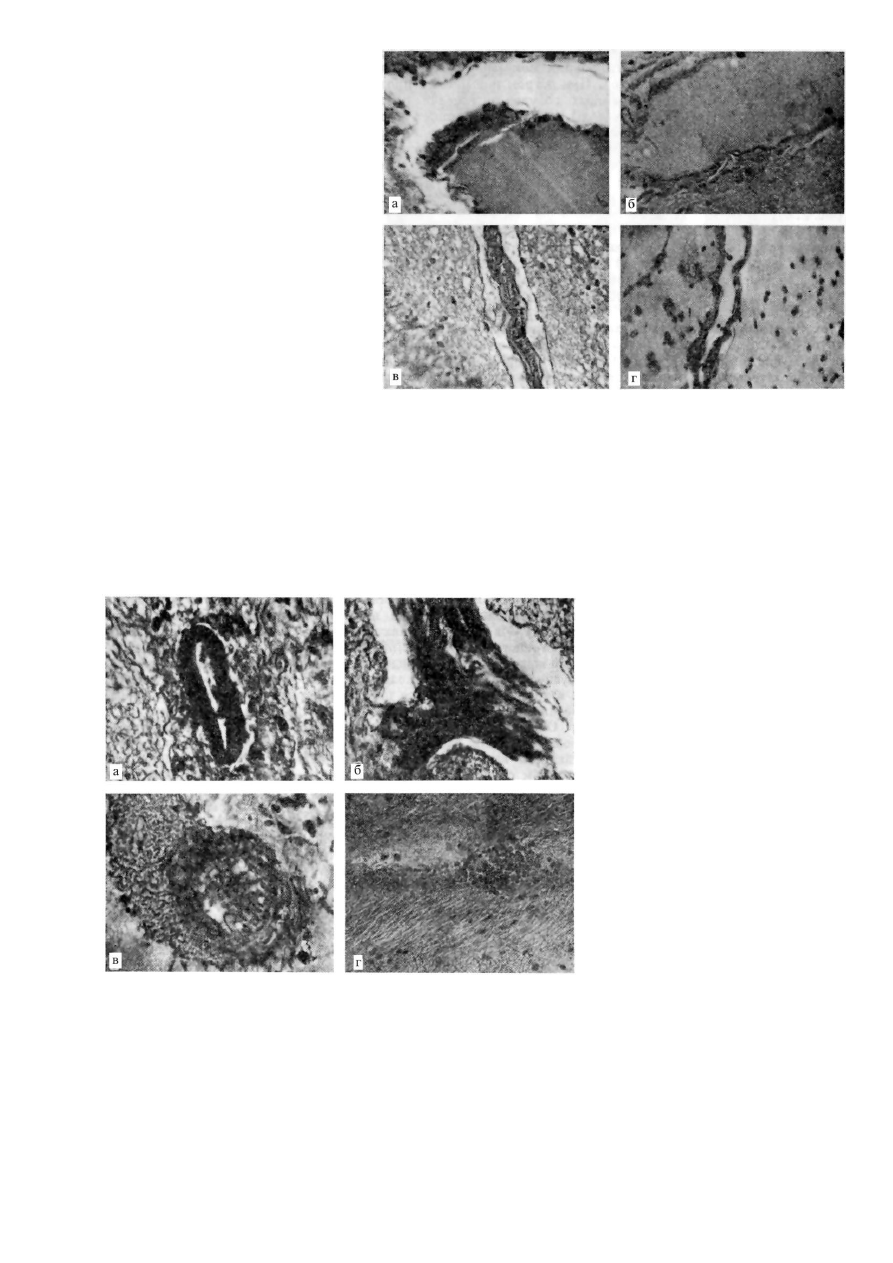
Рис. 3. Соотношение кровеносных сосудов и мозговой паренхимы;
а
— периваскулярное пространство в окружности переполненного кровью
сосуда;
б
— несмотря на гемостаз, пространство отсутствует;
в
— дистония
сосуда и образование периваскулярного пространства;
г
— несмотря на
дистонию, пространство не выражено. Целлоидин. Гематоксилин-эозин. Об.
40, ок. 10 (
а
), об. 20, ок. 10 (
б
,
в
,
г
).
Рис. 4. Соотношение кровеносных сосудов и мозговой паренхимы;
а
— фиброз адвентиции интрацеребрального сосуда при отсутствии периваску-
лярного пространства;
б
— фиброзно измененный сосуд, окруженный перивас-
кулярным пространством;
в
— околососудистое кровоизлияние без образования
пространства;
г
— «вал» глиальных волоконец в окружности дистрофически
измененного сосуда. Парафин (
а
), целлоидин (
б
,
в
,
г
). Метод Маллори (
а
), ге-
матоксилин-пикрофуксин (
б
), гематоксилин-эозин (
в
,
г
). Об. 40, ок. 5 (
а
,
в
,
г
), об.
20. ок. 10 (
б
).
15
К условиям, определяющим образование названных пространств, относится не только по-
вышение проницаемости внутримозговых кровеносных сосудов (как это принято считать), но и
состояние самой мозговой паренхимы, ее определенная предуготовленность. Вне этого допущения
не удается объяснить того, что при одной и той же предпосылке — сосудистой патологии (спадение
или переполнение сосуда при дистрофических изменениях его стенки) — в одних случаях возни-
кает обширное периваскулярное пространство (см. рис. 2,
б
), в других происходит только частич-
ный выход плазмы за пределы сосудистого русла, несмотря на диффузное разрыхление околосо-
судистой паренхимы (см. рис. 2,
в
), а в третьих наблюдается параваскулярное разрыхление без
образования пространства (см. рис. 3,
б
,
г
, 4,
в
).
Очевидно, существует сопротивление околососудистых участков мозговой ткани, зависящее
от особенностей индивидуальной реактивности вещества центральной нервной системы в каждом
отдельном случае, и распространение в мозге свободной жидкости и клеточных инфильтратов
возможно не по одним периваскулярным путям.
Литературные данные и гистологический анализ ткани головного мозга при различных со-
стояниях центральной нервной системы не дают оснований отказаться от понятия «периваску-
лярное пространство» мозговой ткани. Так как характер изученного нами материала охватывает
главным образом различные стадии функциональных и органических нарушений центральной
нервной системы (включая пограничное состояние норма — патология), мы не можем демон-
стрировать периваскулярные пространства в нормальном мозговом веществе. Однако отмеченное в
вышеуказанных условиях разнообразие и своеобразие пространств заставляет предполагать, что
они возникают на базе предсуществующих конструкционных особенностей головного мозга (это
подтверждают и некоторые электронномикроскопические наблюдения). Привлекая данные гисто-
патологии к освещению одной из проблем нормальной гистологии, мы все же условно говорим о
«возникновении», а не о расширении периваскулярных пространств при соответствующих пред-
посылках. Видимые в условиях световой микроскопии периваскулярные пространства, вероятно,
образуются за счет различных (нередко сочетающихся) механизмов: повышения проницаемости
внутримозговых кровеносных сосудов и собственно паренхиматозных нарушений.
Образование
пространств является не механическим, а биологическим, активным процессом
.
Взаимодействие собственно сосудистого и паренхиматозного факторов в образовании пери-
васкулярных пространств свидетельствует об их прижизненном происхождении, и в связи с этим
они могут рекомендоваться в качестве показателей, характеризующих состояние головного мозга.