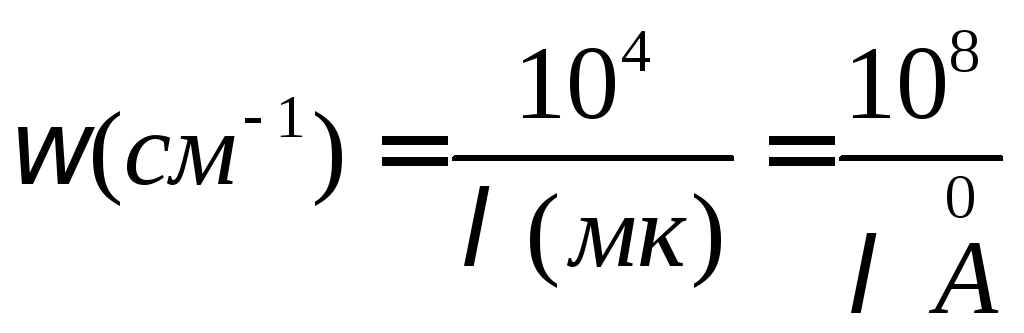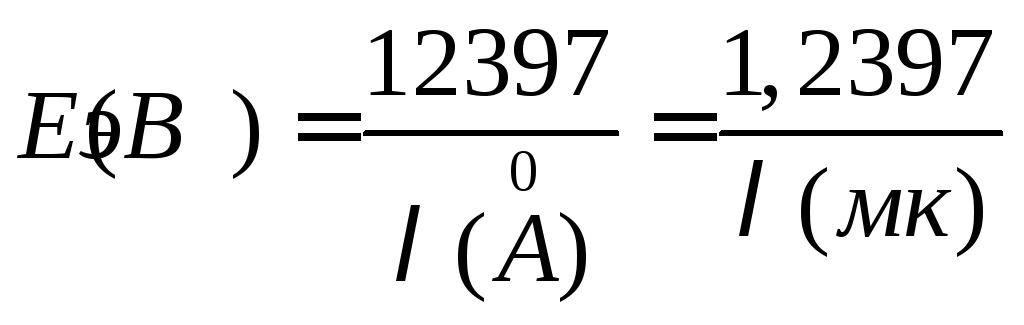ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 30.07.2024
Просмотров: 416
Скачиваний: 0
СОДЕРЖАНИЕ
Федеральное агентство по образованию
Глава 1. Металлические материалы 7
Глава 1. Металлические материалы
1.1. Основные сведения о производстве металлов и сплавов
1.2. Основные свойства металлов и сплавов
1.3. Механические свойства металлов и сплавов
Глава 2. Физические основы Спектрального анализа
2.1. Общее представление о строении вещества
2.2. Строение атома и атомные спектры
3.1. Возбуждение вещества и интенсивность спектральных линий
3.3. Схемы питания газовых разрядов
Глава 4. Оптика спектральных аппаратов
4.3. Оптическая схема спектрального аппарата
4.4. Основные характеристики и параметры спектральных аппаратов
3. Увеличение спектрального аппарата
4.5. Типы приборов спектрального анализа
Оптическая схема стилоскопа сл-13
Оптическая схема стилоскопа слу
6.1. Подготовка изделий и стандартных электродов к анализу
Группы аналитических спектральных линий с условными обозначениями
Линия "v4" надежно выявляется при концентрации V свыше 0,1%
6.3. Меры безопасности при работе со стилоскопом
6.4. Организация и оформление работ по спектральному анализу
Сварной стык; задвижка;тройник;расходомерная шайба; 65-77 - сварные стыки
Видимая
область
занимает узкий участок спектра примерно
от 4000 до 7500![]() ).
Электромагнитное излучение, соответствующее
этой области, воспринимается глазом
человека как видимый свет различных
цветов в зависимости от длины волны.
Видимое излучение занимает только
маленький участок во всем электромагнитном
спектре, но способность глаза
непосредственно видеть только эти волны
делает его главным для человека. Для
спектрального анализа эта область также
представляет значительный интерес,
хотя и меньший, чем соседние: ультрафиолетовая
и ближняя инфракрасная области.
).
Электромагнитное излучение, соответствующее
этой области, воспринимается глазом
человека как видимый свет различных
цветов в зависимости от длины волны.
Видимое излучение занимает только
маленький участок во всем электромагнитном
спектре, но способность глаза
непосредственно видеть только эти волны
делает его главным для человека. Для
спектрального анализа эта область также
представляет значительный интерес,
хотя и меньший, чем соседние: ультрафиолетовая
и ближняя инфракрасная области.
Ультрафиолетовая
область
спектра примыкает к фиолетовому участку
видимой области и продолжается в сторону
коротких волн вплоть до рентгеновских
лучей. В связи с некоторыми различиями
в спектральных приборах и методах
регистрации спектра ее разделяют на
три участка: область
ближнего и среднего ультрафиолета
(4000![]() - 2300
- 2300![]() ),область
дальнего ультрафиолета
(2300
),область
дальнего ультрафиолета
(2300![]() - 1850
- 1850![]() )
и областьвакуумного
ультрафиолета
(1850
)
и областьвакуумного
ультрафиолета
(1850![]() - 50
- 50![]() ),
излучение в которой поглощается воздухом.
),
излучение в которой поглощается воздухом.
К области вакуумного ультрафиолета примыкает рентгеновская область, которая важна для медицины и техники а также и для спектрального анализа, так как излучение и поглощение рентгеновских лучей связано с изменением внутреннего строения атомов.
За рентгеновской областью расположена область -лучей, которые возникают при различных процессах в ядрах атомов.
Изображение областей спектра приведено на рис. 7
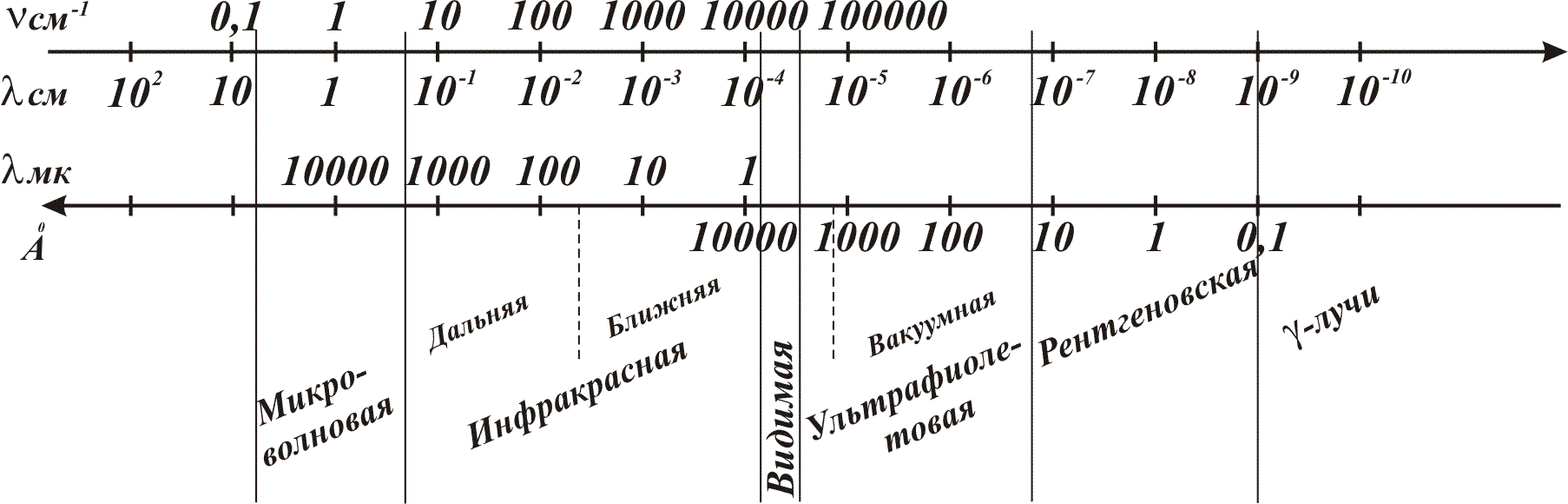
Рис. 7. Области спектра
В таблице 1 приведены применяемые в спектральном анализе величины и соотношения между ними.
Таблица 1
Единицы измерения
|
Величина |
Единица измерения |
Соотношение между единицами |
Соотношение между величинами |
|
Длина волны
|
Метр (м) |
1м=106мк=109ммк=1010 |
|
|
Микрон (мк) или микрометр (мкм) |
1мк=10-6м=103ммк=104 |
||
|
Миллимикрон (ммк) или нанометр (нм) |
1ммк=10-9м=10-3мк=10 |
||
|
Ангстрем
( |
1 |
||
|
Частота
|
Герц (Гц) или сек-1 |
|
|
|
Мегагерц (МГц) |
1МГц=106Гц |
||
|
Волновое число
|
Обратный метр (м-1) |
1м-1=10-2см-1 |
|
|
Обратный сантиметр (см-1) |
1см-1=102м-1 |
||
|
Энергия фотона Е |
Джоуль (Дж) |
1Дж=107эрг=6,24191018эВ |
|
|
Эрг (эрг) |
1эрг=10-7Дж=6,24191011эВ |
||
|
Электронвольт (эВ) |
1эВ=1,6020710-19Дж=1,60207 10-12эрг |
Глава 3. Источники света
3.1. Возбуждение вещества и интенсивность спектральных линий
Рассмотрим возбуждение вещества, находящегося в источнике света в газообразном состоянии при высокой температуре. Обладая большой кинетической энергией, частицы двигаются с большой скоростью и часто сталкиваются друг с другом. Если кинетическая энергия частиц меньше, чем потенциал возбуждения ближайшего энергетического уровня, то возбуждения не будет, сколько бы последовательных соударений не произошло. Такие соударения называют упругими.
Средняя кинетическая энергия Е частиц в газе определяется его температурой Т. При упругих ударах имеет место только перераспределение кинетической энергии между отдельными частицами. Но в тех случаях, когда кинетическая энергия больше потенциала возбуждения, может произойти неупругое столкновение, при котором вся или часть кинетической энергии идет на увеличение внутренней энергии атома, иона или молекулы. Именно неупругие соударения приводят к возбуждению вещества и появлению линейчатого излучения.
При соударении тяжелых частиц (атомов и молекул) между собой только часть кинетической энергии может переходить во внутреннюю энергию. Такие соударения бывают большей частью упругими, они не приводят к возбуждению. Гораздо эффективнее соударения тяжелых частиц с электронами. Масса электрона очень мала, и при неупругих соударениях практически вся кинетическая энергия электрона идет на возбуждение атомов или молекул. Поэтому число возбужденных частиц зависит, главным образом, от числа свободных электронов и от их кинетической энергии.
При неупругом соударении может также произойти ионизация нейтральных частиц, если кинетическая энергия электрона достаточно велика. При этом увеличивается общее число заряженных частиц в газе.
Например,
если направить поток электронов,
ускоренных электрическим полем при
напряжении 4,9эВ или несколько больше,
на пары ртути, то при соударениях с
электронами произойдет возбуждение
атомов, которые имеют первый потенциал
возбуждения 4,9эВ. Наиболее эффективно
происходит возбуждение при энергии
электронов, равной точно 4,9эВ. Пары ртути
начнут излучать линию =2536,5![]() .
При увеличении напряжения, ускоряющего
электроны, появляются линии с более
высокими потенциалами возбуждения. При
напряжении 10,4В (потенциалы ионизации
ртути 10,4эВ) появляются все дуговые линии
ртутного спектра, а также становится
возможной ионизация атомов при соударениях
с электронами.
.
При увеличении напряжения, ускоряющего
электроны, появляются линии с более
высокими потенциалами возбуждения. При
напряжении 10,4В (потенциалы ионизации
ртути 10,4эВ) появляются все дуговые линии
ртутного спектра, а также становится
возможной ионизация атомов при соударениях
с электронами.
В большинстве случаев атом может находиться в возбужденном состоянии в течение примерно 10-8сек. После этого он самопроизвольно переходит на более низкий уровень с излучением фотона. Чем чаще совершаются такие переходы, тем больше интенсивность соответствующей спектральной линии. Для определения интенсивности линии необходимо знать число атомов, находящихся в возбужденном состоянии на соответствующем верхнем уровне.
За время жизни атома в возбужденном состоянии он сталкивается с другими частицами. Такие соударения могут быть гасящими – тогда внутренняя энергия возбужденного атома идет на увеличение кинетической энергии другой частицы. Эти соударения уменьшают число возбужденных частиц и снижают интенсивность спектральной линии. Возможны и обратные случаи, когда при втором соударении произойдет дальнейшее возбуждение частицы на более высокий уровень или ее ионизация.
Число неупругих соударений зависит от соотношения между потенциалом возбуждения вещества и кинетической энергией электронов и других частиц. Средняя кинетическая энергия частиц в газе определяется его температурой. Ее можно вычислитm при учете движения в одной плоскости по формуле
![]() (13)
(13)
где k=1,38010-23дж/град=8,61610-5эВ/град – постоянная Больцмана;
Т – абсолютная температура газа.
При комнатной температуре (Т=3000К):
![]()
При обычном давлении происходит большое число соударений, что приводит к перераспределению энергии между частицами и, в результате, устанавливается тепловое равновесие, при котором число частиц с данной энергией остается постоянным. В этом случае можно пользоваться формулой (13). Чем больше энергия той или иной частицы отличается от среднего значения, тем меньше таких частиц в газе. Распределение частиц по энергиям будет иметь вид, представленный на рисунке 8.
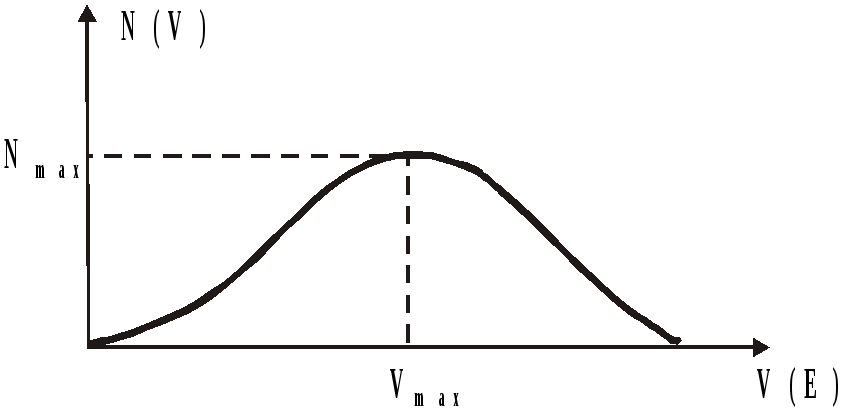
Рис. 8. Распределение частиц по энергиям: N – число частиц, обладающих данной энергией, V – скорости частиц
Для
примера рассмотрим возбуждение паров
ртути и натрия, которые состоят из
отдельных атомов, и молекулярного азота
в условиях теплового равновесия при
разных температурах. При комнатной
температуре средняя кинетическая
энергия частиц 0,026эВ. Первый молекулярный
уровень в молекуле азота имеет потенциал
возбуждения приблизительно 0,0005эВ.
Поэтому уже при комнатной температуре
большинство молекул азота находятся в
возбужденном состоянии. Электронные
уровни как у азота, так и у натрия и
ртути, не возбуждены. При температуре
Т=20000
(![]() )
за счет соударения с наиболее быстрыми
частицами, имеющими кинетическую
энергию, во много раз большую, чем
средняя, становится заметно возбуждение
атомов натрия: потенциал возбуждения
линий желтого дуплета равен 2,1эВ.
Возбуждение электронных уровней ртути
и азота практически еще не происходит,
так как они имеют более высокие потенциалы
возбуждения (4,9эВ –Hg,
6,2эВ – N2).
При Т=110000С,
средняя кинетическая энергия частиц
около
)
за счет соударения с наиболее быстрыми
частицами, имеющими кинетическую
энергию, во много раз большую, чем
средняя, становится заметно возбуждение
атомов натрия: потенциал возбуждения
линий желтого дуплета равен 2,1эВ.
Возбуждение электронных уровней ртути
и азота практически еще не происходит,
так как они имеют более высокие потенциалы
возбуждения (4,9эВ –Hg,
6,2эВ – N2).
При Т=110000С,
средняя кинетическая энергия частиц
около
![]() .
При этой температуре хорошо возбуждаются
электронные уровни ртути, а у натрия
наряду с возбуждением происходит сильная
ионизация, так как его потенциал ионизации
всего 5,1эВ. Потенциал ионизации ртути
10,4эВ, поэтому появляется сравнительно
небольшое число ионовHg+.
При этой температуре происходит почти
полная диссоциация молекул азота на
атомы.
.
При этой температуре хорошо возбуждаются
электронные уровни ртути, а у натрия
наряду с возбуждением происходит сильная
ионизация, так как его потенциал ионизации
всего 5,1эВ. Потенциал ионизации ртути
10,4эВ, поэтому появляется сравнительно
небольшое число ионовHg+.
При этой температуре происходит почти
полная диссоциация молекул азота на
атомы.
При тепловом равновесии наступает также равновесие между процессами возбуждения частиц и переходом их в обычное состояние. Чем больше потенциал возбуждения вещества, тем меньше число частиц, находящихся в возбужденном состоянии при данной температуре. Число возбужденных атомов в этих условиях можно определить по формуле
![]() (14)
(14)
где N0 - общее число атомов данного элемента;
N – число атомов, находящихся в возбужденном состоянии с потенциалом возбуждения Е;
g и g0 – число простых термов, составляющих возбужденный и нулевой термы соответственно;
Т – температура источника света;
![]() -
постоянная для данной спектральной
линии величина.
-
постоянная для данной спектральной
линии величина.
При увеличении Т возбуждаются электронные уровни у различных элементов. В этом случае возникают атомные спектры.
Зная распределение атомов по уровням энергии, можно определить интенсивность любой спектральной линии по температуре источника света и концентрации атомов данного элемента. Из формулы (14) видно, что интенсивность линии J определяется числом фотонов в единицу времени и энергией каждого фотона. Число излучаемых фотонов пропорционально числу атомов, находящихся в соответствующем возбужденном состоянии. Поэтому для линии с потенциалом возбуждения Е можно записать
![]() (15)
(15)
Объединив все постоянные для данной спектральной линии величины и обозначив полученную величину через А, приходят к следующему выражению
![]() (16)
(16)
в котором число атомов N0 заменено концентрацией С вещества в источнике света.
Из формулы (16) видно, что при постоянной концентрации вещества в источнике света интенсивность спектральной линии сильно зависит от температуры. По мере увеличения температуры интенсивность любой линии быстро растет, проходит через максимум, а затем начитает уменьшаться. Уменьшение интенсивности связано с ионизацией при высокой температуре и уменьшением числа нейтральных атомов. Каждая линия в зависимости от ее потенциала возбуждения и потенциала ионизации вещества имеет максимум при определенной температуре. Например, спектральные линии нейтральных атомов щелочных металлов имеют максимальную интенсивность при температуре источника света около 40000. При более высокой температуре их интенсивность падает. У бора, потенциал ионизации которого гораздо выше, наибольшая интенсивность дуговых линий наблюдается при температуре около 60000.