Файл: Перевозка опасных веществ на судах (навалом, в упаковке) (в т ч. включая ознакомление с разделом С 49 Кодекса Федеральных правил сша).doc
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 26.10.2023
Просмотров: 262
Скачиваний: 4
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
-
2-й том перекрывает классы опасности 1-3, -
3-й том – классы 4 и 5, -
4-й – с 6-го по 9-й.
В каждом томе представлены наиболее важные сведения в отношении классификации и стандартов упаковки грузов, тип и требования к упаковке, требования по маркировке грузов, размещению и сегрегации грузов на борту судна.
После общей информации следует описание каждого груза в отдельности, содержащие детальные инструкции по его обработке.
Некоторые страницы разделены пополам: в верхней и нижней части даются сведения о РАЗНЫХ ГРУЗАХ.
Для каждого груза указаны «Свойства» (Properties) и «Замечания» (Observations), в которых может содержаться ВАЖНАЯ ИНФОРМАЦИЯ в отношении мер безопасности или использования номера ООН.
Дополнение к МКМПОГ Содержит:
· Перечень аварийных процедур
· Кодекс по оказанию первой помощи
· Кодекс перевозки навалочных грузов
· Процедуры оповещения в случаях инцидентов с грузом
· Сведения об упаковке и маркировке грузов
· Кодекс по использованию пестицидов на судах
· Кодекс по перевозке радиоактивных материалов.
РАЗДЕЛ 2. Основные физические и химические свойства опасных грузов
Более половины опасных грузов – это продукция нефтехимии, (органические и неорганические), углеводороды и растительные масла.
Физические свойства грузов – это все, что можно взвесить, измерить, рассчитать: относительный удельный вес, температуру кипения, вспышки и самовоспламенения, замерзания; давление паров, плотность паров, вязкость груза, коэффициент объемного расширения, способность накопления заряда статического электричества и т.п.
Химические свойства груза – химическая формула, группа химической продукции, способность вступления в реакцию с кислотами, основаниями, водой, воздухом, с другими химическими веществами, материалами судовых конструкций.
Физические и химические характеристики жидких опасных грузов имеют прямое отношение к транспортным опасностям. К этим характеристикам относятся давление паров, воспламеняемость газов, выделяемых из жидкостей, и плотность этих газов.
Давление паров
Переход из жидкого состояния в парообразное возможен двумя различными процессами: испарением или кипением.
Испарение происходит при любой температуре (выстиранное белье сохнет на морозе).
Кипение происходит при определенной температуре кипения, при которой давление насыщенного пара данной жидкости становится равным внешнему давлению.
Процесс, обратный парообразованию, называется конденсацией.
Когда скорость парообразования и конденсации становится равной, то это состояние называется равновесием, а давление пара при таком равновесии называется насыщенным.
Зависимость между давлением и температурой паров
Температура кипения воды составляет 100°С. Однако при понижении атмосферного давления температура кипения падает, а при повышении давления – увеличивается.
Давление насыщенного пара
В координатах Давление–Температура можно построить «кривую кипения».
Для воды табличные данные этих координат равны:
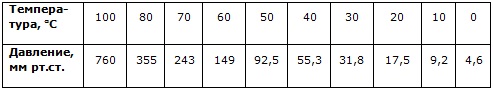
Эта кривая является границей между жидким и парообразным состоянием.
Из таблицы видно, если насос при всасывании создает вакуум 149 мм рт. ст., то вода закипит при 60°С. При этом же давлении, но при температуре 25°С пар будет ненасыщенным.
Для сравнения давление насыщенного пара приведено ниже в м.вод.ст. для воды, легкой нефти (уд. вес 0,85) и бензина (уд.вес 0,78).
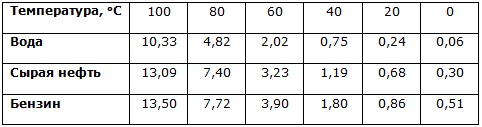
При повышении температуры увеличивается давление насыщенных паров.
При разряжении атмосферного давления снижается температура кипения жидкости.
Парциальное давление
Давление смеси газов равно сумме их парциальных давлений (от лат. слова pars=часть). Этот закон открыл Дальтон.
Чтобы понять физический смысл давления насыщенного пара и парциального давления, ознакомимся с таким примером:
Пусть над водой собрано 570 мм3 газа при температуре 20°С и давлении 781 мм рт. ст.
Это давление складывается из двух величин – парциального давления самого газа и давления насыщенного водяного пара. Последнее при температуре 20°С равно 17,5 мм рт. ст. Следовательно, парциальное давление газа в данном случае равно 781-17,5 = 763,5 мм рт. ст.
Диффузия :
Это самопроизвольный процесс перемещения вещества, приводящий к выравниванию его концентрации без вступления в реакцию.
Пределы воспламеняемости:
или взрываемости – это одно и то же, только различная скорость окисления=сгорания).
Жидкие грузы, испаряясь, образуют смесь паров углеводородов с воздухом. Эта смесь воспламеняется не при любой концентрации, а только в определенных пределах:
-
один из них называется верхним (ВПВ), -
а другой – нижним (НПВ).
Предел взрываемости измеряется в процентах по объему. В танкерной практике взрывоопасность определяется по температуре груза, т.к. в замкнутом объеме давление паров становится насыщенным.
Летучесть
Если воспламенение уже произошло, смесь паров углеводородов с воздухом горит синим пламенем (как на газовой плите).
Способность к образованию паров углеводородов называется летучестью.
Мерой летучести является температура вспышки (см. далее).
При температуре вспышки 60°С и выше груз считается нелетучим; менее 60°С - летучим.
Температура вспышки
Определяется в лаборатории на специальном оборудовании.
Есть два метода:
в закрытом тигле (англ. сокр. с.с.) и
в открытом тигле (о.с.).
На флоте применяется «в закрытом тигле». Температура вспышки сообщается в паспорте качества и указывается в карте данных по грузу. При этой температуре смесь паров вспыхнет при поднесении открытого огня.
Температура воспламенения
Температура, при которой нагреваемый в определенных условиях продукт загорается при поднесении к нему пламени и горит не менее 5 секунд.
Температура воспламенения для большинства нефтепродуктов на 20-25°С выше температуры вспышки.
Температура самовоспламенения
При нагревании пробы груза до определенной температуры процесс окисления (горения) начинается без поднесения открытого огня.
Например, груз фенол:
температура вспышки 79°С (с.с.)
температура самовоспламенения 605°С
пределы взрываемости: НПВ=1,5%, ВПВ=10% (об.).
Температура кипения
Температура кипения и давление паров взаимосвязаны: если давление пара превышает атмосферное давление, то жидкость начинает кипеть.
Если внешнее давление становится выше атмосферного, то увеличивается температура кипения.
Если внешнее давление становится ниже атмосферного давления, то понижается температура кипения (см. сравнительную таблицу в пункте «Давление насыщенного пара», представленную ранее).
Электростатические заряды
В процессе перемещения груза под действием сил трения некоторое количество электронов переходит с одного тела на другое. При этом электризуются оба тела, образуя разделенные заряды, которые стремятся вновь соединиться и нейтрализовать друг друга.
Если один из разъединенных материалов или оба материала, несущие заряд, обладают очень низкой электропроводимостью, то повторное соединение зарядов затруднено, и данный материал аккумулирует заряд на себе
Если проводимость материала сравнительно высока, то заряды соединяются очень быстро, тем самым препятствуя накоплению статического электричества. Разряд статического электричества может послужить причиной воспламенения.
Обозначения элементов из таблицы Д.И.Менделеева.
В природе вещества встречаются всегда как смеси. Формула простейшего углеводорода СН4 = газ метан. Углерод С - 4-х валентен, водород Н одновалентен.
Далее углеводороды имеют состав по общей формуле:
где n - количество атомов углерода
Если
-
n=1 - 4 = газы -
n=5 - 19 = жидкости -
n=20 и более = твердые вещества
Во всех случаях температуры кипения и затвердевания тем выше, чем больше молекулярная масса углеводорода, т.е. чем больше количество атомов углерода.
При перегонке нефть разделяют на отличающиеся по температуре кипения фракции:
-
бензины (температура кипения 40-180°С) содержат углероды от С5Н12 до С10Н22.
При повторной перегонке из них могут быть выделены легкие нефтепродукты, кипящие в более узких пределах:
- петролейный эфир (40-70°С)
- авиационный бензин (70-100°С)
- автомобильный бензин (100-120°С) -
керосины (температура кипения 180-270°С) содержат углеводороды от С10Н22 до С16Н34 -
соляровые масла (температура кипения 270-360°С) содержат смеси углеводородов от С12 до С20.
Из них получают смазочные масла и различные виды дизельного топлива -
мазут (нефтяные остатки – до 40-50%) – из него получают тяжелые смазочные масла, вазелин, парафин С22Н46
Изомеры
С увеличением числа С-атомов в молекулах резко возрастает число изомеров предельных углеводородов (т.е. когда атом углерода имеет по одной валентной связи с атомами водорода).
Метан СН4, этан С2Н6 и пропан С3Н8 не имеют изомеров.
Бутанов С4Н10 существует два:
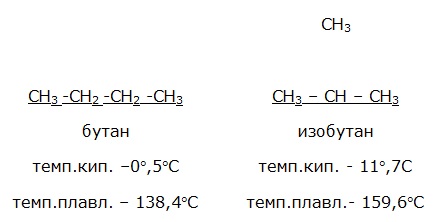
Изомерных пентанов С5Н12 существует 3,
гексанов С6Н12 – 5,
гептанов С7Н16 – 9,
октанов С8Н18 – 18,
нонанов С9Н20 – 35.
Все эти углеводороды получены.
Деканов С10Н22 может быть 75,
формулу С15Н32
могут иметь уже 4 347 изомерных углеводородов.
Кислоты
К кислотам относят вещества, способные отдавать ион водорода.
Кислоты классифицируются по их силе, по основности и по наличию или отсутствию кислорода.
Важнейшие сильные кислоты:
-
азотная НNO3 -
серная H2SO4 -
соляная НСl
По основности, т.е. по числу атомов водорода в молекуле кислоты подразделяются на:
-
одноосновные (НСl, НNO3) -
двухосновные (H2S, H2SO4) -
трехосновные (Н3РО4) и т.д.
Основания
К основаниям относятся вещества, способные присоединять ионы водорода.
Наиболее характерное химическое свойство оснований – их способность взаимодействовать с кислотами с образованием солей.
Химические реакции известных групп
Например, кислота + основание:
Например, основание + кислота: