Добавлен: 07.11.2023
Просмотров: 335
Скачиваний: 4
СОДЕРЖАНИЕ
ОПРЕДЕЛЕНИЯ, ОБОЗНАЧЕНИЯ И СОКРАЩЕНИЯ
Химизм, механизм и кинетика реакций
Технологическое оформление процесса получения МТБЭ
Схема получения МТБЭ IFP показана на рисунке 1.4.
Схема технологии НИИМСК показана на рисунке 1.6.
Описание принципиальной технологической схемы
Принципиальная технологическая схема производства МТБЭ представлена на рисунке 2.1.
Материальный баланс производства
Определение количества образующихся ТМК и ДИБ
Расчет годового материального баланса
Технологический расчет основного оборудования
Геометрические размеры реактора
3 Контрольно-измерительные приборы и автоматизация производства
Схема автоматизации реакторного узла представлена на рисунке 3.1.
Спецификация приборов КИП и А основного реакторного узла представлена в таблице 3.1.
Тепловой баланс реактора
Расчет теплового баланса реактора Р-1 обусловлен вычислением количества несбалансированного тепла, выделяющегося в процессе синтеза и в расчете количества водяного конденсата, необходимого для снятия избытка тепла. Количество вносимого в реактор или уносимого из аппарата тепла находится согласно уравнению
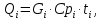 (2.16)
(2.16)где Gi – расход i-го компонента, кг/с; Сpi – теплоемкость i-го компонента,
кДж/(кг∙град); ti – температура, °С.
Для углеводородных компонентов сырья и продуктов реакции теплоемкость определим по формуле
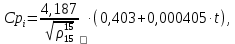 (2.17)
(2.17)где
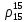 – относительная плотность.
– относительная плотность.Значение
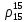 определим по формуле
определим по формуле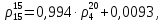 (2.18)
(2.18)где
 - относительная плотность при 20°С. Является справочной величиной.
- относительная плотность при 20°С. Является справочной величиной.Значения плотностей углеводородных компонентов сырья представлены в таблице 2.10.
Таблица 2.10 – Плотности углеводородных компонентов сырья
| Компонент | Плотность, ρ420 | Плотность, ρ1515 |
| Углеводороды С3 | 0,5100 | 0,5162 |
| i-бутилен | 0,5950 | 0,6007 |
| н-бутилен | 0,5945 | 0,6002 |
| i-бутан | 0,5573 | 0,5633 |
| н-бутан | 0,5789 | 0,5847 |
| Бутадиен | 0,6211 | 0,6267 |
| Углеводороды С5 | 0,6262 | 0,6317 |
Значения теплоемкости метанола, третметилкарбинола и МТБЭ являются справочной величиной.
Потери тепла в реакторе принимаются равными 1 % от входящего тепла.
Реакция синтеза МТБЭ протекает с выделением тепла. Тепловой эффект реакции определяется по формуле
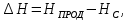 (2.19)
(2.19)где НПРОД и НС – теплоты образования продуктов реакции и исходного сырья соответственно, кДж/моль.
Ввиду малой доли побочных реакций в ходе процесса их влиянием на тепловой эффект пренебрегаем. Теплоты образования метанола, изобутилена и МТБЭ приведены в таблице 2.11.
Таблица 2.11 – Теплоты образования компонентов
| Компонент | МТБЭ | Метанол | Изобутилен |
| Теплота образования, кДж/моль | -291 | -201 | -16,92 |
Таким образом, согласно реакции, по которой протекает процесс, тепловой эффект реакции составит
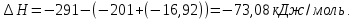
Мольное количество образовавшегося МТБЭ составит
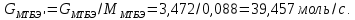
Таким образом, количество тепла, выделившееся в ходе синтеза МТБЭ составит
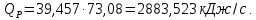
Тепловой баланс реактора представлен в таблице 2.12.
Из таблицы 2.12 видно, что разность входящего и уходящего тепла равняется
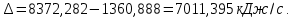
Массовый расход воды, необходимой для снятия избытка тепла процесса, вычисляется по формуле:
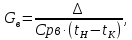 (2.20)
(2.20)где Срв – теплоемкость воды, принимается равной 4,187 кДж/(кг∙К); tН и tК – начальная и конечная температура соответственно охлаждающей воды, °С; принимаем соответственно 20 и 40 °С.
Используя найденные значения, получим
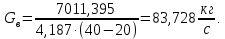
Тепловой баланс реактора представлен в таблице 2.12.
Таблица 2.12– Тепловой баланс реактора
| Компонент | Расход, кг/с | Температура, °С | Теплоемкость, кДж/(кг∙град) | Количество тепла, кДж/с |
| Приход | | | | |
| Углеводороды С3 | 0,017 | 70 | 2,514 | 2,922 |
| i-бутилен | 2,325 | 70 | 2,330 | 379,226 |
| н-бутилен | 0,039 | 70 | 2,331 | 6,323 |
| i-бутан | 3,083 | 70 | 2,406 | 519,386 |
| н-бутан | 0,061 | 70 | 2,362 | 10,067 |
| Бутадиен | 0,006 | 70 | 2,281 | 0,884 |
| Углеводороды С5 | 0,006 | 70 | 2,272 | 0,880 |
| Свежий метанол | 19,120 | 70 | 2,610 | 3493,165 |
| Циркулирующий метанол | 5,883 | 70 | 2,610 | 1074,855 |
| Вода | 0,004 | 70 | 4,187 | 1,051 |
| Тепло реакции | - | - | - | 2883,523 |
| Итого | 7,386 | - | - | 8372,282 |
| Расход | | | | |
| МТБЭ | 3,472 | 70 | 2,511 | 610,313 |
| Непрореагировавший метанол | 0,584 | 70 | 2,61 | 106,700 |
| Непрореагировавший изобутилен | 0,093 | 70 | 2,330 | 15,169 |
| Углеводороды С3 | 0,017 | 70 | 2,514 | 2,922 |
| н-бутилен | 0,039 | 70 | 2,330 | 6,320 |
| i-бутан | 3,083 | 70 | 2,406 | 519,386 |
| н-бутан | 0,061 | 70 | 2,362 | 10,067 |
| Бутадиен | 0,006 | 70 | 2,281 | 0,884 |
| Углеводороды С5 | 0,006 | 70 | 2,272 | 0,880 |
| Диизобутилен | 0,011 | 70 | 2,129 | 1,663 |
| Третметилкарбинол | 0,015 | 70 | 2,771 | 2,860 |
| Потери | - | - | - | 83,723 |
| Итого | 7,386 | - | - | 1360,888 |
- 1 ... 10 11 12 13 14 15 16 17 18
Геометрические размеры реактора
Общий массовый расход сырьевой смеси составляет (таблица 2.9) 26588,645 кг/ч. Объемный расход сырьевой смеси GОБ = 42,204 м3/ч. Требуемая объемная скорость подачи сырья в реактор синтеза ω = 1,5 ч-1. [6]
Нужный объем реакционной зоны определяется по уравнению
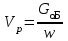 (2.21)
(2.21)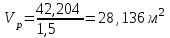
Используем шестиугольное расположение труб в аппарате и следующие характеристики реактора:
- внутренний диаметр трубок dВН = 0,1 м;
- толщина стенок δ = 0,01 м;
- наружный диаметр трубок dН = 0,12 м;
- кольцевой зазор между крайними трубками и корпусом k = 0,01 м;
- длина трубок l = 12 м.
Условное размещение труб в решетке приведена на рисунке 2.2.
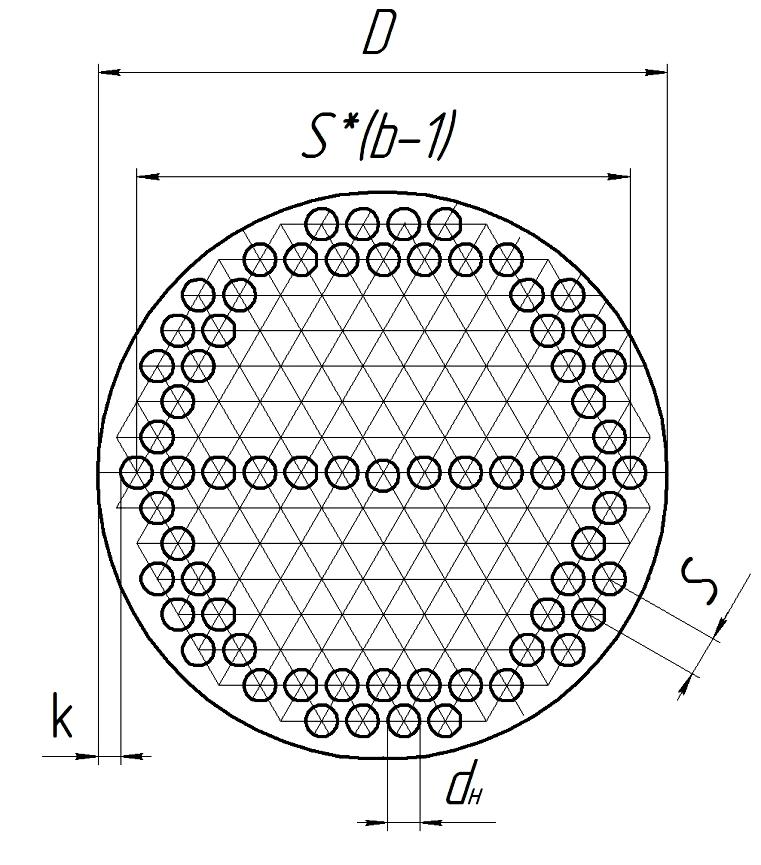
Рисунок 2.2 – Схематичное размещение труб в решетке реактора
Объем одной трубки находим по формуле
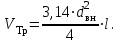 (2.22)
(2.22) 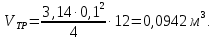
Необходимое количество трубок находится по следующей формуле
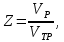 (2.23)
(2.23)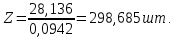
Возьмём с запасом количество трубок в реакторе равным Z = 300 штук.
Шаг трубок определяется по формуле
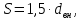 (2.24)
(2.24)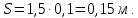
Связь между числом трубок на стороне наибольшего шестиугольника (а) и общим числом трубок (Z) определяется уравнением
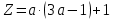 (2.25)
(2.25)При количестве трубок Z = 300, а = 9 шт.
Число труб, размещенных на диагонали наибольшего шестиугольника, вычисляется по формуле
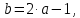 (2.26)
(2.26)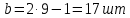 .
.Диаметр реактора находим по формуле