ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 07.09.2021
Просмотров: 1216
Скачиваний: 3
При заживлении в лимфатических узлах наблюдаются рассасывание перифокального воспаления, уплотнение казеоза, отложение солей кальция в казеозе, нарастание фиброзных изменений в капсуле и окружающей прикорневой области.
Первичный туберкулез может проявляться формированием в легком первичного туберкулезного очага. Этот очаг имеет пневмонический характер с казеозом в центре и широкой перифокальной зоной воспаления снаружи. Вслед за формированием легочного аффекта отмечается поражение регионарных лимфатических узлов с «дорожкой» из измененных лимфатических сосудов между ними.
Рис.
1.4. Первичный комплекс в легком ребенка.
ЗГистотопограмма.
Окраска гематоксилином и эозином.
Это соответствует картине первичного комплекса с его тремя составными компонентами (рис. 1.4).
При заживлении перифокальное воспаление рассасывается, казеоз в очаге уплотняется, откладываются соли кальция, а вокруг очага формируется соединительнотканная капсула. Может произойти полное замещение казеозного очага фиброзом. В лимфатических узлах преобладают процессы инкапсуляции и обызвествления казеозных масс.
В случае прогрессирования первичного комплекса пневмонический фокус увеличивается в размерах, подвергается казеинфикации с формированием острых пневмониогенных каверн. Вокруг каверны затем формируется соединительнотканная капсула, и процесс переходит в фиброзно-кавернозный туберкулез.
Прогрессирующее течение первичного туберкулеза может проявиться в виде милиарного туберкулеза в результате «прорыва» инфекции в кровеносное русло. Важно помнить о возможности острой диссеминации инфекции; необходимо своевременно диагностировать подобные случаи, так как рано начатое лечение дает хороший эффект.
Следовательно, периоду первичного заражения наряду с распространением инфекции по лимфатическим путям присущи и гематогенные отсевы, характеризующие бациллемию с возникновением очагов специфического воспаления в различных органах и тканях. Очаги-отсевы в легких, формирующиеся в различные периоды первичного туберкулеза, нередко являются случайной находкой при рентгеноанатомическом обследовании людей, не страдающих активными формами туберкулеза. Такие очаги состоят из казеоза, окруженного фиброзной капсулой, бедной клеточными элементами. Очаги, как правило, множественные, располагаются в верхних сегментах легких под плеврой. С обострения процесса в этих очагах начинается вторичный туберкулез, характеризующийся локальным поражением органа. Таким образом, послепервичным очагам принадлежит большое значение в патогенезе вторичного туберкулеза.
1.3.3. Диссеминированный туберкулез
Кассификация диссеминированного туберкулеза легких объединяет диссеминации различного генеза: лимфогенные, гематогенные, бронхогенные.
Гематогенный и лимфогематогенный туберкулез по своему генезу занимают промежуточное положение между первичным и вторичным туберкулезом, часто возникая из различных очагов первичного комплекса. Для появления гематогенной диссеминации туберкулеза недостаточно попадания микобактерии туберкулеза в кровеносное русло, необходима еще сенсибилизация сосудистой стенки и всего организма. При острой гематогенной диссеминации, при милиарном туберкулезе наиболее распространенными являются продуктивные бугорки. Важное значение имеют и состояние возбудителя, появление различных форм его персистирования. Специфическая химиотерапия способствует быстрому рассасыванию воспалительных очагов, при этом на месте бугорков формируются звездчатые соединительные рубчики или незначительно утолщается строма легкого.
Хронические формы диссеминированного туберкулеза чаще встречаются у взрослых, и диссеминация имеет обычно лимфогематогенный характер. В генезе этих форм может быть туберкулезное поражение лимфатических узлов, из которых по лимфатическим путям ретроградно происходит рассеивание инфекции с последующим прорывом в сосудистое русло и формированием очагов в легких. Эти формы обычно ограничиваются поражением легочной ткани, хотя возможны и гематогенные отсевы в другие органы. Очаги, как правило, имеют продуктивный характер, локализуются преимущественно в верхушечных сегментах легкого, характеризуются значительным уменьшением диссеминации в нижних отделах легких. Очаги диссеминации обычно полиморфны: одни из них инкапсулированы, другие отличаются отсутствием хорошо выраженной капсулы, что свидетельствует о волнообразном течении процесса. Очаги локализуются по ходу утолщенной соединительнотканной стромы
Рис.
1.5. Хронический гематогенно-диссеминированный
(мелкоочаговый) туберкулез легких.
Гистотопограмма. Окраска гематоксилином
и эозином.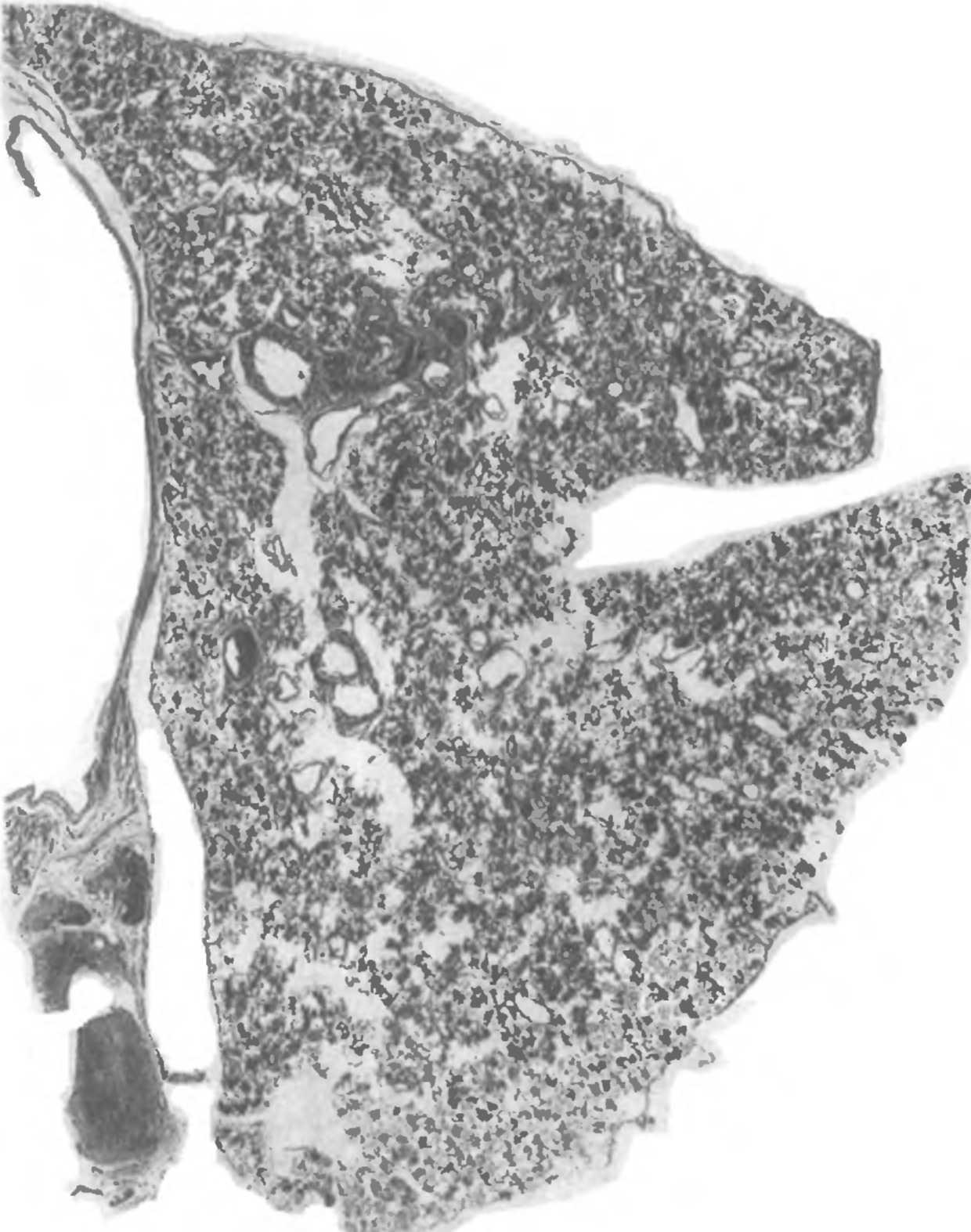
легкого, в периваскулярной или перибронхиальной ткани. Некоторые из них располагаются непосредственно в стенке кровеносных сосудов. Вокруг очагов обычно развивается эмфизема. В поздние фазы процесса развивается интерстициальный сетчатый склероз, особенно выраженный в верхних отделах легкого. В последних наряду с поражением интерстициальной ткани наблюдается образование массивных фиброзных рубцов на месте бывших туберкулезных очагов. В легочной ткани на фоне эмфиземы и фиброзных изменений могут быть инкапсулированные казеозные очаги, четко отграниченные от окружающей ткани (рис. 1.5).
Хронический гематогенно-диссеминированный туберкулез легких может осложняться формированием своеобразных каверн округлой формы, располагающихся в симметричных отделах легких, — «штампованные» каверны. Они отличаются тонкими стенками со слабо-выраженным фиброзом, внутренняя поверхность их обычно очищена от казеозно-некротических масс, слой специфических грануляций неширокий, пронизан кровеносными и лимфатическими сосудами. При возникновении каверн в патологический процесс вовлекаются бронхи, и туберкулез может осложняться бронхогенной диссемина-цией.
Рис.
1.6. Очаговый
туберкулез
легких. Гистотопограмма. Окраска
гематоксилином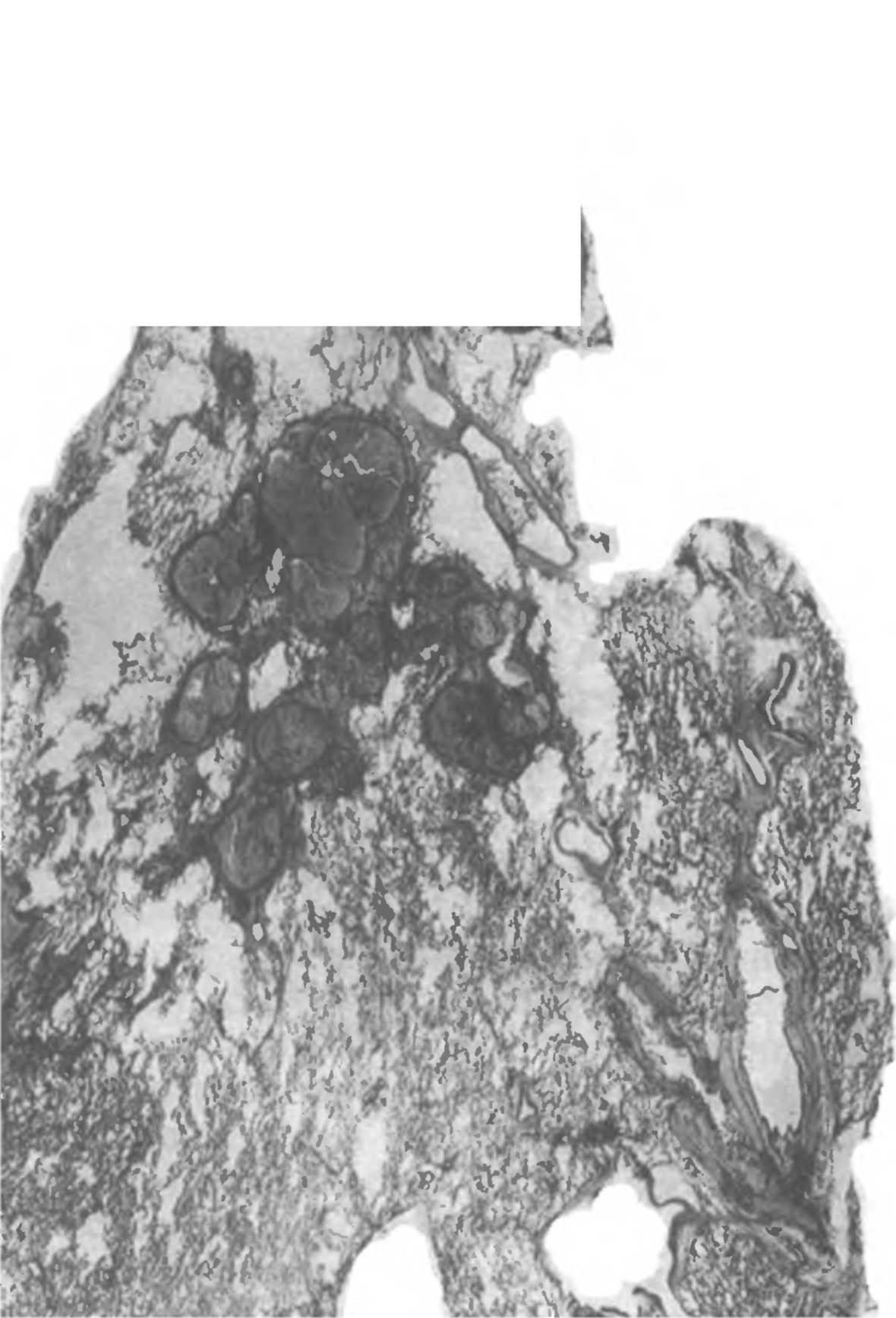
При развитии бронхогенного туберкулеза, локализующегося главным образом в нижних отделах легких, могут образоваться сливные очаги бронхолобулярной пневмонии. В последующем эти очаги распадаются и образуются острые бронхогенные каверны.
1.3.4. Очаговый туберкулез
Очаговый туберкулез является одной из наиболее распространенных форм туберкулеза. Эта форма связана с образованием очагов-отсевов или очагов реинфекта, возникающих чаще всего эндогенно при лимфогенном рассеивании туберкулезной инфекции из очагов первичного туберкулеза. В последующем очаги-отсевы ведут к образованию новых, более свежих очагов в непосредственной близости от ранее возникших. В связи с этим очаговый туберкулез характеризуется наличием целой группы очагов казеоза, локализующихся преимущественно односторонне, чаще справа в верхней доле субплеврально.
Очаги располагаются среди фиброзированной стромы легкого, утолщенной плевры и междольковых перегородок, что указывает на их лимфогенный генез [Штефко В. Г., 1936; Иванова М. Г., 1939] (рис. 1.6). Одни очаги характеризуются хорошо выраженной капсулой, бедной клеточными элементами, и уплотненным казеозом, иногда даже частично фиброзированным; другие очаги более «свежие», казеоз в них окружен зоной из макрофагов, эпителиоидных и лимфоидных клеток с гигантскими клетками между ними. Капсула вокруг таких очагов выражена слабо, фиброзные волокна в ней инфильтрированы лимфоидными клетками. Рядом могут располагаться совсем «свежие» казеозные очаги, окруженные широкой клеточной зоной. Лимфоцитарная инфильтрация в таких очагах без четкой границы переходит на окружающую ткань.
Распространение процесса чаще всего происходит по лимфатическим путям, реже контактным путем и еще реже — по бронхам и кровеносным сосудам [Ильина Т. Я., 1982]. Заживление очагов происходит обычно посредством их инкапсуляции, уплотнения ка-зеоза и частичного его замещения соединительной тканью, врастающей в казеоз со стороны капсулы. Обострение процесса выражается в нарастании воспалительных изменений в капсуле очагов и окружающей их легочной ткани с образованием так называемого инфильтрата. Обострение процесса может проявляться расплавлением казеоза в одном из очагов с формированием вначале щелевидной, а затем и более крупной полости. Исходом очагового туберкулеза при благоприятном течении процесса является развитие фиброза как в очагах, так и вокруг них.
1.3.5. Инфильтративный туберкулез
Инфильтративный туберкулез обычно возникает при обострении очагового туберкулеза. При этом чаще всего в 1 или 11 бронхоле-гочных сегментах появляется уплотнение с диаметром 2—3 см. В его центре определяются мелкие очаги казеоза, вокруг последних образуется зона перифокального воспаления. При благоприятном течении процесса происходят рассасывание перифокального, преимущественно неспецифического, воспаления, отграничение и уплотнение казеозных очагов, их инкапсуляция и обызвествление, фиброзные изменения в прилежащих участках легкого (рис. 1.7).
При прогрессировании инфильтративного туберкулеза очаги казеоза в его центральных отделах увеличиваются, так же как и зона перифокального воспаления, которая может занять всю долю легкого по типу лобита [Струков А. И., Соловьева И. П., 1976]. Наряду с участками казеоза, окруженными эпителиоидными, лимфоидными и гигантскими клетками, имеются участки воспаления, в которых просветы альвеол заполнены фибрином, клетками десквамирован-ного альвеолярнго эпителия и альвеолярными макрофагами, а также экссудатом. Расплавление казеоза в очаге и прорыв казеозных масс в бронхи ведут к образованию на месте инфильтрата острой каверны.
Наряду с патоморфологической картиной инфильтрата представим
Рис
1 8 Крупная туберкулема в легком с
разрушением стенки прилежащего бронха
Гистотопограмма
Окраска гематоксилином и эозином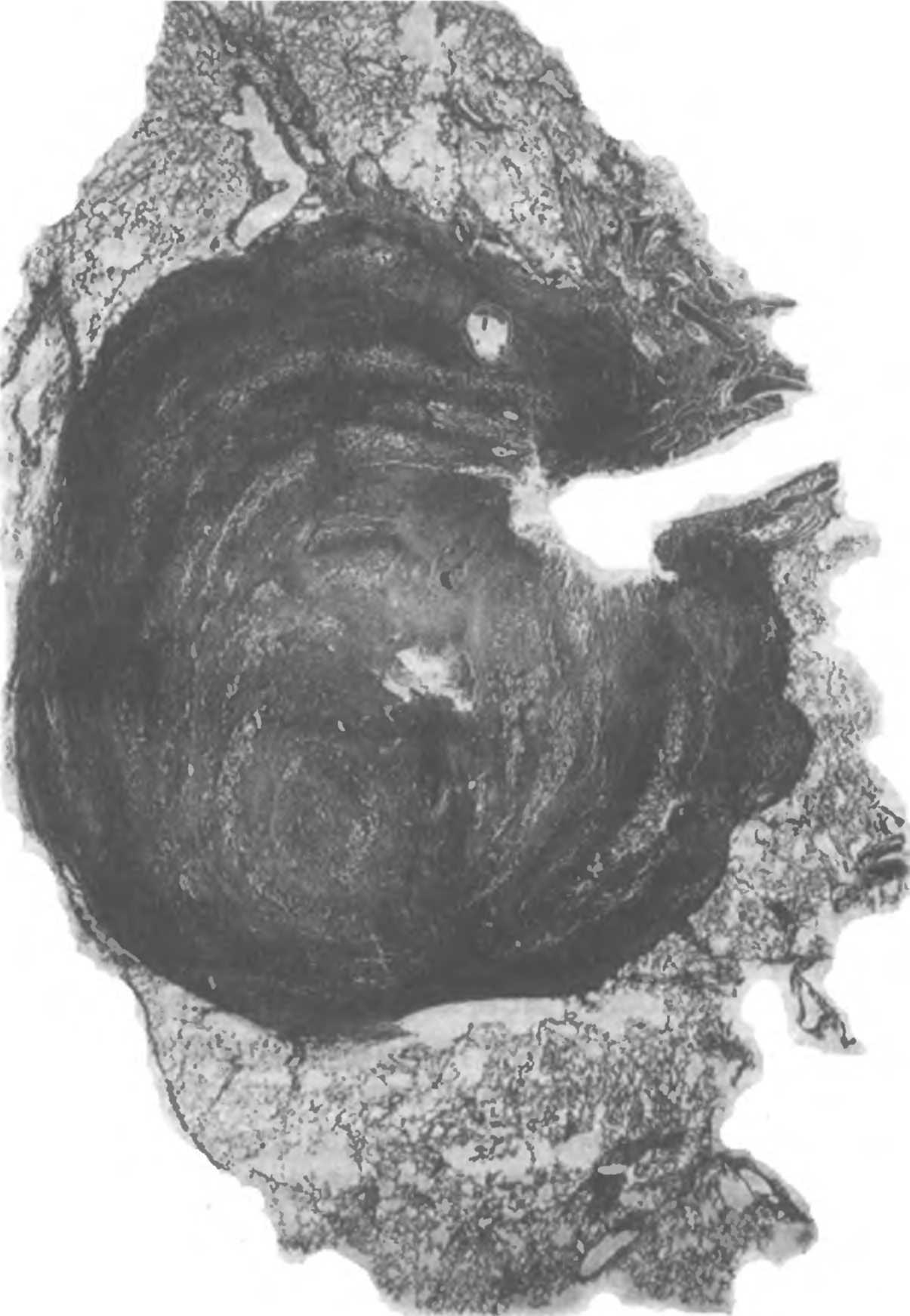
больше 1 см. В связи со значительным учащением формирования таких очагов в клинике они были выделены в отдельную форму. Их возникновение связывают с гиперергической реакцией организма на микобактерии туберкулеза [Авербах М. М., 1969]. Туберкулемы чаще бывают одиночными, реже множественными, с диаметром 2—4 см, располагаются они преимущественно в I—II сегменте легкого [Авербах М. М., 1969].
Туберкулемы делят на солитарные, слоистые, конгломератные и инфильтративно-пневмонические, Солитарная гомогенная туберкулема (казеома — по Л. К. Богушу) представляет собой очаг казеозной пневмонии округлой формы, четко отграниченный от окружающей легочной ткани тонкой фиброзной капсулой. На границе последней с казеозом имеется узкий слой специфических грануляций. При специальном окрашивании в казеозах удается выявить остатки стро-мы легкого, что подтверждает их возникновение из очага специфической пневмонии. В казеозе могут также определяться остатки более старых туберкулезных очагов, вокруг которых и произошло
Рис
17
Инфильтративный туберкулез легких
В центре определяется казеоз
Гистотопограмма
Окраска гематоксилином и эозином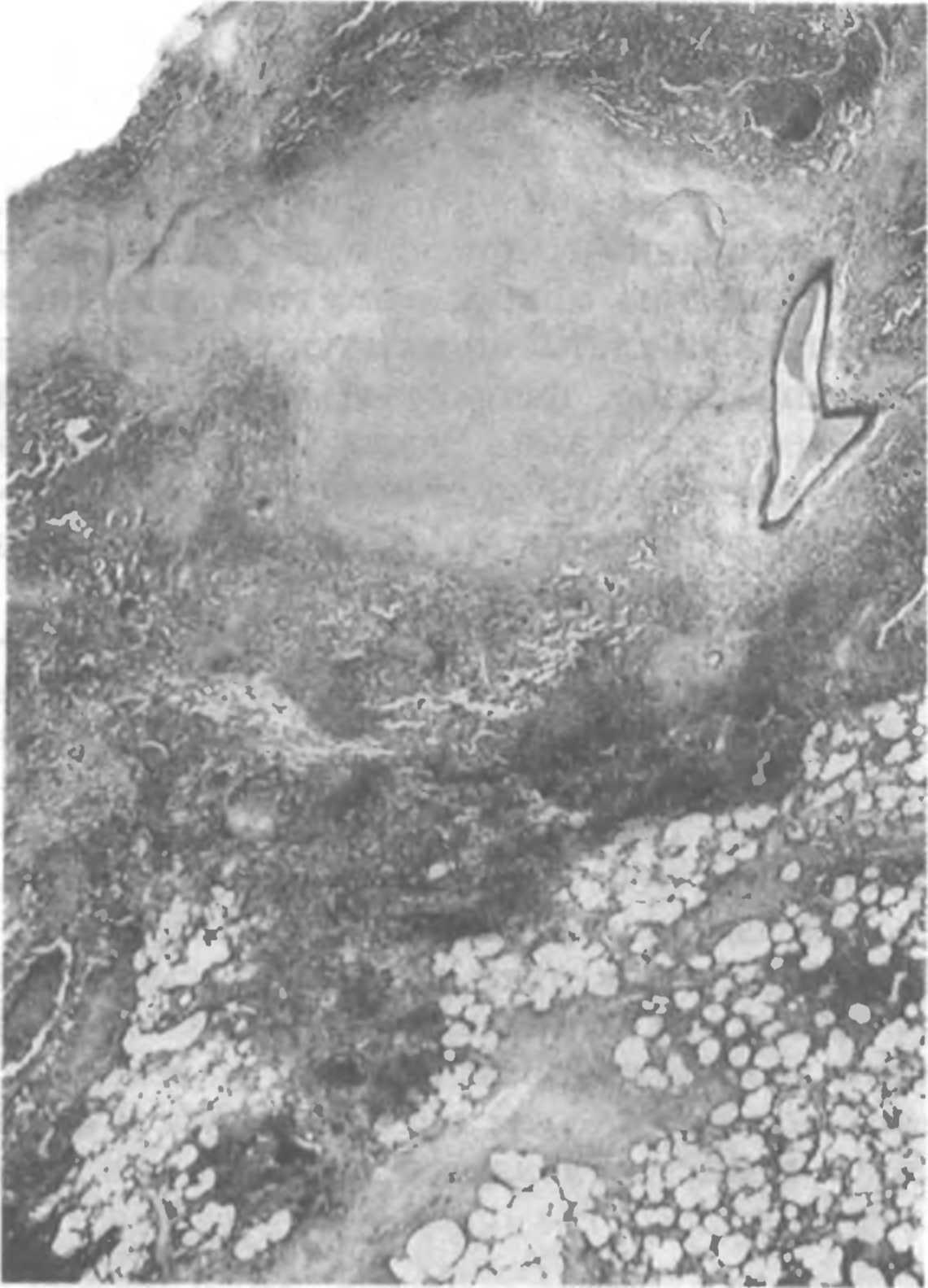
данные о казеозной пневмонии. Для такой пневмонии характерно преобладание острого казеозного распада. Различают ацинозную форму казеозной пневмонии, при которой поражение ограничивается пределами ацинуса, лобулярную казеозную пневмонию, когда процесс захватывает дольки легкого, и лобарную форму, когда в процесс вовлекается целая доля легкого. При лобулярной форме казеозно измененные дольки могут сливаться, формируя сегментарные, лобарные очаги и приводя к тотальной казеозной пневмонии. Лобарная казеозная пневмония является наиболее тяжелой формой туберкулеза. Большая часть пораженной доли в этих случаях оказывается занятой казеозом, в котором могут наблюдаться расплавление казеоза и образование острых полостей распада. В современных условиях казеозная пневмония отличается отграничением процесса по периферии казеозного фокуса или наоборот острым, обширным расплавлением казеоза с формированием множественных полостей распада.
1.3.6. Туберкулема
К этой форме туберкулеза относятся разнообразные по генезу инкапсулированные казеозные очаги округлой формы с диаметром обострение процесса (рис. 1.8). На границе туберкулемы с окружающей легочной тканью обычно выявляются лимфоцитарные скопления, свидетельствующие о выраженности иммунных реакций в легких. Слоистые туберкулемы отличаются концентрическим расположением казеозных масс и коллагеновых волокон. Зона специфической грануляционной ткани очень узкая, местами отсутствует, фиброзная капсула тонкая, но выражена четко. Конгломератная туберкулема имеет обычно неправильно округлую форму и состоит из нескольких казеозных очагов различного размера, объединенных одной общей капсулой. Туберкулема инфильтративно-пневмониче-ского типа представляет собой нечетко отграниченное округлое или неправильной овальной формы образование, в котором участки творожистого некроза чередуются с фокусами туберкулезного воспаления гранулематозного типа и участками пневмонии полиморфного типа.
К туберкулемам иногда относят заполненные каверны, в которых в связи с облитерацией дренирующего бронха происходит скопление казеозно-слизистых масс и они приобретают округлую форму. В отличие от истинных туберкулем в их казеозных массах отсутствуют элементы стромы легкого, капсула их значительно толще за счет более широкого слоя грануляционной ткани и фиброза.
При прогрессировании туберкулемы она может увеличиваться в размерах, казеоз в ней подвергается расплавлению, воспалительный инфильтрат переходит на прилежащие бронхи, в просвет которых выделяются расплавляющиеся казеозные массы. В этих случаях на месте туберкулемы образуется каверна.
При стабилизации туберкулемы или ее заживлении наблюдаются рассасывание перифокального воспаления, нарастание в капсуле процессов трансформации специфической грануляционной ткани в неспецифическую фиброзную ткань, проникающую в казеоз и его замещающую.
1.3.7. Деструктивный туберкулез легких
Любая форма туберкулеза может осложниться расплавлением казеоза, выделением казеозных масс через бронхи и формированием полости, т. е. переходом процесса в деструктивную форму. Сформированная каверна характеризуется трехслойным строением стенок: внутренний казеозно-некротический слой; слой специфических грануляций, содержащий макрофаги, эпителиоидные, лимфоидные и гигантские клетки Пирогова—Лангханса; наружный фиброзный слой, граничащий с окружающей легочной тканью, состоящий из волокон соединительной ткани, инфильтрированных лимфоидными клетками, и содержащий в большем или меньшем количестве кровеносные и лимфатические сосуды. Казеозно-некротические массы и туберкулезные грануляции со стенок каверн переходят на стенки дренирующих бронхов.
По генезу каверны могут быть пневмониогенными, образующимися на месте очага туберкулезной пневмонии, бронхогенными, формирующимися на месте пораженных туберкулезом бронхов, гематогенными, возникающими при гематогенно-диссеминированном туберкулезе [Штефко В. Г., 1938; СтруковА. И., 1948; Пузик В. И. и др., 1973]. По величине диаметра каверны различают: малые — до 2 см, средние — от 2 до 4 см, большие — от 4 до 6 см, гигантские — более 6 см [Струков А. И., 1959]. При заживлении каверн наблюдаются отторжение казеозно-некротического слоя, уменьшение просвета полости за счет сморщивания стенок, разрастания грануляционной ткани и фиброза. В конечном итоге на месте каверны может образоваться рубец, в центре которого иногда имеется небольшая остаточная полость, выстланная эпителием и содержащая прозрачную жидкость.
В процессе заживления каверны просвет дренирующих бронхов может облитерироваться, и в таком случае на месте каверны образуется инкапсулированный очаг казеоза типа туберкулемы. При заживлении каверна может трансформироваться в кистоподобную полость.
Процесс этот длительный, и в стенках подобных каверн долгое время могут сохраняться участки специфической грануляционной ткани. При развитии в каверне процессов заживления большое значение имеет состояние крово- и лимфообращения, особенно в системе микроциркуляции — как в стенках каверны, так и окружающей ее легочной ткани [Штефко В. Г., 1938; Пузик В. И. и др., 1973; Струков А. И., Соловьева И. П., 1976; Ерохин В. В., 1987, и др.].
При отграничении каверны, стабилизации патологического процесса (особенно при применении противотуберкулезных препаратов) полиморфные, пневмонические участки вокруг каверны рассасываются, нарастают фиброзные изменения, «тянущиеся» от фиброзного слоя стенки каверны в окружающую легочную ткань. В такой каверне обычно выявляется большое количество разной величины лимфоцитарных скоплений и узелков, располагающихся между соединительнотканными волокнами капсулы.
Прогрессирование деструктивного туберкулеза выражается в увеличении казеозно-некротического слоя, который может переходить на слой специфической грануляционной ткани и фиброза. В окружающей легочной ткани наблюдается перифокальное воспаление, формируются очаги специфической пневмонии. Прогрессируют изменения и в бронхах с появлением очагов острой бронхогенной диссеминации.
Кавернозный туберкулез легких выделен в отдельную форму. Он характеризуется наличием изолированной сформированной каверны без выраженных фиброзных изменений в ее стенках и окружающей легочной ткани. Чаще всего каверна располагается в одном бронхоле-гочном сегменте. Казеозно-некротический слой в ее стенках тонкий, а основную часть стенки составляет грануляционный слой, богатый лимфоидными клетками и микрососудами. В связи с отсутствием выраженного фиброза в стенках такой каверны она может под влиянием лечения спадаться и заживать рубцом. Заживление может также про-
(включая
и измененные формы микобактерии
туберкулеза), мор-фофункциональная
неполноценность макрофагов и
незавершенность фагоцитоза, нарушение
процессов фибриллообразования,
недостаточность сурфактантной
системы легких и др. [Ерохин В. В.,
Ель-шанская М. П., 1986].
Цирротический туберкулез легких характеризуется развитием в легочной ткани грубого, деформирующего орган склероза (цирроза), бронхоэктатических, носткавернозных (типа кист) полостей, эмфи зематозных булл или каверн без признаков прегрессирования. Между
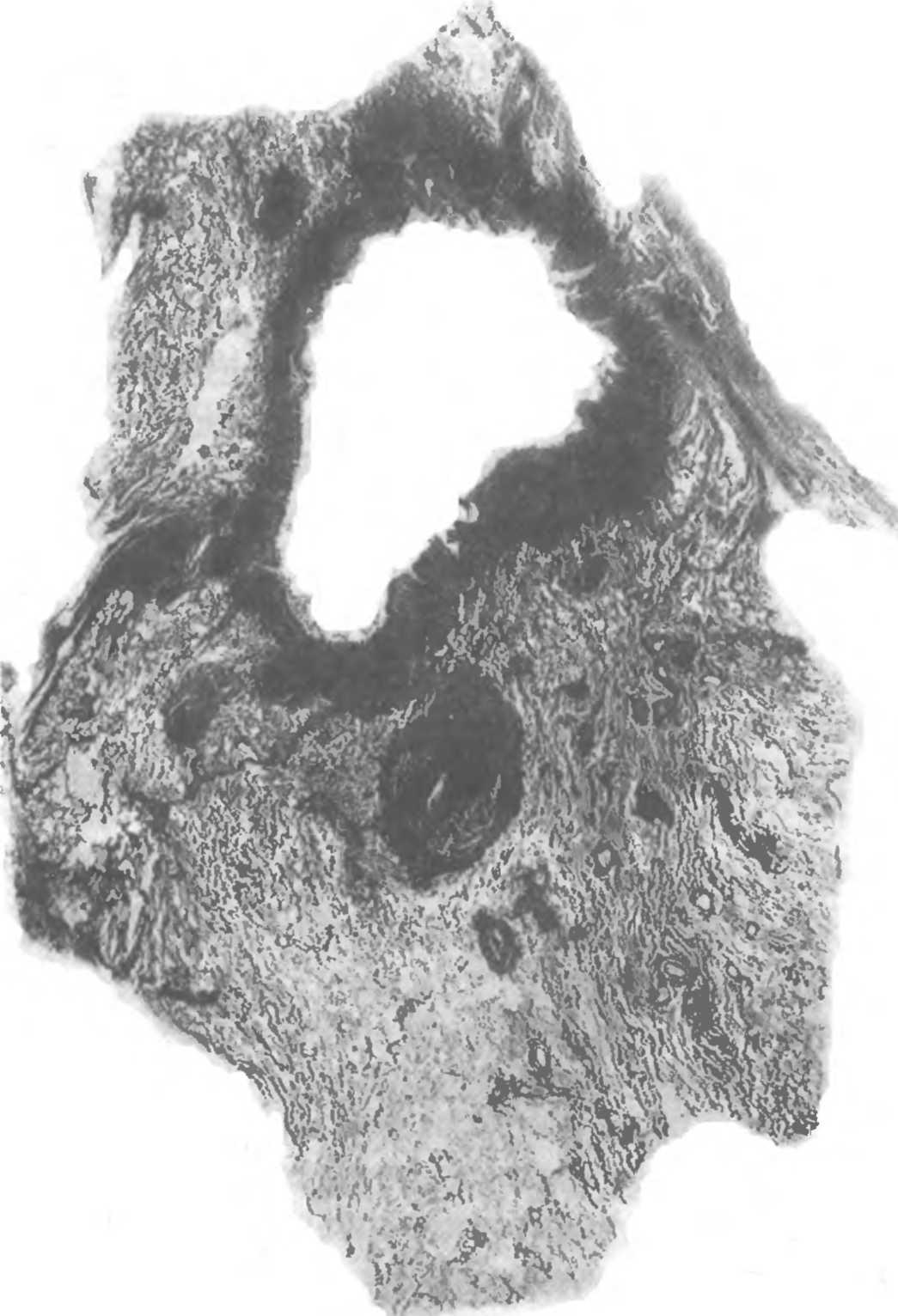
Рис 19 Кавернозный ту беркулез
Гистотопограмма Окраска ге-
матоксилином и эозином
исходить по типу очищения внутренней поверхности каверны и перехода ее в кистоподобную полость (рис. 1.9).
Фиброзно-кавернозный туберкулез характеризуется наличием в одном или в обоих легких каверны или каверн, расположенных среди фиброзно измененной легочной ткани. В стенках каверн в отличие от кавернозного туберкулеза фиброзный слой, как правило, резко выражен и превалирует над казеозно-некротическим и грануляционным (рис. 1.10). Вблизи каверн обычно имеются очаги бронхогенной диссеминации, инкапсулированные или свежие.
Отличительной особенностью бронхогенных диссеминации в настоящее время является их четкое отграничение от окружающей ткани, препятствующее переходу процесса на альвеолы. Однако в условиях недостаточности иммунитета процесс может принять остропрогрессирующий характер. При этом появляются очаги своеобразной полиморфной пневмонии, казеоз, формируются острые полости распада с тонкими, плохо сформированными стенками и большой пери фокальной реакцией
Фиброзно-кавернозный туберкулез отличается волнообразным течением, в период стабилизации или затихания процесса нарастают явления фиброза и деформации легочной ткани. Фиброз препятствует циркуляции крови и лимфы, разрушает сосуды микроцирку-
Рис
1 10
Фиброзно-кавернозный туберкулез
Гистотопограмма
Окраска гематоксилином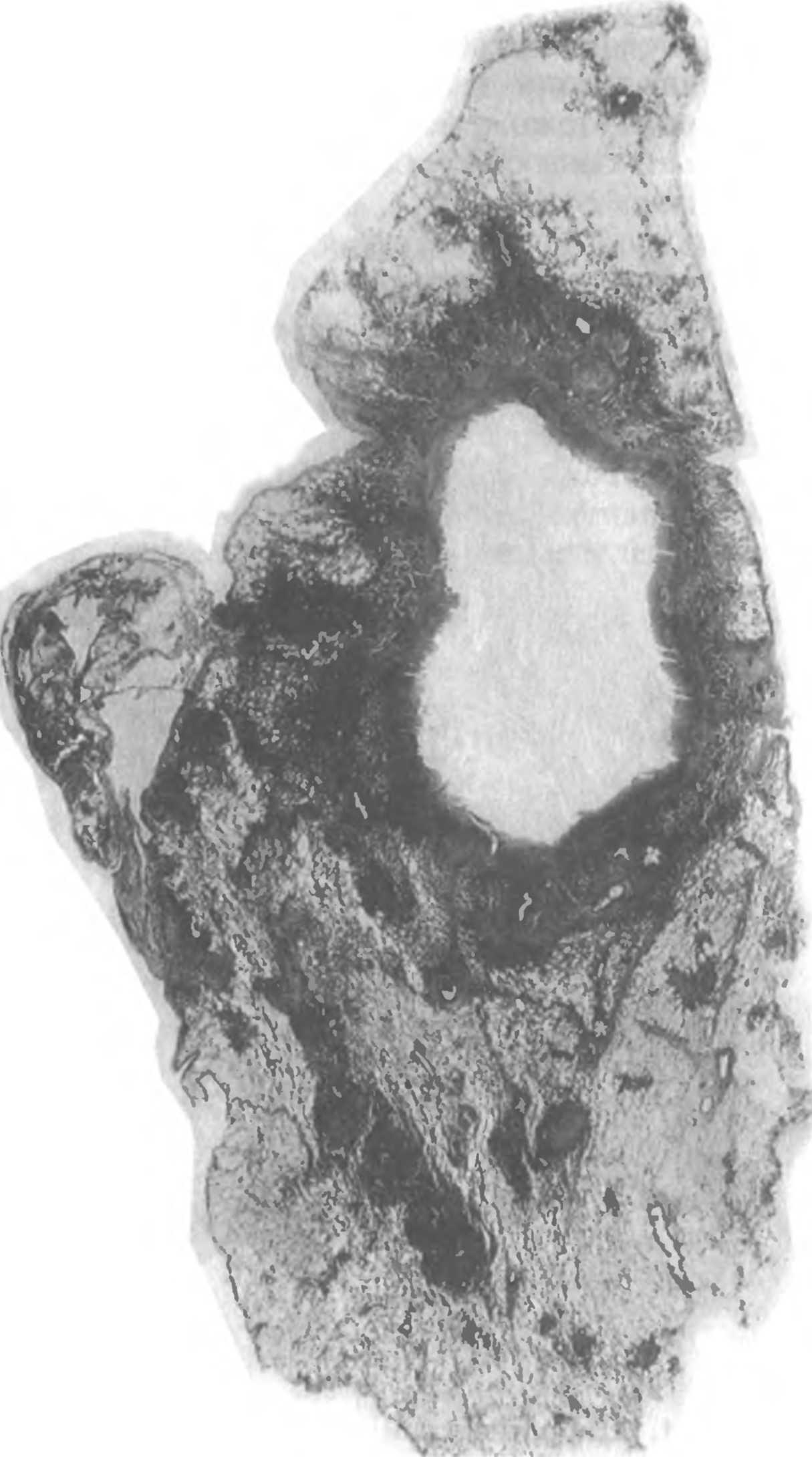
ляторного русла, ухудшает условия микроокружения клеток грануляционной ткани, при фиброзе снижается функциональная активность макрофагов. Изменения в корне легких, плевре и окружающей легочной ткани препятствуют спадению и рубцеванию полостей. Поэтому только каверны малых размеров могут заживать с развитием рубца. Крупные фиброзные каверны чаще заживают по типу очищения их стенок и формирования кистоподобной полости. Установлены основные причины, затрудняющие развитие процессов заживления в стенке каверны: наличие антигенного раздражителя
2-1213
33
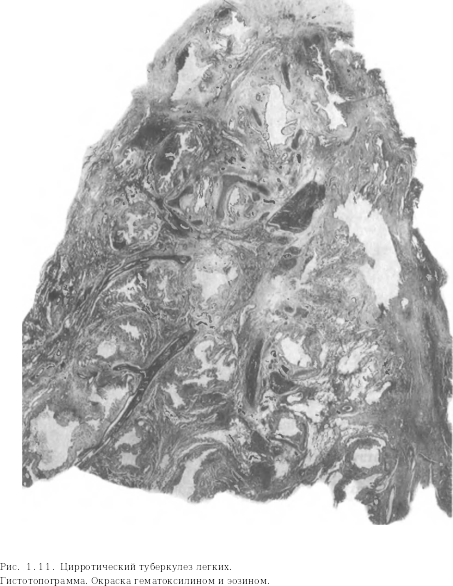
рубцами могут определяться туберкулезные очаги разного размера и строения. Цирротически измененное легкое резко деформировано, уменьшено в объеме, плотное. Плевра утолщена, иногда значительно, панцирем покрывает все легкое, в ней может происходить окостенение. В связи с наличием массивных фиброзных тяжей воздушность легочной ткани резко снижена, участки ателектаза чередуются с участками эмфиземы. Резко деформировано бронхиальное дерево, имеются бронхоэктазы различных размеров и формы. В кровеносных сосудах наблюдаются перестройка с перекалибровкой их просвета, появление сосудов замыкающего типа и множества зияющих артериовенозных анастомозов.
В стенках расширенных бронхов, бронхоэктатических полостей и очищенных каверн обычно выражено неспецифическое воспаление. При значительном склерозе и отсутствии при нем активных туберкулезных изменений имеется цирроз легкого как последствие перенесенного туберкулеза (рис. 1.11).
ГЛАВА 2
ИММУНОЛОГИЯ И ГЕНЕТИКА
Туберкулез — хроническое инфекционное заболевание, протекающее с внутриклеточным (в макрофагах) паразитированием микобактерии. Несмотря на самую современную химиотерапию, лечение туберкулеза, как правило, бывает длительным и не всегда эффективным. Одной из причин случаев безуспешного лечения по общепринятому мнению является недостаточная эффективность защитных механизмов, в значительной мере генетически обусловленная.
Взаимодействие микроорганизма и возбудителя при туберкулезе — это классический пример внутриклеточной инфекции. Ее характерными чертами являются недостаточность собственных бактерицидных систем макрофагов для элиминации микобактерии, необходимость иммунологического усиления активности макрофагов с помощью медиаторов, синтезируемых Т-лимфоцитами, отсутствие прямого или опосредованного (через разные типы клеток) бактерицидного действия антител. При этом существенные особенности инфекции связаны с преимущественно аэрогенным путем заражения и длительным течением заболевания, особенно при его хронических формах, сопровождающихся антигенемией и интоксикацией.
Существует огромное число работ, в которых была изучена роль различных иммунологических феноменов при туберкулезе и их генетический контроль. Этому есть много объективных причин.
-
Туберкулез хорошо моделируется на экспериментальных животных (в том числе на линейных мышах).
-
Туберкулез у человека представляет собой хроническое инфекционное заболевание, имеющее, вероятно, самое широкое распространение в мире среди хронических бактериальных инфекций.
-
Клиническая и морфологическая картина туберкулеза полиморфна, и разным формам и особенностям его течения соответствуют различные иммунологические характеристики.
-
Туберкулез является классической моделью, на которой уже в течение почти 100 лет изучают один из важнейших феноменов иммунитета — гиперчувствительность замедленного типа (ГЗТ).
-
Микобактерии туберкулеза обладают известным адъювантным действием, и при изучении иммунного ответа на те антигены, которые вводятся в адыованте, как правило, исследуют и иммунный ответ на компоненты микобактерии. Этот как бы «побочный продукт» подобных исследований дал очень много для понимания природы иммунного ответа при туберкулезе.
2.1. ИММУНОЛОГИЧЕСКИЙ СТАТУС БОЛЬНЫХ ТУБЕРКУЛЕЗОМ, ВОПРОСЫ ПРОГНОЗА И ИММУНОДИАГНОСТИКИ
По аналогии со «спектром» лепры описан «спектр» проявлений туберкулеза у человека, определенный на основании клинических, бактериологических, иммунологических и гистологических данных
[Lenzini LM 1977; Turk J., 1979; Ellner J., 1986]. Этот «спектр» включает 4 формы.
-
Реактивная форма — микроочаговый, ограниченный туберкулез. При этой форме в 100% случаев определяются типичные реакции замедленного типа на туберкулин (ГЗТ) и отсутствуют ранние (РР) и смешанные (CP) реакции на туберкулин, наблюдается выраженное подавление миграции лейкоцитов (ПМЛ), гуморальные антитела к PPD выявляются редко (5% случаев). Микобактерии не определяются ни в мокроте, ни в тканях. Реакции в зародышевых центрах лимфатических узлов и в других регионах, где находятся плазматические клетки, слабые, а в паракортикальных зонах, где локализуются Т-лимфоциты, — выраженные. Эффект лечения этой формы достигает 100%.
-
Промежуточная реактивная форма — очаговый или микроочаговый, ограниченный кавернозный туберкулез, односторонняя или двусторонняя лимфоаденопатия, туберкулезный серозит. ГЗТ положительна в 30%, РР — в 10—15% и CP — в 50—60% случаев. ПМЛ выражено в меньшей степени, чем при реактивной форме, гуморальные антитела к PPD определяются в 70% случаев, микобактерии в мокроте не выявляются, а в тканях обнаруживаются редко. Реакция плазматических клеток слабая, а з пара-кортикальной зоне выраженная, но в меныпй степени, чем при реактивной форме. Антибактериальное лечение эффективно в 90% случаев.
-
Промежуточная ареактивная форма — хронический распространенный фиброзно-кавернозный туберкулез, туберкулезная лимфоаденопатия, осложнения образованием свищей. ГЗТ положительна примерно в 5%, РР — в 15%, CP — в 80% случаев, ПМЛ положительна очень редко, гуморальные антитела против PPD определяются почти в 100% случаев, микобактерии в мокроте выявляются в большинстве случаев, а в тканях — всегда, реакция плазматических клеток выраженная, а в паракортикальных зонах слабая. Эффективное излечение удается только в 30% случаев.
-
Ареактивная форма — острый милиарный туберкулез. Все виды туберкулиновых реакций отрицательные, как и ПМЛ, гуморальные антитела к PPD и микобактерии в мокроте и тканях обнаруживаются в 100% случаев, реакция плазматических клеток слабая, а в паракортикальных зонах отсутствует. Антибактериальное лечение неэффективно.
Хотя эта классификация в принципе отражает соотношение разных клинических, морфологических, микробиологических и иммунологических параметров, однако значительное число случаев туберкулеза в нее не укладывается. М. М. Авербах и соавт. (1990) на основании анализа результатов собственных исследований и данных литературы суммировали (разумеется, условно) спектр нарушений иммунитета при туберкулезе (табл. 2.1)
Изучение иммунологического статуса больных туберкулезом необходимо для решения ряда практических задач: 1) диагностики и дифференциальной диагностики туберкулеза; 2) выявления нару-
Таблица 2.1. Характеристика нарушений иммунологической реактивности у больных и влияние этих нарушений на течение туберкулезного процесса
Иммунологическая характеристика
Клинический статус
-
Отсутствие изменения соотношения Т- и В-лимфоцитов, Тх/Тс и нарушений функции Т- и В-клеток (по их реакции иа ми-тогеиы, кожным пробам, уровню иммуноглобулинов) . Выраженная кожная ГЗТ и реакции in vitro на антигены микобактерии, противотуберкулезные антитела определяются в разных титрах. Уровень комплемента (С) в норме, число и функция нейтрофилов и макрофагов не изменены
-
Умеренные нарушения специфического клеточного иммунитета (подавление реакции in vitro иа фоне сниженной или отсутствия кожной ГЗТ на антигены микобактерии). Уровень противотуберкулезных антител может быть высоким или средним. Число Т-лимфоцитов и их функция умеренно снижены, число В-лимфоцитов и уровень иммуноглобулинов в норме или повышены. Функция макрофагов в норме или нарушена умеренно. Уровень С и число нейтрофилов в норме
3. а) выраженная супрессия Т-системы главным образом за счет Тх, соотношение Тх/Тс увеличено в сторону Тс. Функция Т-клеток существенно нарушена. На этом фоне специфический клеточный иммунитет может быть подавлен в большей или меньшей степени
б) выраженная
депрессия специфическо-
го клеточного
иммунитета (туберкули-
новая анергия,
определяемая in
vivo
и
in
vitro).
На этом фоне изложенные вы-
ше (За)
изменения Т-системы могут
быть
выражены в большей или меньшей
степени
в) то
же, что 36, плюс носительство DR2.
Во
всех подгруппах пункта 3 состояние
В-системы
может варьировать, могут оп-
ределяться
(или нет) макрофаги-супрес-
соры.
Уровень С и число нейтрофилов
нарушаются
редко
Чаще первичный ограниченный туберкулез у детей. Ограниченные формы (инфильтративный и очаговый туберкулез легких) у взрослых. Излечение практически в 100% случаев
Чаще относительно неблагоприятное течение инфильтративного или очагового туберкулеза, диссеминиро-ванный (ограниченный) туберкулез (у детей и взрослых), кавернозный и ограниченный фиброзно-кавернозный туберкулез. Но в конечном итоге удается практически во всех случаях добиться излечения
Неблагоприятное течение впервые выявленного и хронического туберкулеза у детей и взрослых. Плохая эффективность химиотерапии и необходимость иммунокоррекции
То же
Особенно неблагоприятное течение туберкулеза и устойчивость к химиотерапии даже при иммунокоррекции. Положительный эффект лечения временный и достигается не всегда
шений иммунитета, контроля за эффективностью лечения и прогноза заболевания; 3) определения показаний для применения иммуно-корректоров и контроля за их эффектом. В частности, показано [Литвинов В. И. и др., 1976; ПахомовА. М,, 1983], что наличие нарушений Т-клеточного и специфического клеточного противотуберкулезного иммунитета повышает риск развития послеоперационных осложнений, существенно увеличивает число случаев перехода впервые выявленного инфильтративного туберкулеза в хронический фиброзно-кавернозный туберкулез. Установлено, что носительство Н1А-ОЯ2-антигена служит плохим прогностическим признаком: у таких впервые выявленных больных эффективность химиотерапии низкая, а процент перехода впервые выявленного очагового или инфильтративного процесса в фиброзно-кавернозный — высокий [Поспелов Л. Е. и др., 1987].
Иммунологические исследования в клинике при туберкулезе используются не только для выявления нарушений иммунитета и соответственно прогноза заболевания. Они, в частности, служат для определения эффективности лечения по восстановлению иммунологической реактивности (наряду с улучшением клинического статуса) [ХоменкоА. Г. и др., 1976, 1982]. Кроме того, результаты таких исследований служат основанием для назначения иммунокорриги-рующих средств. Учитывая, что в клинической картине туберкулеза доминируют нарушения Т-клеточного иммунитета, при этом заболевании чаще всего назначают Т-клеточные иммуностимуляторы, такие как диуцифон, тактивин, тимозин, тимостимулин, тималин и др. Эффективность использования этих препаратов продемонстрирована многократно в эксперименте и клинике. При применении иммунокорригирующих препаратов всегда необходимо помнить, что эти средства действуют в первую очередь на иммунитет и критерии для их назначения должны быть иммунологическими — наличие нарушений в соответствующих звеньях иммунитета.
И наконец, вероятно, не менее важная практическая проблема — иммунодиагностика туберкулеза. Эта проблема существует, во-первых, потому, что известен целый ряд заболеваний, имеющих сходную с туберкулезом клинико-рентгенологическую симптоматику, во-вторых, вакцинация BCG, а также инфицирование атипичными ми-кобактериями, а возможно, и другими микроорганизмами, имеющими перекрестные антигены с микобактериями — возбудителями туберкулеза, затрудняют изучение иммунного ответа на антигены микобактерии туберкулеза. Наиболее широко применяемая для диагностики туберкулеза туберкулиновая проба в настоящее время мало пригодна для дифференциальной диагностики в силу указанных выше причин и низкой специфичности и активности препарата, с которым ставится эта проба, — туберкулина (PPD).
Возможно несколько подходов для решения этой сложной проблемы. Например, Е. Ф. Чернушенко и соавт. (1976, 1982) проводят дифференциальную диагностику туберкулеза и других болезней легких на основании результатов изучения соотношения специфического иммунитета и неспецифической реактивности. М. М. Авербах и соавт, (1982, 1986) для этого исследуют состояние Т- и В-кле-точного иммунитета, специфического клеточного и гуморального иммунитета и дополнительных факторов иммунитета (комплемент, фагоциты). Диагностика в этих случаях основывается на совокупности полученных данных. Однако идеальным было бы создание какого-либо специфического (для туберкулеза) теста, который по возможности давал бы 100% положительных результатов у больных туберкулезом (чувствительность) и 100% отрицательных результатов у больных с другой патологией и здоровых лиц, в том числе инфицированных атипичными микобактериями и вакцинированных БЦЖ (специфичность). Решение этой проблемы затрудняется тем, что для такой диагностики нужны антитела, реагирующие с уникальными антигенными детерминантами, а также антигены, реагирующие с такими антителами либо выявляющие ГЗТ, направленную против уникальных детерминант. Необходимо также применение высокочувствительных методов, поскольку такие антигены и антитела часто имеют низкую активность. Серологические тесты в этом отношении предпочтительней, чем тесты клеточного иммунитета in vitro, так как хотя антитела не играют защитной роли при туберкулезе, но они, как правило, синтезируются и стало быть присутствуют в крови, а их специфичность определения выше, чем ГЗТ [КнорингБ. Е. и др., 1985; DhandR., 1986].
В настоящее время имеются высокочувствительные и воспроизводимые микротесты определения антител с автоматизированным и компьютерным учетом результатов (РИА, ИФА). Для получения высокоспецифических реагентов существует несколько подходов: физические и химические методы фракционирования, получение мо-ноклональных антител, выделение с помощью последних антигенов узкой специфичности, получение «генно-инженерных» белков и синтетических антигенов [Литвинов В. И. и др., 1988; Raheman S. et ah, 1988; Ridell М., 1988].
Еще одним подходом в серодиагностике может быть определение различий антительного спектра сывороток — антител к разным антигенным детерминантам с помощью метода иммуноблоттинга или радиоиммунопреципитации. Получены данные о том, что у разных больных туберкулезом определяются антитела к различным антигенным компонентам комплексного микобактериального препарата [Литвинов В. И. и др., 1989].
И наконец, в будущем, вероятно, для целей иммунодиагностики будет использовано Т-клеточное клонирование, т. е. изучение Т-клеточных клонов, реагирующих на определенные антигены микобактерии.
2.2. МЕХАНИЗМЫ ПРОТИВОТУБЕРКУЛЕЗНОГО ИММУНИТЕТА
Огромное число исследований посвящено изучению роли факторов неспецифической реактивности и специфического противотуберкулезного иммунитета, а также механизмов индукции различных феноменов иммунитета при туберкулезе и их взаимосвязи с резистентностью к туберкулезной инфекции. Полученные результаты позволяют сформулировать ряд общих положений.
Установлено, что антигенным компонентом микобактерии, индуцирующим и обнаруживающим ГЗТ, являются белки; полисахариды и лип иды таким действием не обладают. Вероятно, во всех работах, в которых сообщалось о роли в данном феномене небелковых препаратов, соответствующий эффект обусловлен присутствием примесей. Напротив, антителообразование могут стимулировать и выявлять самые различные компоненты микобактерии [Литвинов В. И. и др., 1989; Grange J., 1989].
Микобактерии обладают мощным адъювантным действием, что широко используется для усиления иммунного ответа на слабоим-мунногенные антигены. Основной адъювантный эффект микобактерии осуществляется за счет гликолипидов (мурамиллипептид, ди-миколат трегалозы) клеточной стенки [Masihi К. et al,, 1985].
Показано, что клеточный противотуберкулезный иммунитет, тестируемый как in vivo (туберкулиновые пробы), так и in vitro (как правило, реакция бласттрансформации), наиболее выражен в тех ситуациях, когда можно говорить о высокой (относительно) резистентности к инфекции: у иммунизированных людей и животных, на ранних стадиях вирулентной инфекции у животных и при тех моделях (например, у кроликов), когда инфекция протекает благоприятно. У человека наиболее высокий клеточный противотуберкулезный иммунитет также обнаруживается при благоприятном течении процесса, успешном его лечении и ограниченных формах заболевания.
Что касается уровня антител, то такой четкой закономерности обнаружить не удается, поскольку антитела к разным антигенам микобактерии имеют неодинаковую динамику при туберкулезном процессе, а часто природа антигена, использованного теми или иными авторами, неясна. Например, PPD (очищенный белковый дериват туберкулина) на самом деле в основном состоит из полисахаридов и полипептидов. Можно отметить также, что, вероятно, концентрация антипротеиновых антител наиболее высокая при относительно неблагоприятном течении туберкулезного процесса, а антиполисахаридных, наоборот, — при благоприятном.
Установлено, что нет полного параллелизма между «общим» состоянием Т-системы иммунитета и специфическим клеточным иммунитетом, как и состоянием В-клеточного иммунитета и уровнем противотуберкулезных антител, хотя в обоих случаях отмечаются сходные тенденции в изменении соответствующих показателей. В частности, данные о количестве иммуноглобулинов при туберкулезе противоречивы, хотя многие авторы отмечают тенденцию (часто статистически недостоверную) к увеличению уровня IgG и IgA и противотуберкулезных антител соответствующего класса при активном процессе. При наиболее тяжелом течении туберкулеза имеется подавление как Т-клеточного (вообще), так и специфического клеточного противотуберкулезного иммунитета. Однако выраженная депрессия Т-клеточного иммунитета определяется лишь в редких случаях; при очень тяжелых распространенных формах заболевания, в ситуации, напоминающей таковую при лепроматозной лепре.
Гуморальный и клеточный противотуберкулезный иммунитет часто находится как бы в конкурентных взаимоотношениях при туберкулезе, точнее, возникновение высокого антителообразования может ингибировать клеточный иммунитет — феномен иммунологического отклонения, возможно подобный иммунологическому усилению роста опухоли. Механизмы этого явления изучены недостаточно, однако, вероятно, данный феномен определяется действием Т-супрессоров.
Пока нет четких сведений о том, какие компоненты микобактерии индуцируют протективный эффект, направленный против этих микробов. Данные, полученные до последнего времени, не позволяют по крайней мере отвергнуть бытующее представление, что для проявления протективного эффекта нужно несколько антигенных детерминант (на белковых и полисахаридных молекулах), одна часть из которых уникальна, а другая часть является перекрестной с другими микобактериями, а возможно, и рядом других микроорганизмов. При этом, вероятно, необходимо предъявление иммуноген-ных детерминант таким образом, чтобы они были переработаны и предъявлены иммунокомпетентным клеткам (Т-лимфоцитам) макрофагами.
Для проявления протективного эффекта важны адъювантное действие микобактерии и длительное персистирование иммуногенных антигенов в организме.
Большая часть имеющихся данных свидетельствует о том, что иммунные противотуберкулезные сыворотки, как и В-лимфоциты, не оказывают прямого токсического действия на микобактерии и не усиливают бактерицидную активность макрофагов против этих микроорганизмов. Однако есть отдельные работы, в которых это положение оспаривается.
В настоящее время практически не вызывает сомнения, что центральным звеном в проявлении резистентности к микобактериям являются Т-клетки, специфически сенсибилизированные к мико-бактериальным антигенам. Они адоптивно переносят способность к протективному эффекту, такой перенос не удается с помощью взвеси лимфоцитов, обработанных анти-0- или анти-Thy-l-сывороткой (антисыворотками к антигенам Т-лимфоцитов).
Вместе с тем Т-лимфоциты непосредственно не действуют на микобактерии. Эффективным звеном противотуберкулезной резистентности служат макрофаги. Только в клетках этого типа размножаются и гибнут микобактерии туберкулеза. При этом защитные системы макрофагов, небактерицидные, обеспечивают лишь инги-бицию размножения микроорганизмов. Ранее предполагалось, что за этот эффект ответственны ферменты лизосом, которые воздействуют на микроорганизмы после слияния лизосом с фагосомой. Так, Q. Myrvik и соавт. (1984), G. Frenkel и соавт. (1986) показали, что имеются существенные различия в судьбе фагосом, содержащих вирулентные и авирулентные микобактерии, поскольку только первые препятствуют их слиянию с лизосомами. Получены данные, свидетельствующие о том, что на микобактерии действуют перекиси. Так, показано повышенное высвобождение перекиси водорода альвеолярными и перитонеальными макрофагами у иммунных животных (морские свинки, мыши) в ответ на стимуляцию соответствующим видом микобактерии. Отмечено также резкое снижение содержания чувствительных к перекиси изониазидрезистентных микобактерии туберкулеза (мутантный штамм H37RV) в легких иммунных животных. Однако в экспериментах, проведенных на мышах, не удалось обнаружить зависимости между клиренсом микобактерии макрофагами и непосредственным токсическим действием перекисей на бактерии. Эти данные свидетельствуют о том, что перекиси также не являются универсальным механизмом воздействия макрофагов на микобактерии и, вероятно, этот эффект обусловлен комплексом различных факторов.
Вместе с тем следует подчеркнуть, что взаимодействие макрофагов с микроорганизмами, в том числе с микобактериями, неспецифическое и требует иммунологического усиления. Таким усиливающим фактором для макрофагов, содержащих микобактерии, являются сенсибилизированные Т-лимфоциты, которые непосредственно, а скорее с помощью медиаторов (лимфокинов), стимулируют миграцию макрофагов в очаги воспаления (с помощью, в частности, факторов хемотаксиса), а также повышают фагоцитарную активность и ингибицию микобактерии внутри макрофагов. При этом действие сенсибилизированных Т-лимфоцитов на макрофаги в конечном итоге также оказывается неспецифическим. Т-клетки, иммунные к микобактериям, адоптивно переносят усиление протективного эффекта против разных внутриклеточно паразитирующих микроорганизмов. Такие данные получены в исследованиях, выполненных как in vivo, так и in vitro. Например, Т-клетки, иммунные к микобактериям туберкулеза, приобретают способность защищать мышей от инфицирования и нетуберкулезными микобактериями, что I. Orme и F. Collins (1986) связывают с наличием перекрестных антигенов. Однако, вероятно, более важным является неспецифическое усиление активности макрофагов.
Как отмечалось выше, противотуберкулезные антитела как непосредственно, так и при пассивном переносе, как правило, непосредственно не ингибируют размножение микобактерии и не повышают бактериостатическую активность макрофагов (хотя имеется небольшое число данных, оспаривающих это положение). Более того, синтез антипротеиновых антител, которые выступают в качестве конкурирующих факторов с клеточным иммунитетом (феномен отклонения), отрицательно сказывается на течении туберкулезной инфекции. Такая ситуация была воспроизведена в экспериментальных условиях и наблюдалась (редко) в клинической картине туберкулеза.
Элиминация Т-клеток (например, тимэктомией, облучением), а также через длительные сроки после тимэктомии или при выраженной иммунодепрессии (у животных и людей) отрицательно влияет на течение туберкулезной инфекции. Аналогично сопротивляемость к туберкулезу снижена у мышей с врожденным дефектом Т-клеток (линии nu/nu, NZB) [Авербах М. М. и др., 1980, 1984; Lefford J. etal., 1982], что подтверждает роль Т-лимфоцитов в защите от этого заболевания. Подобным же образом индукция толерантности (иммунологической ареактивности) в тех случаях, когда она затрагивает специфический Т-клеточный иммунитет и независимо от того, страдает или нет гуморальный иммунитет, также является крайне неблагоприятным фактором для взаимодействия микобактерии туберкулеза и макроорганизма [Марков А. Н., 1980].
В тех случаях, когда имеются нарушения Т-клеточного иммунитета, введение иммунокорригирующих средств (Т-активин, лева-мизол, тимозин, диуцифон и др.), действующих преимущественно на Т-клеточный иммунитет, восстанавливает нормальное функционирование Т-системы и вместе с тем оказывает положительное действие на течение туберкулезной инфекции [Хоменко И. С. и др., 1986].
Учитывая роль Т-клеточного иммунитета в сопротивляемости к туберкулезной инфекции, необходимо понять, почему развивающийся Т-клеточный иммунитет оказывается не всегда эффективным несмотря на то, что общее число Т-лимфоцитов очень редко существенно уменьшается при этой патологии. В настоящее время имеются данные, позволяющие в определенной мере вскрывать причины этого явления. В частности, показано, что при тяжелом течении туберкулеза у людей уменьшается число лимфоцитов, несущих маркеры Т-хелперов (ОКТ-4 и Т/*), и изменяется соотношение Тх/Тс в сторону последних. Используя моноклональные антитела к поверхностным маркерам Т-лимфоцитов, J. Rook и соавт. (1985) установили, что у больных активным легочным туберкулезом в IV2 раза снижено число Т- и Т4-лимфоцитов, а число В- и Т8-клеток (супрессоров) не отличается у больных и здоровых лиц. Выраженность Т4-лимфоцитопении не зависела от тяжести туберкулезного процесса и интенсивности туберкулиновых проб. Авторы считают, что Т-лимфоцитопения — это не проявление приобретенного иммунодефицита, а результат иммунодепрессии. Действительно, при туберкулезе (однако, вероятно, только при его наиболее тяжелых формах) может развиваться иммунодепрессия, в первую очередь вследствие интоксикации. М. М. Авербах и соавт. (1986), В. В. Еремеев и соавт. (1986) установили, что уменьшение числа Т-хелперов и соотношения Тх/Тс в сторону последних более существенно при прогрессирующем течении туберкулеза, а также при распространенных деструктивных формах заболевания.
Количественные изменения субпопуляций Т-лимфоцитов могут определяться не только в периферической крови, но и в других органах и тканях. Так, у больных туберкулезным плевритом в плевральной полости увеличивается общее число Т-лимфоцитов, число ОКТ-4~лимфоцитов (хелперов), а также соотношение ОКТ-4/ОКТ-8 по сравнению с таковым в периферической крови. При стимуляции PPD in vitro соотношение Т4/Т8 возрастает в культурах лимфоцитов плевральной полости в большей степени, чем в периферической крови. Показано, что на PPD реагировали Т4-(но не Т8)-лимфоциты. После стимуляции PPD увеличивалось также число DR-положительных лимфоцитов [Shiratsuhi Н., Tsuynguchi Т., 1984]. Это очень важно, так как для взаимодействия лимфоцитов с макрофагами, поглотившими микобактерии, необходима экспрессия таких антигенов.
Особенно актуальным является изучение механизмов супресии иммунного ответа при туберкулезе. И у людей, и у экспериментальных животных ареактивность (или гипореактивность) к мико-бактериальным антигенам ассоциируется, по-видимому, с активностью клеток-супрессоров. При этом обнаружены 2 типа супрессоров: Т-клетки — Tj+OKT8+ (у человека), Lytl+2+ (у мышей) и макро-фаги-супрессоры. Механизмы супрессии хорошо изучены при системном (внутривенном) введении вакцинного штамма мышам. Показано, что в разных ситуациях могут стимулироваться антиген-специфические и антигеннеспецифические механизмы супрессии, опосредованные соответствующими супрессорными медиаторами, которые влияют на синтез и рецепцию интерлейкинов (ИЛ) [Campa М. et al, 1984; ColizziV. et al, 1985].
Одним из посредников активации лимфоцитов в реакции на митогены (как специфической, так и неспецифической) является ИЛ-2. В этом плане представляют интерес исследования Z. Toossi и соавт. (1986). Показано, что лимфоциты больных туберкулезом («свежевыявленным») в ответ на стимуляцию PPD вырабатывали ИЛ-2 на 81,2% меньше, чем лимфоциты здоровых туберкулинпо-ложительных доноров. У этих больных в 3 раза была снижена пролиферативная реакция на PPD в культурах лимфоцитов. Вместе с тем в таких культурах не содержались супрессивные факторы. Однако макрофаги были частично или полностью (у разных больных) ответственны за снижение синтеза ИЛ-2 и бластогенеза в культурах с PPD (макрофаги больных, в частности, подавляли синтез ИЛ-2 в культурах лимфоцитов здоровых людей). Экзогенный ИЛ-2 усиливает пролиферацию лимфоцитов как в присутствии PPD, так и без него. С помощью моноклональных антител было обнаружено снижение числа рецепторов для ИЛ-2 на лимфоцитах периферической крови больных. Следовательно, в данном случае супрессорный эффект был обусловлен как действием макрофагов-супрессоров, так и снижением реакции лимфоцитов на ИЛ-2. Все эти данные в целом свидетельствуют о том, что супрессия иммунного ответа при туберкулезе является сложным процессом, в котором участвуют макрофаги и Т-лимфоциты (вероятно, и В-лимфоциты, и иммунные комплексы), действующие в разных ситуациях на различные этапы иммуногенеза.
Интенсивно исследовалась роль в защите от туберкулеза «местных» факторов бронхиального эпителия, альвеол, так называемого сурфактанта. Имеются сведения (противоречивые) об определенном значении альвеолярных макрофагов и секреторного IgA, в одних работах отмечается дефект этих систем у больных туберкулезом, в других, наоборот, мобилизация данных защитных факторов в брон-хоальвеолярном содержимом. То же самое относится и к соотношению в бронхоальвеолярном содержимом Т- и В-лимфоцитов, субпопуляций Т-лимфоцитов, к содержанию и роли опсонизирующих факторов (компонентов комплемента, IgG). Получены новые данные, в частности, о значении местных факторов супрессии противотуберкулезного иммунитета [Мороз А. М и др., 1990]. Учитывая, что заражение туберкулезом в естественных условиях происходит, как правило, аэрогенным путем, изучение тех защитных факторов (особенно выявление их дефекта), которые первыми контактируют с ннфектом, представляется весьма важным. В этом плане наши знания пока менее совершенны, чем соответствующие представления о роли «местного» иммунитета, например, при кишечных инфекциях. Однако надо учитывать, что все защитные элементы, обнаруживаемые в бронхоальвеолярном содержимом, попадают туда из циркуляции (Т- и В-лимфоциты, и макрофаги, и иммуноглобулины, и компоненты комплемента). Кроме того, их количественная оценка затруднена, особенно у человека.
Считалось, что при туберкулезе существенную роль играет замедленная аллергия (ГЗТ), которую оценивали по кожным туберкулиновым пробам. Однако было показано, что кожная ГЗТ является одним из феноменов Т-клеточного иммунитета. Ранее предполагалось, что ГЗТ лежит в основе образования казеоза в туберкулезных очагах (другие исследователи считали, что немедленная гиперчувствительность). Однако более вероятно, что казеоз образуется в результате воздействия ферментов макрофагов, скапливающихся в очагах туберкулезных поражений. Многие авторы пытались разделить ГЗТ (оцениваемую по кожным пробам) и иммунитет (так называли повышение резистентности к туберкулезу). Такие попытки, осуществляемые с помощью десенсибилизации туберкулином или путем поиска фракций микобактерии, индуцировавших один из этих феноменов (без другого), чаще оказывались безуспешными.
Следует отметить, что пока не найден субстрат ГЗТ, который вызывал бы (подобно тому, как это происходит при немедленной аллергии) неспецифическое повреждение клеток в результате специфического взаимодействия антител с антигенами (или иммуно-компетентными клетками), и поэтому «место» замедленной аллергии (если такая существует) при туберкулезе не определено.
Что касается немедленной аллергии, обусловленной антителами-реагинами (IgE) и иммунными комплексами, то показано, что такие реакции при туберкулезной инфекции развиваются. Так, по данным Е. Gatner и соавт. (1983), содержание IgE-антител в сыворотках крови больных туберкулезом в 17а/г раза выше, чем у здоровых доноров, однако эти антитела находятся в связанном (в иммунных комплексах) состоянии. В циркулирующих иммунных комплексах у больных туберкулезом содержатся иммуноглобулины (чаще IgG и IgA), компоненты комплемента (Clg, СЗ и С4) и антигены микобактерии. Не исключено, что в иммунных комплексах при туберкулезе могут быть обнаружены и другие антигены (тканевые, антигены других микроорганизмов у вторично инфицированных больных). Однако о том, какую роль в патогенезе туберкулеза играют эти медиаторы немедленной аллергии, пока неизвестно.
Многие годы дискутируется вопрос о том, развиваются ли при туберкулезе аутоиммунные реакции и если развиваются, то как это влияет на течение туберкулезной инфекции. Разумеется, коль скоро при данной инфекции происходит деструкция тканей и изменяется химическая структура тканевых компонентов, могут открываться детерминанты, с которыми иммунекомпетентные клетки организма в нормальных условиях не имеют контакта, то какая-то реакция иммунной системы на собственные (вероятно, измененные) ткани развивается. Учитывая сложный характер нарушений иммунитета при туберкулезе, адъювантное действие микобактерии, а также то, что толерантность «к своему» в значительной мере имеет активный характер, а не связана с элиминацией всех возможных реагирующих на «свое» клонов, вопрос о возникновении и роли аутоиммунных реакций при туберкулезе требует пересмотра.
В определении роли аутоиммунитета при туберкулезной инфекции важны данные, полученные в последнее десятилетие. Так, С. Thorns и J. Morris (1985) показали, что некоторые моноклональ-ные антитела (см. ниже) к антигенам микобактерии реагировали и с тканевыми антигенами. Подобным же образом ИЛ-2 продуцирующие Т-клеточные клоны (см. ниже), полученные слиянием клеток лимфатических узлов мышей линии С57В1/6 и мышиной миеломы, реагировали как на микобактериальные, так и тканевые (свои) антигены [Miller L, 1986].
2.3. РОЛЬ НАСЛЕДСТВЕННОСТИ
Имеется много фактов, свидетельствующих о роли наследственности при туберкулезе у человека. Главные из них следующие. 1. Частота заболевания (конкордантность) туберкулеза у монозиготных (однояйцевых) близнецов выше, чем у дизиготных. 2. Значительно большая частота заболевания туберкулезом среди родственников больного — пробанда (больного туберкулезом, с которого начинается такой анализ), даже в тех случаях, когда родственники не находятся в семейном контакте. 3. «Накопление» числа случаев заболевания туберкулезом в семьях с близкородственными браками.
В последнее десятилетие появились данные о роли восприимчивости к туберкулезу конкретных генетических систем. При этом, естественно, в первую очередь обращалось внимание на главный комплекс гистосовместимости человека — HLA-систему, в которой (в ее DR-локусе) локализуются гены иммунного ответа. Так, показано, что имеются выраженные и статистически достоверные ассоциации ряда антигенов HLA В-локуса с туберкулезом: В8 — у канадцев, В15 — у американских негров, В35 — у китайцев, В5 — у египтян.
В исследованиях А. Г. Хоменко и соавт. (1981, 1985), В. И. Литвинова и соавт. (1982, 1985), Л. Е. Поспелова и соавт. (1982, 1985) установили, что в различных этнических группах заболевание туберкулезом ассоциируется с разными HLA-специфичностями: у туркменов и узбеков — В12, у армян — В5, у русских — В5, В14 и В17, у молдаван — В5 и В38. Вместе с тем этот же коллектив авторов [Поспелов Л. Е. и др., 1986; Литвинов В. И. и др., 1986] показал, что во всех обследованных популяциях (среди населения бывшего Советского Союза) заболевание туберкулезом ассоциируется с одним и тем же антигеном системы HLA DR-локуса — DR2.
С этим же антигеном заболевание ассоциируется у индусов, больных туберкулезом [Singh S. et al., 1983]. Прямые указания на роль генов HLA в патогенезе туберкулезной инфекции дали результаты семейного анализа наследования двух признаков — HLA-специфичностей и заболеваний туберкулезом: с помощью ряда моделей сцепление этих двух признаков в семьях было установлено бесспорно [Поспелов Л. Е. и др., 1986].
Кроме того, показано, что Н1А-(в первую очередь DR)-фенотип отличается у больных разными формами туберкулеза (ограниченными, благоприятно протекающими, с одной стороны, и распространенными, хроническими, с другой). Это указывает на роль генов HLA в качестве факторов, влияющих на течение и форму туберкулеза у человека. Естественно возникает вопрос, через какие иммунологические (или неиммунологические) гены HLA-комплекса воздействуют на восприимчивость к туберкулезу и его течение.
Число исследований, посвященных изучению связи генетических маркеров при туберкулезе с иммунологическими параметрами, пока невелико.
В. И. Литвинов и соавт. (1986) показали, что у больных туберкулезом — носителей ОЯ2-антигена статистически достоверно повышен уровень противотуберкулезных IgG-антител (по данным ИФА) и снижена реакция in vitro лимфоцитов на микобактериальный белковый антиген. Исходя из этих результатов, можно предположить, что гены иммунного ответа (Iг-гены, предположительно находящиеся в DR-локусе) влияют на чувствительность к туберкулезу, регулируя силу иммунного ответа на микобактериальные антигены. Показано также, что неспособность к развитию клеточного противотуберкулезного иммунитета, в частности возникновение туберкулиновой анергии после ревакцинации БЦЖ, контролируется генами HLA (DR-локуса) [Поспелов Л. Е. и др., 1986].
Особенно четкие данные (наряду с результатами близнецовых исследований) о роли наследственных механизмов при туберкулезе получены в исследованиях на линейных мышах. При изучении чувствительности мышей к туберкулезной инфекции (как и к другим внутриклеточным инфекциям) используют, как правило, два основных критерия: 1) продолжительность жизни после заражения и 2) количество высеянных из органов (селезенка, легкие, печень) микобактерии, т. е. численность микобактериальной популяции, что отражает размножение микробов или его ингибицию.
Получены данные, свидетельствующие о том, что разные линии мышей неодинаково чувствительны к туберкулезной инфекции. Наиболее детально этот процесс изучали М. М. Авербах и соавт. (1980, 1985). Заражая разными дозами вирулентных микобактерии (Н37 Rv) мышей более 30 линий, авторы установили, что большинство линий мало различались по продолжительности жизни после заражения (в среднем 30—40 дней), однако между двумя линиями (чувствительной I/St и резистентной A2g), которые названы оппозитными, были существенные различия (соответственно 19 и 53 дня).
Динамический анализ высеваемости микобактерии из селезенки и легких, морфологическая характеристика легочных изменений, а также оценка специфической иммунологической реактивности позволили цитируемым авторам установить принципиальные отличия большинства показателей у разных линий мышей, причем наибольшие различия касались бактериальной высеваемости и активности Т-клеток. Были также выявлены межлинейные различия в сопротивляемости к туберкулезу предварительно вакцинированных животных. Показано, что при введении стандартной дозы БЦЖ межлинейные различия были те же, что и при первичном заражении, но у высокочувствительных животных протективный эффект почти отсутствовал, в то время как резистентные мыши после вакцинации жили значительно дольше, чем после первичного заражения.
На гибридах первого поколения между оппозитными линиями и потомках возвратного скрещивания с родительскими линиями проанализированы особенности наследования восприимчивости к туберкулезу. Установлено, что доминантным признаком является резистентность к инфекции, а восприимчивость находится под полигенным контролем гена чувствительности и генов резистентности, причем ген чувствительности к туберкулезу не сцеплен с комплексом Н2 (главный комплекс гистосовместимости мышей) [Авербах М. М. и др., 1985]. Также показано, что ранняя фаза инфекции у мышей при заражении микобактериями туберкулеза штамма BCG находится под контролем одного гена (BCG), расположенного на хромосоме 1 и имеющего два аллеля — чувствительный и резистентный. Проявление этого гена осуществляется главным образом через систему макрофагов [Scamene Е. et al., 1980].
Изучены некоторые механизмы генетического контроля специфического противотуберкулезного иммунитета и межклеточного взаимодействия иммунокомпетентных клеток. Показано, что введение сыворотки против генетического маркера Т-супрессоров I-J приводит к увеличению срока жизни мышей и активации показателей специфического иммунного ответа [Апт А, С и др., 1988].
2.4. НОВЫЕ НАПРАВЛЕНИЯ И ПЕРСПЕКТИВЫ ИССЛЕДОВАНИЙ
В последние десятилетия возник ряд новых подходов к изучению механизмов противотуберкулезного иммунитета. Эти подходы (точнее, полученные с их помощью вещества) могут использоваться и частично уже используются в практической фтизиатрии. Это гибридом-ная технология, генная инженерия и Т-клеточное клонирование. Так, с помощью гибридомной технологии получен большой набор моноклинальных антител к разным антигенам микобактерии. Они синтезированы одним клоном В-лимфоцитов и направлены соответственно к одной антигенной детерминанте. Эти антитела с большим или меньшим успехом пытаются применить для решения следующих задач.
1. Оценка
влияния in
vivo
и in
vitro
антител к разным компонентам
микобактерии
на течение туберкулезной инфекции.
Такие иссле-
дования пока не дали
реальных результатов.
2. Изучение
антигенной структуры микобактерии, в
частности
антигенных различий разных
видов микобактерии. Получены
мо-ноклональные антитела, реагирующие
как с уникальными (точнее, представленные
с большей плотностью), так и с перекрестно
реагирующими антигенами [Engers
A.
et
al.,
1986; Ljungavist
L.
et
al.,
19881.
-
Обнаружение микобактерии (например, в мокроте) и их видовая идентификация [Андросова М. В. и др., 1989].
-
Выявление антигенов микобактерии (например, в спинномозговой жидкости или в сыворотке крови в составе иммунных комплексов) [Литвинов В. И. и др., 1990].
-
Выделение отдельных антигенов из сложной антигенной смеси. Характеристика генно-инженерных белков (см. ниже) и антигенов, выделенных иммунохимическими методами [IvanyiJ. et al., 1985].
-
Обнаружение антител конкурентными методами [Ivanyi J. et al., 1989].
Т-клеточное клонирование (получение «потомков» одного Т-лим-фоцита) используется для изучения: 1) спектра Т-клеток (хелперов или супрессоров), реагирующих на разные антигенные детерминанты при туберкулезе и вакцинации БЦЖ (такая работа только начинается); 2) роли Т-клеточных субпопуляций и клонов, реагирующих на определенные детерминанты, в протективном иммунитете и им-муносупрессии (в частности, получен ряд Т-клеточных клонов, индуцированных антигенами микобактерии, которые продуцируют суп-рессорные или хелперные медиаторы) [Miller I., KanfmamrS., 1986; Lam J. et al., 1989]; 3) использования Т-клонов для поиска протек-тивных антигенов в целях конструирования будущей противотуберкулезной вакцины.
Уже получена серия генно-инженерных белков, как общих, так и специфических для различных видов микобактерии. Эти белки используются или будут использоваться для стимуляции Т-клеточных клонов [Thole J. et al., 1988], серодиагностики (пока такие работы не опубликованы) и, вероятно, перспективными будут ре-комбинантные белки при конструировании химической вакцины. Главные направления в исследованиях фундаментальных механизмов противотуберкулезного иммунитета и их генетического контроля связаны, вероятно, с определением локализации генов, ответственных за чувствительность и/или резистентность к туберкулезу и механизмов их действия, а также с изучением взаимного влияния процессов (опосредованных иммунологическими факторами) в органах иммунитета, циркуляции и в местах туберкулезных поражений.
ГЛАВА 3
ЭПИДЕМИОЛОГИЯ
Эпидемиология туберкулеза, являясь разделом, составной частью фтизиатрии, изучает источники заражения туберкулезом, пути передачи инфекции, распространенность туберкулеза как инфекционного заболевания среди населения и наиболее угрожаемые группы населения, среди которых имеется наибольший риск заболевания туберкулезом. Необходимо учитывать, что туберкулез является не только медико-биологической проблемой, связанной с взаимодействием организма человека и возбудителя, но и проблемой социальной, поскольку социальные факторы влияют на состояние здоровья населения в целом и отдельных его групп. В частности, большое значение имеют материальный уровень жизни, санитарная грамотность и культура, род занятий, жилищные условия, обеспеченность медицинской помощью и др. Демографические особенности также должны быть приняты во внимание при изучении туберкулеза с эпидемиологических позиций: возрастной состав населения, в том числе удельный вес детей, распределение по полу, рождаемость, плотность населения и т. д.
Основным источником заражения окружающих является больной туберкулезом, выделяющий микобактерии туберкулеза. Как правило, это больные туберкулезом легких. Наибольшую опасность представляют больные с обильным, постоянным бактериовыделением, которое выявляется с помощью микроскопии. Однако и при скудном бактериовыделении, обнаруживаемом только при посеве на питательные среды, больные также могут заражать окружающих, особенно при тесном контакте.
Больные в нелегочным и формами туберкулеза, выделяющие микобактерии туберкулеза (туберкулез почек и мочевыводящих путей, свищевые формы туберкулеза костей и суставов, периферических лимфатических узлов и других органов), считаются также опасными для окружающих из-за риска заражения последних.
Заражение туберкулезом может быть при наличии прямого контакта с больным, который рассеивает микобактерии при кашле, чиханье, с капельками слюны при разговоре, поцелуях и т. д. С давних пор основным путем заражения считался воздушно-капельный. Однако заражение возможно и без прямого контакта с больным — при соприкосновении с зараженными предметами, бельем, с пылевыми частицами, содержащими засохшую мокроту, другим материалом, содержащим микобактерии (воздушно-пылевой путь заражения). Естественно, что опасность воздушно-пылевого заражения возрастает при невыполнении больным правил личной гигиены, недостаточной дезинфекции или ее отсутствии, при некачественной уборке помещения. В связи с тем что микобактерии туберкулеза обладают высокой устойчивостью к воздействию внешних факторов, они длительное время (месяцы и годы) сохраняют жизнеспособность и патогенность в темноте в почве и сточных водах, при низкой температуре и обработке многими дезинфицирующими средствами, — воздушно-пылевой путь заражения заслуживает особого внимания.
Заражение туберкулезом возможно также алиментарным путем при пользовании общей посудой.
Вторым по значимости источником заражения является крупный рогатый скот, больной туберкулезом. При этом наибольшая опасность создается для животноводов и других работников, контактирующих с животными. В этом случае заражение также чаще происходит воздушно-капельным или воздушно-пылевым путем. Возможен и алиментарный путь заражения — при потреблении некипяченого или непастеризованного молока, или приготовленных из него продуктов. Следовательно, алиментарный путь заражения может иметь место и при отсутствии прямого контакта с больными животными.
Остальные источники заражения туберкулезом имеют меньшее эпидемиологическое значение, так как встречаются реже. Такими источниками могут быть куры (Р. В. Тузова), различные животные (свиньи, овцы, верблюды и др.), в том числе и домашние (кошки, собаки) (Я. А. Благодарный).
От больного туберкулезом человека заражение происходит обычно человеческим видом микобактерии туберкулеза. Для человека эпидемиологически опасным является не только этот вид микобактерии, но и бычий вид (Я. А. Благодарный, В. Devulder). Особенностью заболевания туберкулезом, вызванном бычьим видом микобактерии, является частое поражение мочеполовых органов и периферических лимфатических узлов (К. К. Курманбаев), лекарственная резистентность к изониазиду, что затрудняет химиотерапию. Легочный туберкулез иногда приобретает прогрессирующее течение, особенно в условиях позднего выявления заболевания.
Заражение человека может иногда вызываться птичьим видом микобактерии, которые обычно обладают полирезистентностью к химиопрепаратам. В случае возникновения заболевания (что отмечается весьма редко) оно, как правило, принимает прогрессирующий характер с образованием множественных деструкции в легких. У отдельных лиц отмечается заражение различными атипичными микобактериями. Вызванное ими заболевание в настоящее время принято называть микобактериозом. По клинико-рентгенологическим проявлениям и морфологическим реакциям оно не отличается от туберкулеза. Описаны случаи заболевания, вызванные М. Kansasii, М. Scrofulaceum, М. Xenopei, М. Fortuitum и др. (Н, М. Макаревич, J. Weiszfeller и др.). Пути заражения атипичными микобактериями не описаны, хотя резервуар инфекции уже известен — почва, водоемы. Многие животные, в том числе крупный рогатый скот, могут быть заражены атипичными микобактериями, которые длительное время сохраняются в их организме. Заболевания микобактериозом носят спорадический характер, случаи передачи инфекции от человека к человеку не описаны.
Как известно, инфекционный процесс является результатом взаимодействия возбудителя (микобактерии туберкулеза) и организма, поэтому в эпидемиологических исследованиях важное место занимает изучение восприимчивости человека в туберкулезной инфекции. Наиболее опасно заражение туберкулезом в детском возрасте, особенно в раннем детском возрасте (до года и в 1—5 лет). В этот период естественная резистентность еще несовершенна и не совершенствуется из-за недостаточного развития иммунологических механизмов. Определенную роль играет наследственная предрасположенность или, наоборот, резистентность к туберкулезу. С возрастом эти механизмы совершенствуются, приобретают значение другие факторы, которые отрицательно влияют на восприимчивость: недостаточное питание, сопутствующие заболевания, тяжелая работа, приводящая к систематическому переутомлению, нервно-психические срывы (стрессовые состояния) и т. д.
Очень большое влияние на течение инфекционного процесса оказывает наличие или отсутствие приобретенного иммунитета у заразившихся туберкулезом людей. Как ни важны индивидуальные особенности каждого человека, эпидемиология туберкулеза изучает общие закономерности, определяющие распространение туберкулеза среди населения или его отдельных групп. Этим эпидемиологический подход к проблеме туберкулеза отличается от клинического, который изучает индивидуум. С данных позиций очень важно среди населения выделить группы с наибольшей восприимчивостью к туберкулезу. Такие группы принято называть группами населения с повышенным риском развития туберкулеза.
Принимая во внимание патогенез туберкулеза, повышенный риск развития первичных форм туберкулеза имеют неинфицированные лица, дети, подростки и взрослые до 30 лет, так как с увеличением возраста среди населения возрастает число инфицированных туберкулезом лиц: к 40 годам число таких случаев достигает 70—90%. Число инфицированных людей также рассматривается как эпидемиологический показатель — инфицированность, которая выражается в процентах, т. е. на 100 жителей. Часто инфицированность определяют применительно к различным возрастным группам. В странах, в которых проводятся противотуберкулезная иммунизация новорожденных, ревакцинация детей и подростков, определение показателя инфицированное™ населения сталкивается с большими трудностями из-за появления положительной туберкулиновой пробы после вакцинации и ревакцинации. Тем не менее разработана методика расчетов, позволяющая установить «риск заражения» и взаимосвязь между этим показателем и численностью больных заразными формами туберкулеза.
Вторичный туберкулез развивается у инфицированных лиц в любом возрасте, но чаще у мужчин в возрасте 49—50 лет. При эпидемиологических исследованиях нет возможности дифференцировать первичные и вторичные формы туберкулеза (в клинических условиях также далеко не всегда имеются данные, позволяющие различать эти формы), поэтому случаи заболевания, несмотря на их разный патогенез, регистрируются суммарно. Случаем заболевания туберкулезом считается развитие любой клинической формы при наличии клинико-лабораторных данных, свидетельствующих об активности заболевания.
Такой подход к определению случая заболевания туберкулезом признается далеко не во всех странах, хотя близкие к этому определению подходы существуют в Германии, Болгарии, Дании, США, Франции и ряде других экономически развитых стран. Для развивающихся стран Комитет экспертов ВОЗ и Международный противотуберкулезный союз рекомендовали другой подход: случаем заболевания туберкулезом считается заболевание, при котором микобактерии выделяются с помощью микроскопии (7—9-й доклад Комитета экспертов по туберкулезу ВОЗ), Всех остальных больных не рекомендовалось регистрировать, и для таких случаев было предложено определение «подозрение на туберкулез». Естественно, при таком определении учитывается примерно 30—50% заболевших туберкулезом. Ошибочность данного подхода была зафиксирована на Международной конференции по туберкулезу в 1982 г. (Аргентина), особенно применительно к больным детского возраста с наличием милиарного туберкулеза, менингита, туберкулеза внутригрудных и периферических лимфатических узлов, плеврита и полисерозита.
В настоящее время среди заболевших туберкулезом определяется численность больных с заразными формами.
Проведенные эпидемиологические исследования позволили рассчитать для целого ряда территорий и стран ежегодный риск заражения туберкулезом.
Анализ числа заболевших туберкулезом в различных группах населения еще в 1966 г. позволил Horwitz установить, что наибольший риск заболевания туберкулезом в экономически развитых странах, в которых в послевоенный период отмечается постепенное уменьшение распространенности туберкулеза, имеют инфицированные лица, а наименьший — неинфицированные, по иммунизированные вакциной БЦЖ. Оказалось также, что наибольший риск среди инфицированных имеется у лиц с наличием остаточных изменений излеченного туберкулеза (см. ниже), а также при наличии сопутствующих заболеваний (см. ниже).
О распространенности туберкулеза в стране или на какой-либо территории принято судить по эпидемиологическим показателям. Наибольшее значение имеет показатель заболеваемости туберкулезом, который определяется по числу впервые зарегистрированных больных в течение текущего года на каждые 100 ООО или 10 000 населения. Более детальное представление о структуре заболеваемости могут дать показатели заболеваемости туберкулезом органов дыхания и внелегочных форм, заболеваемось бациллярными формами туберкулеза органов дыхания. В свою очередь последний показатель может быть еще более детализирован: бактериовыделение обнаружено методом микроскопии, а кроме того, при посеве материала на питательных средах. Часто выделяется заболеваемость деструктивными формами легочного туберкулеза и фиброзно-кавер-нозным туберкулезом. Совокупность перечисленных показателей, а также удельный вес различных проявлений туберкулеза среди всех впервые зарегистрированных больных позволяют получить довольно детальное представление о заболеваемости туберкулезом. Например, высокий показатель заболеваемости фиброзно-кавернозным туберкулезом или его высокий удельный вес среди заболеваемости органов дыхания свидетельствует о большом резервуаре инфекции среди населения, плохо поставленной работе по раннему выявлению больных, а также о большом рассеивании туберкулезной инфекции среди окружающего населения.
Показатель заболеваемости может быть также рассчитан среди различных возрастных групп у мужчин и женщин. При этом очень важное эпидемиологическое значение имеет показатель заболеваемости туберкулезным менингитом среди детей, не менее важное значение имеет показатель заболеваемости детей от 0 до 1 года, особенно при высоком удельном весе детей среди всего населения. Последние два показателя свидетельствуют о наличии большого риска первичного заражения из-за наличия источников распространения и условий, способствующих рассеиванию инфекции, о восприимчивости коллектива и плохо поставленной работе по выявлению и профилактике туберкулеза.
Показатели заболеваемости туберкулезом должны анализироваться в совокупности с применением методики организации выявления больных. Это позволяет судить о степени осведомленности лечебно-профилактических учреждений и противотуберкулезных диспансеров о распространенности туберкулеза среди населения.
В большинстве стран Западной Европы, США, а также во всех развивающихся странах Азии, Африки и Латинской Америки выявление больных туберкулезом организовано среди лиц, обратившихся за медицинской помощью по поводу кашля с выделением мокроты и проявлением других грудных симптомов. Такой принцип, как правило, приводит к низкой степени осведомленности органов здравоохранения о распространенности туберкулеза, особенно при недостаточных санитарной грамотности населения и доступности медицинской помощи. Гораздо выше осведомленность при осуществлении массовых осмотров с максимально возможным охватом (90— 95%) населения. Поэтому в странах, в которых выяление больных туберкулезом основано на обращаемости за помощью лиц с грудными симптомами, периодически проводят осмотры населения на выбранных территориях. Это позволяет получить данные, которые можно будет распространить на всю территорию страны, региона и т. д. и рассчитать число имеющихся больных туберкулезом на соответствующее население.
Чем больше разница между данными о заболеваемости туберкулезом по материалам ежегодной регистрации и полученными при проведении массового осмотра населения, тем меньше осведомленность о распространении болезни.
Методика осмотров варьирует в зависимости от имеющихся возможностей. В развивающихся странах, как правило, это подворные обходы населения, выявление лиц с наличием кашля и выделений мокроты, сбор мокроты и ее микроскопическое исследование или посев на питательные среды. Естественно, что при такой методике выявляются лишь бактерионосители. В экономически развитых странах применяют рентгенографическое исследование с последующим дообследованием лиц с изменениями в легких. Такие исследования проводятся или на отдельных территориях, или на территории всей страны (при этом последовательно проводят осмотры по графику), или среди отдельных групп населения с повышенным риском заболевания туберкулезом.
В нашей стране для выявления больных туберкулезом используются оба принципа: по обращаемости за медицинской помощью и при проведении профилактических осмотров населения с применением флюорографии 1 раз в 3 года. Такая методика позволяет противотуберкулезным диспансерам иметь высокую осведомленность о заболеваемости туберкулезом среди населения.
Вторыми важными эпидемиологическими показателями являются болезненность и численность контингентов больных активным туберкулезом легких. Этот показатель также вычисляется на 100 ООО или 10 000 населения на конец каждого года. Состоит он из числа впервые выявленных больных в данном году, а также всех ранее зарегистрированных за предыдущие годы больных с соханяющейся активностью туберкулезного процесса. Таким образом, число больных активным туберкулезом ежегодно пополняется за счет впервые выявленных больных и в то же время ежегодно уменьшается за счет умерших и излеченных от туберкулеза (заживление локальных очагов туберкулезного характера и потеря активности процесса).
Контингенты больных туберкулезом по составу неоднородны. Наиболее опасны для окружающих больные с постоянным или периодическим бактериовыделением. Поэтому дом, квартира или другое жилое помещение, в котором постоянно живет такой больной, расценивается как очаг туберкулезной инфекции. При большом числе очагов создается эпидемиологическая опасность не только для членов семьи (бытовой контакт), но и для всего окружающего населения, особенно для детей и подростков. В очагах туберкулезной инфекции проводятся санитарно-профилактические мероприятия, а все лица, контактирующие с больным-бактерионосителем, относятся к группе повышенного риска развития туберкулеза и подлежат диспансерному наблюдению в противотуберкулезных диспансерах.
Остальные больные активным туберкулезом без выделения микобактерии должны оцениваться как потенциально опасные в эпидемиологическом отношении, так как у них в случае ухудшения в течении заболевания может появиться бактериовыделение, что создает опасность рассеивания туберкулезной инфекции.
Смертность — число умерших от туберкулеза в течение года на каждые 100 000 или 10 000 населения. Показатель смертности также весьма высок, хотя были высказывания о том, что его значение в современных условиях снижается. Однако с такой точкой зрения нельзя согласиться, поскольку уровень смертности прямо влияет на численность контингентов больных активным туберкулезом и без учета показателя болезненности. Кроме того, показатель смертности характеризует качество лечения, а также эффективность раннего выявления и диагностики. В частности, состояние диагностики туберкулеза иллюстрируется показателем смертности, а также удельным весом лиц, у которых диагноз туберкулеза поставлен только после смерти, или у больных, наблюдавшихся врачом менее года.
С эпидемиологических позиций также важно выяснить, когда наступила смерть — при пребывании больного в больнице или дома. Последнее создает большой риск для окружающих из-за рассеивания микобактерии, трудностей при проведении уборки и ухода за таким больным в домашних условиях.
Таким образом, совокупность показателей заболеваемости, болезненности и смертности позволяет не только получить представление о распространенности туберкулеза, состоянии различных разделов противотуберкулезной работы, но и оценить закономерности, определяющие эпидемический процесс как в целом по стране, так и применительно к различным ее регионам и территориям. Естественно, что в современных условиях динамика распространенности туберкулеза оценивается в условиях осуществления программы противотуберкулезных мероприятий.
Программа борьбы с туберкулезом имеет конечной целью резкое уменьшение его распространенности среди населения.
Известно, что оценка эффективности противотуберкулезных мероприятий — сложная задача, так как эпидемический процесс является динамичным, изменяющимся как в естественных условиях, так и под влиянием специальных мероприятий социально-экономического и медицинского характера. В связи с этим появилась необходимость следить за динамикой распространенности различных инфекционных заболеваний не по отдельным, разрозненным эпидемиологическим показателям, а по их совокупности в сочетании с такими факторами, как массивность инфекции, характер и продолжительность экспозиции (контакта), состояние организма лиц, соприкасающихся с инфекционным агентом, характер и качество питания населения, экологические условия и др.
Изучение совокупности всех данных, определяющих течение, масштабы и скорость распространения эпидемического процесса, его тенденции к распространению, стабилизации или уменьшению в настоящее время принято обозначать термином «сервейланс». На русском языке, с нашей точки зрения, он может соответствовать термину «эпидемиологический надзор» или «контроль».
В нашей стране проводится работа по комплексному эпидемиологическому контролю за эффективностью противотуберкулезных мероприятий на некоторых территориях и в целом по стране. Предпосылкой для развертывания этой работы явились эпидемиологические исследования, в которых были использованы как отдельные параметры, так и их совокупность. Эти исследования проводились в различных республиках в городах, районах с ограниченным числом населения (г. Родники Ивановской обл., г. Салават Башкирии, г. Клин Московской обл. и др.). Накопленный опыт позволил расширить масштабы последующих исследований, которые были проведены на 9 экспериментальных территориях.
Подведены итоги по специально разработанной единой программе. Эпидемиологический контроль предусматривал: 1) определение пораженное™ населения туберкулезом по данным сплошного флюорографического обследования с картотечным учетом результатов осмотра; 2) изучение контингентов больных, состоящих на учете в противотуберкулезных диспансерах, с вычислением таких показателей, как заболеваемость, болезненность и смертность; изучение их взаимосвязи с динамикой процесса на основе анализа первичной документации — карты диспансерного учета; 3) бактериологическую характеристику «резервуара инфекции» в плане как определения истинного числа больных туберкулезом, представляющих эпидемиологическую опасность для окружающих, так и оценки степени риска заражения в связи с массивностью бацилловыделения, типом микобактерии, их чувствительности к химиопрепаратам и др.; 4) анализ динамики распространенности тубекулеза в условиях применения комплекса противотуберкулезных мероприятий, проводящихся в соответствии с унифицированными программами по выявлению больных туберкулезом и их лечению. В связи с большими масштабами исследования и необходимостью обработки многочисленных результатов индивидуальных исследований, с их обобщением важное значение имело использование вычислительной техники.
Необходимость продолжения противотуберкулезных мероприятий в нашей стране диктуется сравнительно высокой заболеваемостью туберкулезом, а главное — еще большим резервуаром туберкулезной инфекции и большим числом инфицированных лиц с высоким риском развития заболевания.
В России и других странах, ранее входящих в состав СССР, после периода снижения заболеваемости и стабилизации этого показателя отмечается рост заболеваемости туберкулезом. В 1994 г. она составила в России 47,9 случая на 100 ООО населения (рис. 3.1). Отмечаются резко выраженные различия в уровне заболеваемости в разных регионах. В Прибалтийских странах заболеваемость туберкулезом сравнительно низкая: в 1991 г. она достигла в Эстонии 26,4, Латвии — 35,9, Литве — 41,6 случая на 100 000 населения. Заболеваемость в Белоруссии составила 36,6, на Украине — 39,0, Молдавии — 46,4 случая на 100 000 населения. Наиболее высокие показатели заболеваемости в Казахстане (70,0), Туркмении (63,5), Киргизии (60,5), Узбекистане (48,2), Таджикистане (30,7). Столь значительные различия в показателях в разных регионах бывшего СССР требуют специального разъяснения причин сложившейся эпидемиологической ситуации.
Во-первых, уровень заболеваемости туберкулезом зависит от величины резервуара инфекции, т. е. числа больных с эпидемиологически опасными формами туберкулеза. В нашей стране сохраняется довольно большой резервуар инфекции, на учете в противотуберкулезных диспансерах состоит около 200 000 больных эпидемически опасными формами туребкулеза легких, выделяющих или выделяв-