ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 23.11.2023
Просмотров: 193
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
СОДЕРЖАНИЕ
ОБЩАЯ ХАРАКТЕРИСТИКА И КЛАССИФИКАЦИЯ ФИЗИКОХИМИЧЕСКИХ МЕТОДОВ АНАЛИЗА
Основной закон светопоглощения (Закон БугераЛамбертаБера)
Основные узлы приборов абсорбционной спектроскопии
Основные узлы приборов для эмиссионного спектрального анализа
Качественный эмиссионный спектральный анализ
РЕНТГЕНОСПЕКТРАЛЬНЫЙ МЕТОД АНАЛИЗА
Основные узлы рентгеноспектральных приборов
Количественный рентгеноструктурный анализ
Качественный хроматографический анализ
КОНДУКТОМЕТРИЧЕСКИЙ МЕТОД АНАЛИЗА
Измерение электропроводности растворов
ПОТЕНЦИОМЕТРИЧЕСКИЙ МЕТОД АНАЛИЗА
Измерительная ячейка и электроды потенциометрического ме тода анализа.
уравнений (8.5.1) и (8.5.2) дает
lna = (E
— E — E0 ) · nF, (8.5.3)
 или
или
м ср
инд RT
pa = —lga
= [E — (E
— E0 )] · nF
, (8.5.4)
м м ср
инд

2,303RT
Так как аM=CM∙fM, где fM‐ коэффициент активности; CM‐ концентрация иона М, то
pC = —lgC = [E — (E
— E0 )] · nF + lgf , (8.5.5)
м м ср

инд 2,303RT м
Уравнение (8.5.5) лежит в основе нескольких аналитических приемов. Трудности, свя‐ занные с неопределенностью коэффициента активности отдельного иона, при определении pH были преодолены путём разработки шкалы pH на основе стандартных буферных рас‐ творов. Для других ионов таких стандартных растворов нет, поэтому трудности оценки ко‐ эффициентов активности отдельных ионов остаются.
В практике используется несколько приёмов ионометрии.
Уравнение (8.5.5) можно переписать в виде:
pCM = a · E + b, (8.5.6)
где a и b– константы.
 E
E
Ex
Для построения градуировочного графика в координатах E‐lgCMизмеряют ЭДС элемента при нескольких концентрациях определяемого иона. Затем определяют ЭДС, помещая индика‐ торный электрод в анализируемый раствор, и по величине ЭДС и градуировочному графику находят концентрацию иона в ана‐ лизируемом растворе.
‐lgCx
Рисунок 8.5.1
‐lgCM
.Идея метода заключается в том, что составляют концентраци‐ онный элемент с двумя индикаторными электродами и поме‐
щают один из них в раствор с известной концентрацией иона, а другой – анализи‐ руемый раствор. ЭДС этого элемента будет равна



E =
RT · ln Cстfст, (8.5.7)
nF Схfx
где Cст и Cх– концентрации стандартного и исследуемого растворов; fст и fx– коэффициенты активности определяемого иона в стандартном и исследуемом растворах.
При условии fст =fx:

E =
RT · ln Cст. (8.5.8)


nF Сх
При Cст = Cх, очевидно, ln(Cст/Сх) =0 и Е=0. Выполнить условие Е=0 можно разбавлением стандартного раствора раствором фонового электролита или добавлением более концен‐ трированного стандартного раствора.
Для применения этого метода необходимо достаточно точно знать электродную функцию по отношению к определённому иону. Обычно её находят заранее по стандартным растворам. При осуществлении метода добавок сначала определяют ЭДС цепи с анализи‐ руемым раствором Ех, затем добавляют к нему определённый объем стандартного раствора и снова измеряют ЭДС.
До добавления стандартного раствора ЭДС цепи равна
 E = E +
E = E +
RT · lnС f , (8.5.9)
а после добавления
x 0 nF x x
E = E + RT · ln(С + ∆С)f , (8.5.10)
 x+ст 0 nF x x
x+ст 0 nF x x
где ΔС – прирост концентрации определяемого иона за счет введения стандартного раство‐ ра.
Разность этих ЭДС равна
E
— E = ∆E = RT · ln Сx + ∆С = k · lg Сx + ∆С. (8.5.11)
Отсюда
x+ст



x nF Сx Сx

=
∆С
 Сx ∆E
Сx ∆E
10 k — 1
Метод добавок автоматически учитывает влияние третьих компонентов и позволяет находить концентрацию очень разбавленных растворов.
Потенциометрическое титрование основано на определении точки эквивалентность по результатам потенциометрических измерений. Вблизи точки эквивалентности происходит резкое изменение (скачок) потенциала индикаторного электрода. Например, при титрова‐ нии соляной кислоты гидрооксидом натрия (HCl + NaOH = NaCl + H2O) получается кривая титрования представленная на рисунке 8.6.1.


E∆E
∆V
ТЭ
VNaOH
ТЭVNaOH
Рисунок 8.6.1 Рисунок 8.6.2
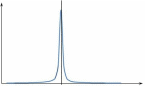
Для нахождения точки эквивалентности часто строят дифференциальную кривую в ко‐ ординатах ΔЕ/ΔV — V. (см. рисунок 8.3.2) На точку эквивалентности указывает максимум по‐ лученной кривой. Определение точки эквивалентности по дифференциальной кривой зна‐ чительно точнее, чем по простой зависимости E — V.
В простом и удобном методеГранаточка эквивалентности определяется по графику в
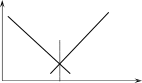 ∆V координатах ΔV/ΔE — V (см. рисунок 8.3.3).
∆V координатах ΔV/ΔE — V (см. рисунок 8.3.3).
 ∆E Достоинства и удобства метода Грана особенно заметны при анализе разбавленных растворов,
∆E Достоинства и удобства метода Грана особенно заметны при анализе разбавленных растворов,
позволяя определить точку эквивалентности с достаточной точностью вследствие линейности графика.
ТЭ
Рисунок 8.6.3
VNaOH
При титровании смеси содержащей соляную и уксусную кислоты, на кривой титрования обнаруживает два скачка. Также нескольких скачков имеют кривые титрования многооснов‐ ных кислот, константы диссоциации которых существенно различаются (хромовая, фосфор‐ ная и т.д.).
Широкие возможности анализа многокомпонентных смесей без разделения открывает применение не водных растворителей. В водных бывает трудно обнаружить двух скачков титрования раздельно, а при титровании в органическом растворителе оба скачка бывают выражены достаточно четко.
lna = (E
— E — E0 ) · nF, (8.5.3)
 или
илим ср
инд RT
pa = —lga
= [E — (E
— E0 )] · nF
, (8.5.4)
м м ср
инд

2,303RT
Так как аM=CM∙fM, где fM‐ коэффициент активности; CM‐ концентрация иона М, то
pC = —lgC = [E — (E
— E0 )] · nF + lgf , (8.5.5)
м м ср

инд 2,303RT м
Уравнение (8.5.5) лежит в основе нескольких аналитических приемов. Трудности, свя‐ занные с неопределенностью коэффициента активности отдельного иона, при определении pH были преодолены путём разработки шкалы pH на основе стандартных буферных рас‐ творов. Для других ионов таких стандартных растворов нет, поэтому трудности оценки ко‐ эффициентов активности отдельных ионов остаются.
В практике используется несколько приёмов ионометрии.
-
Методградуировочногографика
Уравнение (8.5.5) можно переписать в виде:
pCM = a · E + b, (8.5.6)
где a и b– константы.
 E
EEx
Для построения градуировочного графика в координатах E‐lgCMизмеряют ЭДС элемента при нескольких концентрациях определяемого иона. Затем определяют ЭДС, помещая индика‐ торный электрод в анализируемый раствор, и по величине ЭДС и градуировочному графику находят концентрацию иона в ана‐ лизируемом растворе.
-
Методконцентрационногоэлемента
‐lgCx
Рисунок 8.5.1
‐lgCM
.Идея метода заключается в том, что составляют концентраци‐ онный элемент с двумя индикаторными электродами и поме‐
щают один из них в раствор с известной концентрацией иона, а другой – анализи‐ руемый раствор. ЭДС этого элемента будет равна



E =
RT · ln Cстfст, (8.5.7)
nF Схfx
где Cст и Cх– концентрации стандартного и исследуемого растворов; fст и fx– коэффициенты активности определяемого иона в стандартном и исследуемом растворах.
При условии fст =fx:

E =
RT · ln Cст. (8.5.8)


nF Сх
При Cст = Cх, очевидно, ln(Cст/Сх) =0 и Е=0. Выполнить условие Е=0 можно разбавлением стандартного раствора раствором фонового электролита или добавлением более концен‐ трированного стандартного раствора.
-
Методдобавок
Для применения этого метода необходимо достаточно точно знать электродную функцию по отношению к определённому иону. Обычно её находят заранее по стандартным растворам. При осуществлении метода добавок сначала определяют ЭДС цепи с анализи‐ руемым раствором Ех, затем добавляют к нему определённый объем стандартного раствора и снова измеряют ЭДС.
До добавления стандартного раствора ЭДС цепи равна
 E = E +
E = E +
RT · lnС f , (8.5.9)
а после добавления
x 0 nF x x
E = E + RT · ln(С + ∆С)f , (8.5.10)
 x+ст 0 nF x x
x+ст 0 nF x xгде ΔС – прирост концентрации определяемого иона за счет введения стандартного раство‐ ра.
Разность этих ЭДС равна
E
— E = ∆E = RT · ln Сx + ∆С = k · lg Сx + ∆С. (8.5.11)
Отсюда
x+ст



x nF Сx Сx

=
∆С
 Сx ∆E
Сx ∆E10 k — 1
Метод добавок автоматически учитывает влияние третьих компонентов и позволяет находить концентрацию очень разбавленных растворов.
- 1 ... 14 15 16 17 18 19 20 21 22
Потенциометрическое титрование
Потенциометрическое титрование основано на определении точки эквивалентность по результатам потенциометрических измерений. Вблизи точки эквивалентности происходит резкое изменение (скачок) потенциала индикаторного электрода. Например, при титрова‐ нии соляной кислоты гидрооксидом натрия (HCl + NaOH = NaCl + H2O) получается кривая титрования представленная на рисунке 8.6.1.



E∆E
∆V
ТЭ
VNaOH
ТЭVNaOH
Рисунок 8.6.1 Рисунок 8.6.2
Для нахождения точки эквивалентности часто строят дифференциальную кривую в ко‐ ординатах ΔЕ/ΔV — V. (см. рисунок 8.3.2) На точку эквивалентности указывает максимум по‐ лученной кривой. Определение точки эквивалентности по дифференциальной кривой зна‐ чительно точнее, чем по простой зависимости E — V.
В простом и удобном методеГранаточка эквивалентности определяется по графику в
 ∆V координатах ΔV/ΔE — V (см. рисунок 8.3.3).
∆V координатах ΔV/ΔE — V (см. рисунок 8.3.3). ∆E Достоинства и удобства метода Грана особенно заметны при анализе разбавленных растворов,
∆E Достоинства и удобства метода Грана особенно заметны при анализе разбавленных растворов,позволяя определить точку эквивалентности с достаточной точностью вследствие линейности графика.
ТЭ
Рисунок 8.6.3
VNaOH
-
Видыпотенциометрическоготитрования
-
Кислотно‐основное титрование (КОТ). В КОТ в качестве индикаторного обычно ис‐ пользуют стеклянный электрод. Потенциометрический метод позволяет провести количест‐ венное определение компонентов в смеси кислот, если константы диссоциации различаются не менее чем на три порядка.
При титровании смеси содержащей соляную и уксусную кислоты, на кривой титрования обнаруживает два скачка. Также нескольких скачков имеют кривые титрования многооснов‐ ных кислот, константы диссоциации которых существенно различаются (хромовая, фосфор‐ ная и т.д.).
Широкие возможности анализа многокомпонентных смесей без разделения открывает применение не водных растворителей. В водных бывает трудно обнаружить двух скачков титрования раздельно, а при титровании в органическом растворителе оба скачка бывают выражены достаточно четко.
-
Комплексонометрическое титрование. Потенциометрическое титрование катио‐ нов комплексом (ЭДТА) можно проводить с использованием в качестве индикаторного элек‐ трода соответствующего металла: титрование солей меди с медным электродом, солей цин‐ ка с цинковым и т.д. или подходящего ионоселективного электрода. С помощью ртутного, например, электрода можно определить ионы Mg2+, Ca2+, Co2+, Ni2+, Cu2+, Zn2+ и др.
-
Титрование по методу осаждения. Индикаторными электродами в методах потен‐ циометрического титрования, использующих реакции осаждения, служат металлические или мембранные электроды, чувствительные к определённому иону или иону‐осадителю. Прак‐ тически по методу осаждения могут быть определены катионы серебра, ртути, цинка, свин‐ ца, анионы хлора, брома, йода и др. -
Окислительно‐восстановительное титрование. Любое окислительно‐ восстановительное титрование может быть проведено по измерению Е с использованием индикаторного электрода из благородного металла, чаще всего платины. -
Автоматическое титрование. Сравнительная легкость автоматизации потенцио‐ метрических измерений позволила создать ряд автоматических приборов для титрования – автотитраторов. Погрешность титрования ±1%.