ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 30.11.2023
Просмотров: 102
Скачиваний: 2
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Объект исследования: ретинол (витамин А) или рыбий жир.
4.2 Суть метода
Витамин А (ретинол) выявляют по образованию красно-бурого окраса в присутствии хлороформа в кислой среде.
4.3 Техника выполнения работы
В пробирку наливают 2 капли витамина А (рыбьего жира) и 5 капель хлороформа. Перемешивают и прибавляют 2 капли концентрированной сульфатной кислоты. Наблюдают появление окраса.
4.4. Подведение итогов
По образованию красно-бурого окраса сделать вывод о наличии в пробирке витамина А и заполнить таблицу 5.4.
Таблица 5.4 – Результаты определения витамина А – ретинола
| Название объекта | Количество, капли | ||
| Витамин А | Хлороформ | Концентрированная сульфатная кислота | |
| Ретинол | | | |
Вывод: _____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
5.Качественная реакция на витамин Е
5.1 Приборы и реактивы:
Штатив с пробирками, капельницы, концентрированная хлоридная кислота.
Объект исследования: 1% спиртовой раствор токоферола (витамин Е)
5.2 Суть метода
Витамин Е (токоферол) выявляют по образованию красного кольца на границе раздела эмульсии в кислой среде.
5.3 Техника выполнения работы
В пробирку наливают 5 капель раствора витамина Е, добавляют 10 капель хлоридной кислоты и энергично стряхивают. Наблюдают появление окраса который свидетельствует о наличии витамина Е.
5.4 Подведение итогов
По образованию окраса сделать вывод о наличии в пробирке витамина Е и заполнить таблицу 5.5.
Таблица 5.5 – Результаты определения витамина Е – токоферола
| Название объекта | Количество, капли | |
| Витамин Е | HNO3 | |
| Токоферол | | |
Вывод: ___________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
3.Качественная реакция на витамин Д
6.1 Приборы и реактивы:
Штатив с пробирками, капельницы, хлороформ, анилиновый реактив.
Объект исследования: кальциферол (витамин Д) или рыбий жир.
6.2 Суть метода
В основе метода лежит взаимодействие кальциферола с гидрохлоридом анилина с образованием тёмноокрашенных соединений красного цвета.
6.3 Техника выполнения работы
В пробирку наливают 1-2 капли раствора витамина Д, прибавляют 5 капель хлороформа и перемешивают. Потом добавляют 1 каплю анилинового реактива. Нагревают пробирки и наблюдают появление желтого, а затем красного окраса который свидетельствует о наличии витамина Д.
6.4 Подведение итогов
По образованию окраса сделать вывод о наличии в пробирке витамина Д и заполнить таблицу 5.6
Таблица 5.6 – Результаты определения витамина Д - кальциферола
| Название объекта | Количество, капли | ||
| Витамин Д | Хлороформ | Анилиновый реактив | |
| Кальциферол | | | |
Вывод: ___________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
ЛАБОРАТОРНАЯ РАБОТА №4
Тема: Количественное и качественное определение жиров
Цель: приобрести практические навыки и умения при проведении реакции на выявление жиров.
После проведения работы студент должен:
-
Знать: порядок и методы проведения реакций на выявление жиров. -
Уметь: проводить реакции на качественное и количественное выявление жиров.
Контрольные вопросы
-
Охарактеризуйте жиры по химической природе. -
Охарактеризуйте сложные и простые липиды. -
Назовите насыщенные и ненасыщенные жирные карбоновые кислоты. -
Какие основные физико-химические свойства жиров? -
Охарактеризуйте химические константы, которые используют при оценке качества липидов. -
Что такое эмульгирование жиров? -
Какое значение для пищевой промышленности имеют реакции гидролиза, гидрования, окисления глицеридов? -
Назовите жиры, которые используют в пищевой промышленности?
Ход работы
-
Инструктаж по охране труда. -
Инструктаж по выполнению работы. -
Выполнение студентами опытов и обработка результатов. -
Подведение итогов занятия. -
Оформление отчетов. -
Защита отчетов. -
Уборка рабочих мест.
-
Реакция на выявление липидов
Обеспечение работы:
-
Приборы и реактивы:
Штатив с пробирками, пипетка на 1 см3, стеклянная палочка, калий гидросульфат (сухой), фильтровальная бумага.
Пищевые образцы: растительное масло или какой-либо другой жир и воск.
-
Суть метода.
Реакцией на выявление жиров может служить акролейновая проба. Акролейновая проба присутствует в жирах в виде глицеринового остатка, при нагревании жира этот остаток частично переходит в свободный глицерин. При дальнейшем нагревании глицерин далее теряет воду, как в следствие образуется ненасыщенный альдегид – акролеин, который легко определить по специфичному запаху.
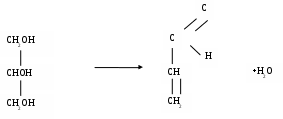
Глицерин Акролеин
Акролеин может образовываться при пережевывании еды и от присутствия его в значительном количестве зависит резкий, удушливый запах кессонного запаха. Акролеиновую пробу проводят, нагревая жир в присутствии бисульфата калия или натрия (в качестве водоотнимающего способа).
Липиды, которые не содержат глицерин (воск, жирные кислоты, стерины и т.д.) акролеиновые пробы не дают.
Также для определения жиров можно использовать их свойство оставлять на бумаге характерное масляное пятно.
-
Техника выполнения анализа
1.3.1 Проба на выявление пятна
Наносят стеклянной палочкой каплю жира на кусок бумаги. Наблюдают появление сального пятна, которое не исчезает при нагреве.
1.3.2 Акролеиновая проба
Помещают в сухую пробирку 1-2 капли жира прибавляют немного сухого сернокислого калия и нагревают до появления белых густых паров. Резкий раздражающий запах (аккуратно) свидетельствует о образовании акролеина.
Проводят ту же самую реакцию с кусочком воска. Наблюдают за тем, что при его нагревании не происходит выделения акролеина, так как молекула воска не содержит остаток глицерина.
-
Подведение итогов:
Сделать выводы о химическом составе липидов.
_____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
______________________________________________________________________________________________________________________________________________________________
-
Эмульгирование жиров
2.1 Приборы и реактивы:
Штатив с пробирками, пипетки на 1 см3, воронки, фильтрующая бумага, капельницы, 1% раствор мыла, 1% раствор натрия гидрокарбоната, раствор яичного белка, желчь.
Объект исследования: растительное масло или какой-либо другой жир и воск.
2.2 Суть метода.
Эмульгированием называется разделение одного нерастворимого вещества в другой в виде капель. Такое дробление на капли обычно осуществляется при энергичном перемешивании двух жидкостей. Чтобы эмульсия не расслаивалась, используют специальные вещества – эмульгаторы или стабилизаторы. Эмульгатор распространяется на поверхности капель дисперсной среды в виде тонкой пленки и препятствует их слиянию. Стойкость полученной эмульсии в значительной мере зависит от природы эмульгатора. Например, молочно-жировая эмульсия маргарина имеет высокую стойкость и не расслаивается при механическом действии. В отечественном маргариновом производстве как эмульгаторы используют смесь моно- и диглицериды фосфатиды сухое молоко. При изготовлении майонезов с этой целью используют яичный и горчичный порошки.
Основными эмульгаторами в желудочно-кишечном тракте являются соли желчных кислот белки фосатиды гидрокарбонаты щелочных металлов. Эмульгирование жиров способствует их лучшему всасываю в кишечнике.
2.3 Техника выполнения анализа
В пять пробирок наливают по 5 см3 дистиллированной воды. В другую пробирку вносят 1 см3 мыла, в третью – 1 см3 желчи, в четвертую – 1 см3 раствора натрия гидрокарбоната, в пятую – 1 см3 раствора яичного белка. Потом ко всем пробиркам прибавляют по 0,2 см3 масла. Пробирки энергично встряхивают и оставляют на 5 минут. В первой пробирке эмульсия быстро расслаивается на воду и масло. Во всех других пробирках благодаря присутствию желчи, мыла, белка и соли образуются стойкие эмульсии.
Содержание пробирок фильтруют через бумажные фильтры в чистые пробирки. В первую пробирку сквозь фильтр проходит прозрачный раствор, а масло остается на фильтре. Ко всем другим пробиркам сквозь фильтр проходит мутная жидкость (эмульсия).
Итак, такие вещества как желчь мыло белок соль являются стабилизаторами способствуют эмульгированию жиров и значительно облегчает их прохождение через мембраны.
2.4 Подведение итогов. Результаты опыта внести в таблицу 2.1.
Таблица 2.1. – Результаты эмульгирования жиров
| Название жира | Количество, см3 | Результаты наблюдения | |||||
| Жир | Вода | Мыло | Желчь | Натрия гидрокарбонат | Яичный белок | ||
| Масло растительное | | | | | | | |
| Жир | | | | | | | |
| Воск | | | | | | | |
-
Определение кислотного числа жира
Обеспечение работы:
-
Приборы и реактивы:
Колбы конические на 50, 100 см3 с пробирками, бюретки, пипетки, нейтрализованная смесь этилового спирта с этиловым эфиром (1:1), 0,1н раствор едкого калия, 1% раствор фенолфталеина.
Пищевые образцы: масло коровье, свежее подсолнечное масло, масло коровье после хранения, масло подсолнечное после хранения, фритюрный жир.
-
Суть метода.
Кислотное число характеризуется содержанием в жире свободных жирных кислот. Его определяют количеством миллиграммов гидроксида калия, которое необходимо для нейтрализации свободных жирных кислот в 1 г жира. Кислотное число – важный компонент качества жиров, потому что при хранении жиров или при их термической обработке его значение увеличивается за счет протекания реакций гидролиза глицеридов.
-
Техника выполнения анализа
В колбу кладут навеску массой 1 г материала, который исследуется (с расчетом разницы массы колбы до и после внесения навески), приливают 10 см3 нейтрализованной смеси спирта. Содержание колбы перемешивают до полного растворения жира. Потом прибавляют в колбу 2...3 капли раствора фенолфталеина и титруют смесь 0,1н раствором КОН до появления розового окраса. Объем раствора в бюретке отсчитывают от нуля; реактивы добавлять каплями при постоянном перемешивании смеси в колбе. Титрование проводить до появления розового окраса, который не исчезает в течение 1 минуты.