Файл: Методические указания и задания к занятиям семинарского типа, контрольной и самостоятельной работе по дисциплине Неорганическая химия.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 30.11.2023
Просмотров: 301
Скачиваний: 2
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Основания (вопрос 3)
| Молекулярная формула основания | Кислотно-основная природа | Способы получения | Химические свойства |
| | | | |
Кислоты (вопрос 4)
| Формула кислоты, ее сила | Схема диссоциации кислоты | Кислотный остаток | Формула возможной соли | |
| формула | название | |||
| | | | | |
Соли (вопрос 5)
| Молекулярная формула и тип соли | Название соли | Уравнение реакции перевода в среднюю соль | ||
| международное | русское | |||
| | | | ||
4.8. Комплексные соединения
Задания 8190
Вопросы заданий
1. Отметить состав перечисленных соединений и привести их названия.
2. Составить уравнения процессов диссоциации указанных соединений и написать выражения констант нестойкости их комплексных ионов.
| № задания | Соединения | № задания | Соединения |
| 81 | Na2[Zn(OH)4] [SnCI2(H2O)4]CI2 | 86 | K2[Pt(CN)4CI2] [Zn(NH3)6]SO4 |
| 82 | Na2[Cd(NO2)4] [FeBr2(NH3)4]NO3 | 87 | Na[BiBr4(H2O)2] [Cd(NH3)4]SO4 |
| 83 | Na5[Cu(SO3)3] [CoCI2(NH3)4]NO3 | 88 | K2[PbJ4] [CuNO2(NH3)3]CI |
| 84 | Na2[Cu(CN)4] [PtCI2(NH3)4]Br2 | 89 | Na2[Ag(OH)3] [Co(CN)2(NH3)4]CI |
| 85 | [FeCI2(H2O)4]Br Na4[AgBr5] | 90 | K2[FeF5] [CrCI2(NH3)4]CI |
Методические указания
Изучите теоретический материал данной темы по рекомендуемой литературе и уясните основные понятия и термины.
Комплексные соединения – это соединения, содержащие в своем составе сложные (комплексные) ионы, существующие как в растворе, так и в кристаллическом состоянии вещества. Комплексный ион (комплекс) составляет внутреннюю сферу комплексного соединения, а более простые ионы – его внешнюю сферу.
Центральный атом комплексного иона называется комплексообразователем, а связанные с ним анионы или нейтральные молекулы – лигáндами. Общее число лигáндов называется координационным числом.
Комплексное соединение с отрицательно заряженным комплексным ионом (комплексом) называется анионным, а с положительно заряженным - катионным комплексным соединением.
Заряд комплексного иона равен по абсолютной величине, но противоположен по знаку заряду внешней сферы. Заряд комплексообразователя (его степень окисления) вычисляют, учитывая электронейтральность молекулы комплексного соединения.
Название комплексного соединения произносят справа налево.
Название анионного комплексного соединения состоит из названия комплексного аниона и русского названия катиона внешней сферы в родительном падеже. В названии аниона перечисляют последовательно названия координационного числа, лигáндов и комплексообразователя, соблюдая определенные правила:
а) координационные числа 1, 2, 4, 6 называют соответственно: моно, ди, тетра, гекса;
б) лиганды называют с добавлением соединительной гласной «o»: OH гидроксо; CN циано; CI хлоро; F фторо; NO2 нитрито; а NH3о и H2Oо называют соответственно аммин и аква;
в) комплексообразователи (чаще всего катионы р- и d- металлов) в анионных комплексных соединениях называют по-латыни с добавлением суффикса «aт» и указанием его степени окисления.
Например: Na2[PbJ4] тетрайодоплюмбат(II) натрия.
Название катионного комплексного соединения состоит из названий аниона внешней сферы и комплексного катиона. При этом комплексообразователь называют по-русски в родительном падеже с указанием его степени окисления.
Например: [Co(NH3)6]CI2 хлорид гексаамминкобальта(II).
Ответ на первый вопрос задания оформите в виде таблицы.
Названия и состав комплексных соединений
| Формула соединения | Na2[Sn(OH)4] | [Ni(NH3)6]SO4 |
| Тип комплексного соединения | Анионное | Катионное |
| Внешняя сфера | 2 Na | SO4 2 - |
| Внутренняя сфера (комплексный ион) | [Sn(OH)4] 2 - | [Ni(NH3)6] 2 |
| Компексообразователь | Sn 2 | Ni 2 |
| Лигáнды | 4 OH- | 6 NH3 |
| Координационное число | 4 | 6 |
| Название | Тетрагидроксостаннат(II) натрия | Сульфат гексаамминникеля(II) |
Процесс диссоциации комплексных соединений протекает ступенчато. По первой ступени диссоциирует комплексное соединение по типу сильных электролитов с образованием ионов внешней и внутренней сфер:
Na2[Sn(OH)4]
 2Na + [Sn(OH)4] 2 ;
2Na + [Sn(OH)4] 2 ;[Ni(NH3)6]SO4
 [NiNH3)6] 2 + SO42 .
[NiNH3)6] 2 + SO42 .5. СПИСОК РЕКОМЕНДУЕМОЙ ЛИТЕРАТУРЫ
Основная литература
-
Неорганическая химия : учебник / Т.В. Мартынова, И.И. Супоницкая, Ю.С. Агеева. — М. : ИНФРА-М, 2018. — 336 с. + Доп. материалы [Электронный ресурс; - Режим доступа: http://www.znanium.com]. — (Высшее образование: Бакалавриат). — www.dx.doi.org/10.12737/25265. - Режим доступа: http://znanium.com/go.php?id=940420 -
Общая и неорганическая химия: учебное пособие / Под ред. Денисова В.В., Таланова В.М.. - Рн/Д: Феникс, 2018. - 144 c. -
Карапетьянц, М.Х. Общая и неорганическая химия / М.Х. Карапетьянц, С.И. Дракин. - М.: Ленанд, 2018. - 600 c.
Дополнительная литература
-
Неорганическая химия: Шпаргалка. — М.: РИОР. — 157 с. - Режим доступа: http://znanium.com/go.php?id=773830 -
Общая и неорганическая химия в креативных картах: Рабочая тетрадь / Тушакова З.Р. - М.:НИЦ ИНФРА-М, 2017. - 32 с.: 60x90 1/16 ISBN 978-5-16-106267-8 (online). - Режим доступа: http://znanium.com/go.php?id=945531
6. СОВРЕМЕННЫЕ ПРОФЕССИОНАЛЬНЫЕ БАЗЫ ДАННЫХ И ИНФОРМАЦИОННЫЕ СПРАВОЧНЫЕ СИСТЕМЫ
| | ||||||||||||||||||||||||||
| | ||||||||||||||||||||||||||
| | ||||||||||||||||||||||||||
| | ||||||||||||||||||||||||||
| | ||||||||||||||||||||||||||
| | | | | | | ||||||||||||||||||||||
| |
| ||||||||||||||||||||||||||
ПРИЛОЖЕНИЯ
Приложение 1
Изотопы некоторых элементов
| № п/п | Элементы | Изотопы | № п/п | Элементы | Изотопы |
| 1 | Азот | 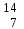 N, N, 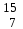 N N | 20 | Мышьяк | 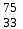 As As |
| 2 | Алюминий | 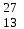 AI AI | 21 | Никель | 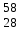 Ni, Ni, 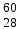 Ni Ni |
| 3 | Барий | 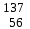 Ba, Ba, 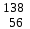 Ba Ba | 22 | Олово | 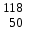 Sn, Sn, 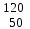 Sn Sn |
| 4 | Бор | 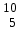 В, В, 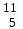 В В | 23 | Платина | 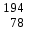 Pt, Pt, 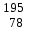 Pt Pt |
| 5 | Бром | 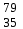 Br, Br, 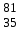 Br Br | 24 | Ртуть | 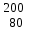 Hg, Hg, 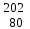 Hg Hg |
| 6 | Висмут | 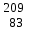 Bi Bi | 25 | Свинец | 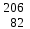 Pb, Pb, 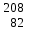 Pb Pb |
| 7 | Водород | 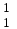 H, H, 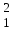 H, H, 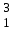 H H | 26 | Селен | 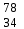 Se, Se, 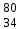 Se Se |
| 8 | Германий | 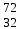 Ge, Ge, 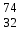 Ge Ge | 27 | Сера | 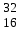 S, S, 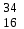 S S |
| 9 | Железо | 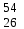 Fe, Fe, 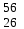 Fe Fe | 28 | Серебро | 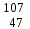 Ag, Ag, 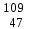 Ag Ag |
| 10 | Йод | 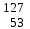 J J | 29 | Стронций | 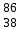 Sr, Sr, 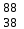 Sr Sr |
| 11 | Кадмий | 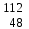 Cd, Cd, 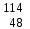 Cd Cd | 30 | Сурьма | 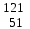 Sb, Sb, 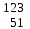 Sb Sb |
| 12 | Калий | 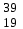 К, К, 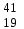 К К | 31 | Теллур | 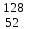 Te, Te, 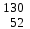 Te Te |
| 13 | Кальций | 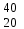 Ca, Ca, 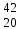 Ca Ca | 32 | Титан | 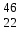 Ti, Ti, 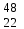 Ti Ti |
| 14 | Кислород | 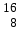 О, О, 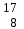 О, О, 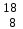 О О | 33 | Углерод | 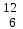 C, C, 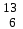 C C |
| 15 | Кобальт | 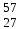 Co, Co, 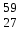 Co Co | 34 | Фосфор | 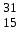 P P |
| 16 | Кремний | 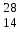 Si, Si, 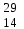 Si Si | 35 | Фтор | 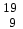 F F |
| 17 | Магний | 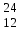 Mg, Mg, 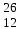 Mg Mg | 36 | Хлор | 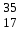 CI, CI, 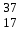 CI CI |
| 18 | Марганец | 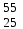 Mn Mn | 37 | Хром | 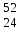 Cr, Cr, 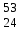 Cr Cr |
| 19 | Медь | 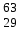 Cu, Cu, 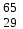 Cu Cu | 38 | Цинк | 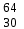 Zn, Zn, 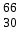 Zn Zn |