Файл: Методические указания и задания к занятиям семинарского типа, контрольной и самостоятельной работе по дисциплине Неорганическая химия.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 30.11.2023
Просмотров: 294
Скачиваний: 2
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Приложение 2
Квантовые числа
| Главное n | Побочное ℓ | Магнитное m | Спиновое S = ± ½ | Число электронов в уровне N = 2 n 2 | |||
| Энергетические уровни | Значения ℓ = 0…(n - 1) | Под-уровни | Значения m = - ℓ…0…+ ℓ | Число АО в подуровне 2 ℓ + 1 | Число ē в подуровне 2 (2 ℓ + 1) | ||
| 1 | К | 0 | 1 s | 0 | 1 | 2 | 2 |
| 2 | L | 0 1 | 2 s 2 p | 0 -1, 0, + 1 | 1 3 | 2 6 | 8 |
| 3 | M | 0 1 2 | 3 s 3 p 3 d | 0 -1, 0, + 1 - 2, - 1, 0, + 1, + 2 | 1 3 5 | 2 6 10 | 18 |
| 4 | N | 0 1 2 3 | 4 s 4 p 4 d 4 f | 0 -1, 0, + 1 - 2, - 1, 0, + 1, + 2 - 3, - 2, - 1, 0, + 1, + 2, + 3 | 1 3 5 7 | 2 6 10 14 | 32 |
Приложение 3
Относительная электроотрицательность элементов
| Номер группы | |||||||
| I | II | III | IV | V | VI | VII | VIII |
| H 2,1 | | | | | | | |
| Li 1,0 | Be 1,5 | B 2,0 | C 2,5 | N 3,0 | O 3,5 | F 4,0 | |
| Na 0,9 | Mg 1,2 | Al 1,5 | Si 1,8 | P 2,1 | S 2,6 | CI 3,0 | |
| K 0,9 | Ca 1,0 | 1,3 Sc | 1,5 Ti | 1,6 V | 1,6 Cr | 1,7 Mn | Fe Co Ni 1,9 1,9 1,9 |
| 1,9 Cu | 1,6 Zn | Ga 1,6 | Ge 1,8 | As 2,0 | Se 2,4 | Br 2,8 | |
| Rb 0,8 | Sr 1,0 | 1,2 Y | 1,5 Zr | 1,6 Nb | 1,8 Mo | 1,9 Tc | Ru Rh Pd 2,2 2,2 2,2 |
| 1,9 Ag | 1,7 Cd | In 1,7 | Sn 1,8 | Sb 1,9 | Te 2,1 | J 2,5 | |
| Cs 0,7 | Ba 0,9 | La-Lu 1,0-1,2 | 1,3 Hf | 1,5 Тa | 1,7 W | 1,9 Re | Os Ir Pt 2,2 2,2 2,2 |
| 2,4 Au | 1,9 Hg | Tl 1,9 | Pb 1,9 | Bi 1,9 | Po 2,0 | At 2,2 | |
| Fr 0,7 | Ra 0,9 | Ac-Md 1,1-1,2 | | | | | |
Приложение 4
Нормальное и возбужденное состояние атомов
элементов второго периода
| Элемент | Нормальное состояние | Возбужденное состояние | ||||||
| 2 s | 2 p x | 2 p y | 2 p z | 2 s | 2 p x | 2 p y | 2 p z | |
| Li | | | | | − | |||
| Be | ¯ | | | | | | | |
| B | ¯ | | | | | | | |
| C | ¯ | | | | | | | |
| N | ¯ | | | | − | |||
| O | ¯ | ¯ | | | − | |||
| F | ¯ | ¯ | ¯ | | − | |||
| Ne | ¯ | ¯ | ¯ | ¯ | − | |||
Приложение 5
Термодинамические константы некоторых веществ
| Вещество | DН 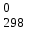 , ,кДж / моль | DS 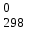 Дж / (моль×град) | DG 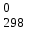 кДж / моль | |||
| 1 | 2 | 3 | 4 | |||
| AI (к) | 0 | 28,31 | 0 | |||
| AI2O3 (к) | -1675,0 | 50,94 | -1576,4 | |||
| AICI3 (к) | -697,4 | 167,0 | -636,8 | |||
| AI2S3 (к) | -723,4 | 96,0 | -492,5 | |||
| AI2(SO4)3 (к) | -3434,0 | 239,2 | -3091,9 | |||
| As2O3 (к) | -656,8 | 107,1 | -575,0 | |||
| As2O5 (к) | -916,0 | 105,4 | -772,4 | |||
| H3AsO3 (р) | -742,2 | 179,5 | -640,5 | |||
| H3AsO4 (р) | -902,5 | 205,0 | -765,7 | |||
| BaO (к) | -556,6 | 70,3 | -528,4 | |||
| BaCO3 (к) | -1202,0 | 112,1 | -1138,8 | |||
| C (алмаз) | 1,897 | 2,38 | 2,866 | |||
| C (графит) | 0 | 5,74 | 0 | |||
| CO (г) | -100,6 | 197,4 | -137,3 | |||
| CO2 (г) | -393,5 | 213,7 | -394,4 | |||
| COCI2 (г) | -220,3 | 283,9 | 266,9 | |||
| CS2 (ж) | 88,7 | 151,0 | 64,4 | |||
| CH4 (г) | -74,85 | 186,19 | -50,79 | |||
| C2H2 (г) | -227,4 | 200,8 | 209,2 | |||
| C2H4 (г) | 52,28 | 219,4 | 68,12 | |||
| C2H6 (г) | -84,67 | 229,5 | -32,89 | |||
| CH3OH (ж) | -238,7 | 126,7 | -166,31 | |||
| C2H5OH (ж) | 227,6 | 160,7 | -174,77 | |||
| C6H12O6 (к) | -1273,0 | - | -919,5 | |||
| Ca (к) | 0 | 41,62 | 0 | |||
| CaO (к) | -635,1 | 39,7 | -604,2 | |||
| Ca(OH)2 (к) | -986,6 | 76,1 | -896,8 | |||
| CaC2 (к) | -62,7 | 70,3 | -67,8 | |||
| CaCO3 (к) | -1206,0 | 92,9 | -1128,8 | |||
Продолжение прил. 5
| 1 | 2 | 3 | 4 |
| Ca3(PO4)2 (к) | -4125,0 | 240,9 | -3899,5 |
| CI2 (г) | 0 | 223,0 | 0 |
| HCI (г) | -92,3 | 186,7 | -95,3 |
| HCI (ж) | -167,5 | 55,2 | -131,2 |
| Cu (к) | 0 | 33,3 | 0 |
| CuO (к) | -165,3 | 42,6 | -127,2 |
| Fe (к) | 0 | 27,2 | 0 |
| FeO (к) | -263,7 | 58,8 | -244,4 |
| Fe2O3 (к) | -821,3 | 90,0 | -741,0 |
| Fe3O4 (к) | -1117,1 | 142,6 | -1014,2 |
| H2 (г) | 0 | 130,6 | 0 |
| H2O (г) | -241,82 | 188,72 | -228,61 |
| H2O (ж) | -285,84 | 70,1 | -237,3 |
| H2S (г) | -21,0 | 205,7 | -33,8 |
| K (к) | 0 | 64,4 | 0 |
| K2O (к) | -361,5 | 87,0 | -193,3 |
| KNO2 (к) | -370,3 | 117,2 | -281,6 |
| KNO3 (к) | -492,7 | 132,9 | -393,1 |
| Mg (к) | 0 | 32,6 | 0 |
| MgO (к) | -601,2 | 27,0 | -569,6 |
| Mg(OH)2 (к) | -924,7 | 63,14 | -833,7 |
| MgCO3 (к) | -1096,2 | 65,7 | -1029,3 |
| N2 (г) | 0 | 191,5 | 0 |
| N2O (г) | 81,55 | 220,0 | 103,6 |
| NO (г) | 90,37 | 210,6 | 86,69 |
| NO2 (г) | 33,89 | 240,5 | 51,86 |
| HNO3 (ж) | -173,0 | 156,2 | -79,91 |
| NH3 (г) | -46,19 | 192,5 | -16,64 |
| NH4CI (к) | -315,4 | 94,6 | -343,64 |
| Na (к) | 0 | 51,4 | 0 |
| Na2O (к) | -430,6 | 71,1 | -376,6 |
| NaOH (к) | -426,6 | 64,2 | -377,0 |
| NaCI (к) | -410,9 | 72,4 | -384,0 |
Окончание прил. 5
| 1 | 2 | 3 | 4 |
| Na2SiO3 (к) | -1518,0 | 113,8 | -1426,7 |
| Na2CO3 (к) | -1129,0 | 136,0 | -1047,7 |
| NiO (к) | -239,7 | 38,0 | -211,6 |
| O2 (г) | 0 | 205,03 | 0 |
| P2O5 (к) | -1492,0 | 114,5 | -1348,8 |
| PCI5 (к) | -369,45 | 362,9 | -324,55 |
| Pb (к) | 0 | 64,9 | 0 |
| PbO (к) | -217,86 | 67,4 | -188,49 |
| PbO2 (к) | -276,6 | 76,44 | -218,99 |
| S (к) | 0 | 31,8 | 0 |
| SO2 (г) | -296,8 | 248,1 | -300,37 |
| SO3 (г) | -395,8 | 256,7 | -371,1 |
| SiO2 (к) | -859,3 | 42,09 | -800,75 |
| SnO (к) | -286,0 | 56,5 | -256,9 |
| SnO2 (к) | -580,8 | 52,3 | -519,3 |
| Zn (к) | 0 | 41,59 | 0 |
| ZnO (к) | -349,0 | 43,5 | -318,19 |
| ZnS (к) | -201,0 | 57,5 | -198,32 |
| ZnSO4 (к) | -978,2 | 124,6 | -871,67 |
Приложение 6
Плотность и концентрация растворов
некоторых кислот и щелочей при температуре 20 0С
| Плотность, г/мл | Массовая доля, % | Плотность, г/мл | Массовая доля, % | |
| 1 | 2 | 3 | 4 | |
| Соляная кислота - HCI | ||||
| 1,02 | 4,39 | 1,09 | 18,43 | |
| 1,03 | 6,43 | 1,10 | 20,39 | |
| 1,04 | 8,49 | 1,11 | 22,33 | |
| 1,05 | 10,52 | 1,12 | 24,25 | |
| 1,06 | 12,51 | 1,13 | 26,20 | |
| 1,07 | 14,50 | 1,14 | 28,18 | |
| 1,08 | 16,47 | 1,15 | 30,14 | |
| Серная кислота - H2SO4 | Азотная кислота - HNO3 | |||
| 1,02 | 3,24 | 1,02 | 3,98 | |
| 1,04 | 6,24 | 1,04 | 7,53 | |
| 1,06 | 9,13 | 1,06 | 10,97 | |
| 1,08 | 11,95 | 1,08 | 14,31 | |
| 1,10 | 14,73 | 1,10 | 17,58 | |
| 1,12 | 17,43 | 1,13 | 22,38 | |
| 1,14 | 20,08 | 1,15 | 25,48 | |
| 1,16 | 22,87 | 1,17 | 28,51 | |
| 1,18 | 25,21 | 1,19 | 31,47 | |
| 1,20 | 27,72 | 1,20 | 32,94 | |
| Гидроксид калия - KOH | Гидроксид натрия - NaOH | |||
| 1,005 | 0,74 | 1,005 | 0,600 | |
| 1,059 | 5,66 | 1,050 | 4,655 | |
| 1,080 | 8,89 | 1,080 | 7,380 | |
| 1,095 | 10,49 | 1,095 | 8,740 | |
| 1,110 | 12,08 | 1,110 | 10,10 | |
| 1,200 | 21,38 | 1,200 | 18,26 | |
| 1,290 | 30,21 | 1,33 | 30,20 | |
Приложение 7
Степень диссоциации кислот, оснований, солей
| Название электролита | Формула | Степень диссоциации (a), % | ||||||
| 1 н | 0,1 н | |||||||
| 1 | 2 | 3 | 4 | |||||
| Кислоты | ||||||||
| Йодоводородная | HJ | | 95 | |||||
| Бромоводородная | HBr | | 93 | |||||
| Азотная | HNO3 | | 92 | |||||
| Соляная | HCI | 82 | 91 | |||||
| Серная | H2SO4 | 51 | 58 | |||||
| Щавелевая | H2C2O4 | | 31 | |||||
| Фосфорная | H3PO4 | | 26 | |||||
| Сернистая | H2SO3 | | 20 | |||||
| Фтороводородная | HF | | 15 | |||||
| Уксусная | CH3COOH | 0,4 | 1,3 | |||||
| Сероводородная | H2S | | 0,07 | |||||
| Борная | H3BO3 | | 0,01 | |||||
| Синильная | HCN | | 0,007 | |||||
| Основания (гидроксиды) | ||||||||
| Гидроксид калия (едкое кали) | KOH | 77 | 89 | |||||
| Гидроксид натрия (едкий натр) | NaOH | 73 | 84 | |||||
| Гидроксид аммония (гидрат аммиака) | NH4OH NH3×H2O | 0,4 | 1,3 | |||||
| Соли | ||||||||
| Типа Me +An - | KCI, NaNO3 | | 85 | |||||
| Типа Me2 +An 2 - Типа Me 2 +An2- | K2CO3 Ca(NO3)2 | | 74 73 | |||||
| Типа Me3 +An 3 - Типа Me 3 +An3- | K3PO4 AICI3 | | 65 60 | |||||
| Типа Me 2 +An 2 - | CuSO4, ZnSO4 | | 40 | |||||