ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 04.12.2023
Просмотров: 124
Скачиваний: 3
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
В
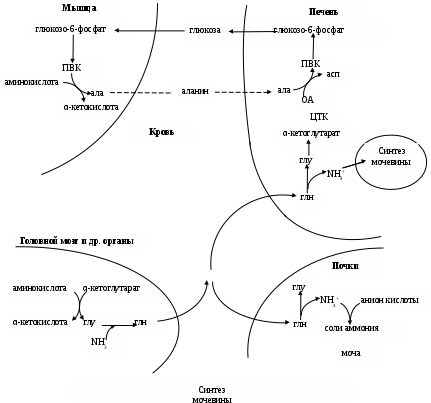 заимоотношения между переаминированием и дезаминированием хорошо иллюстрируются глюкозо-аланиновым циклом (Схема 2),с помощью которого из мышц переносятся Н2N-группы в печень, где преобразуются в мочевину, а миоциты обеспечиваются глюкозой, получившейся в гепатоцитах путем ГНГ из аланина.
заимоотношения между переаминированием и дезаминированием хорошо иллюстрируются глюкозо-аланиновым циклом (Схема 2),с помощью которого из мышц переносятся Н2N-группы в печень, где преобразуются в мочевину, а миоциты обеспечиваются глюкозой, получившейся в гепатоцитах путем ГНГ из аланина. Особенности катаболизма циклических аминокислот
Несмотря на то, что на сходный способ распада циклических аминокислот приходится около 1%, он приобретает особое значение при генетической патологии, когда вследствие точечной мутации блокируется активность одного из физиологических ферментов и тогда накапливающийся субстрат подвергается преобразованиям, сходным с обычным распадом ПВК, но с образованием токсичных продуктов.
Все циклические аминокислоты (фен, тир, три, гис) отличаясь радикалами, в своей основе имеют аланин, который при переаминировании дает ПВК, где в качестве радикала могут служить индол, имидазол, фенол, бензол. Дальнейшие реакции можно изобразить в следующей схеме:
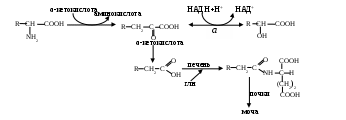
Если в клетке на данный момент гипоксия, при этом растет концентрация НАДН+Н+, чтобы не смещался рН, восстановленная форма НАД отдает свои водороды гомологам ПВК. Эта реакция (а) тупиковая - как только давление О2 приходит в норму, полученные соединения вновь окисляются в исходные вещества, которые в митохондриях подвергаются преобразованиям, сходным с окислительным декарбоксилированием пирувата. Большая часть получившихся при этом метаболитов циклических аминокислот токсична, поэтому они отправляются в печень для обезвреживания. Для этих целей обычно используется глутамин, который взаимодействуя с конечным соединением, инактивирует его, и последний током крови доставляется в почки выделяется в составе мочи (см. Приложение, табл. 5).
Классическим примером опасности появления подобных продуктов в необычных количествах служит наследственное заболевание, получившее название по одному из них - фенилкетонурия (олигофрения фенилпирувика). Его причина – генетический блок фенилаланин -4 -гидроксилазы. В этих условиях сохраняющийся фенилаланин

Схема преобразований циклических аминокислот
подвергается вышеописанным изменениям и в крови появляются патологические продукты:
фенил-ПВК, фенил-лактат, фенилацетат; легко преодолевая гематоэнцефалический барьер, они вызывают повреждения в ЦНС.
Судьба продуктов распада аминокислот
В отличие от углеводов и нейтральных жиров, при катаболизме которых образуются лишь СО2 и Н2О, при распаде аминокислот конечным продуктом, кроме вышеназванных веществ, является аммиак. Учитывая его вероятные токсические эффекты, следует остановиться на способах обезвреживания.
Пути обезвреживания NН3
Свободный аммиак токсичен. Во-первых, он обладает хорошей растворимостью в воде, что сопровождается следующей реакцией:
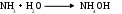
Ее продукт - сильная щелочь, что грозит развитием алкалоза. Во-вторых, нарушается ЦТК, так как его метаболит – α-кетоглутарат – используется клеткой для нейтрализации гидроксида аммония. Образующаяся и накапливающаяся при этом глутаминовая кислота повреждает баланс аминокислот, в ЦНС ее гиперпродукция провоцирует декарбоксилирование, т.е. генез ГАМК, отсюда изменяется равновесие среди тормозных и возбуждающих медиаторов.
Клинически накопление аммония (гипераммониемия) проявляется рвотой, судорогами, спутанностью и помутнением сознания, вплоть до комы. Поэтому в клетках существуют следующие механизмы, предотвращающие развитие этого явления:
1) Восстановительное аминирование:
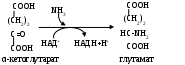


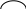

2) Во многих тканях (головном мозгу, печени, почках, мышцах) обезвреживание осуществляется путем синтеза глутамина (реже аспарагина) - нейтрального нетоксического вещества, способного диффундировать через мембраны (одна из форм транспорта NН3).
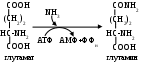
Амидная группа глутамина часто используется в реакциях аминирования (в получении глюкозамина, галактозамина, заменимых аминокислот и т.д.)
3) Работа внутри- и внеклеточных буферных систем; с помощью которых нейтрализуется NН
4ОН до солей аммония.
Продукты обезвреживания аммиака (глн, асн, соли аммония) кровотоком доставляются в гепатоциты, где и происходит окончательная инактивация данного соединения:
4) Синтез мочевины.
Мочевина – полный амид угольной кислоты, значит субстратами в ее образовании служат различные формы углекислоты (НСО3– или карбоксибиотин) и аммиака (амидная группа глутамина или соль аммония): Первая реакция:
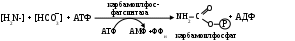
протекает в митохондриях, здесь карбамоилфосфат взаимодействует с орнитином, служащим своеобразным катализатором, вследствие чего данный процесс известен как орнитиновый цикл синтеза мочевины:
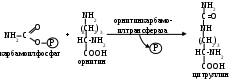
образовавшийся при этом цитруллин, выходя из митохондрий изомеризуется в енольную форму:
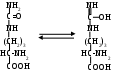
С
аргининосукцинат
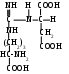
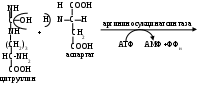 помощью специфической лигазы - аргининосукцинатсинтазы взаимодействует с аспарагиновой кислотой:
помощью специфической лигазы - аргининосукцинатсинтазы взаимодействует с аспарагиновой кислотой: 

Аргининосукцинат из-за наличия сильно поляризованных связей довольно легко разрушается с помощью аргининосукцинатлиазы:
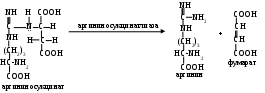
П
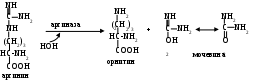 родукт данной реакции фумарат обычно отправляется в митохондрии, где включается в ЦТК, а аргинин гидролизуется до мочевины и орнитина.
родукт данной реакции фумарат обычно отправляется в митохондрии, где включается в ЦТК, а аргинин гидролизуется до мочевины и орнитина. 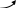
Последний вновь связывается с молекулой карбамоилфосфата, начиная новый цикл.
Суммарно:
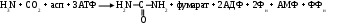
Подводя итог, следует заметить, что в целом мочевина собирает все атомы азота аминокислот: ее одна аминогруппа взята из аспартата, который может получиться путем переаминирования оксалоацетата с любой аминокислотой, другая же аминогруппа является производной аммиака, высвободившегося с помощью дезаминирования.
Двухколесный велосипед Кребса – так называют исследователи два цикла, описанные Г. Кребсом из–за их тесной связи между собой (Схема).
Цикл трикарбоновых кислот, тесно сопряженный с биологическим окислением и окислительным фосфорилированием, не только является поставщиком ОА для переаминирования в аспартат, но и дает СО2, НОН, АТФ для запуска и течения орнитинового цикла, одним из продуктов которого и является фумарат, служащий метаболитом ЦТК.
Нормальное течение синтеза мочевины обеспечивает:
1. окончательное обезвреживание аммиака;
2. избавление организма от NH3 и CO2;
3. баланс рН, поддерживая гомеостаз бикарбонатной буферной системы.
Для контроля нормального течения метаболизма азотсодержащих соединений, и в основном, процессов обезвреживания аммиака в клинике
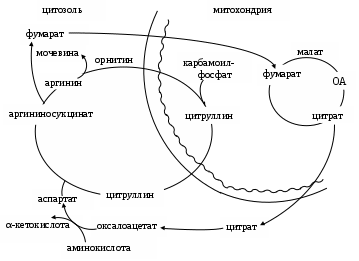
Схема. Взаимосвязь между ЦТК с орнитиновым циклом.
служит определение в крови следующего показателя -остаточного азота (Rest W) – т.е. оценивается суммарное содержание низкомолекулярных азотистых веществ, которые остаются фильтрате после осаждения белков. В их общем количестве около половины приходится на мочевину, 25% составляет доля аминокислот, величины креатина укладываются в 5%, ураты в 4% и т. д.
В норме значения остаточного азота колеблются в пределах 14–25 ммоль/л, у новорожденных они выше (42–71 ммоль/л). При различных патологических состояниях регистрируется гиперазотемия. В зависимости от механизмов возникновения выделяют продукционную и ретенционную гиперазотемии. Первый вариант может быть спровоцирован систематическим избыточным поступлением пищевых белков (у «мясоедов»), усиленный деструкцией тканей, сопровождающейся ускоренным распадом белков (при опухолях, лейкозах, ожоговой болезни и т.д.). Основной причиной ретенционной гиперазотемии служат обычно болезни почек при нарушении их выделительной способности, что обуславливает избыточное накопление в плазме крови мочевины. Кроме того, рост величин остаточного азота может наблюдаться при сердечно–сосудистой декомпенсации, при непроходимости кишечника (усилено всасывание продуктов гниения), сахарном диабете и т.д.
В последние годы стали проводить количественное определение отдельных компонентов остаточного азота – аминокислот (например, гипер-аминоацидемия при усиленном гидролизе тканевых белков распадающихся тканей) и мочевины (гиперкарбамидемия при болезнях почек). Гипокарбамидемия встречается довольно редко, обычно это следствие мутаций ферментов – участников орнитинового цикла (см. «Патохимия наследственных болезней» С. 57).
Анаболизм аминокислот
Появление аминокислот (см. Приложение, т.1) в клетке может носить двойной характер. Для основной их части требуется поступление в организм в составе пищевых белков. Если пропорции содержащихся в них аминокислот близки к таковым у человека, то в кишечнике происходит их полное усвоение, поэтому такие протеины называют полноценными; те же аминокислоты, анаболическая фаза носит экзогенный характер, называются незаменимыми (фен, лей, иле, лиз, мет, три, тре, вал). К заменимым относят 8 их аналогов, они могут всасываться в кишечнике после переваривания белков и могут синтезироваться в тканях человека. Для некоторых аминокислот этот процесс очень прост – переаминирование. Таким способом легко получить из
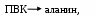
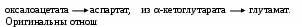
О
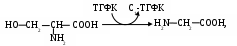 ригинальны отношения между серином и глицином:
ригинальны отношения между серином и глицином:Серин Глицин
где ТГФК – активная форма фолиевой кислоты (витамина Вс).
Восемь заменимых аминокислот (ала, сер, гли, глу, асп и т. д.) легко получаются также при преобразованиях глюкозы и метаболитов гликолиза, ЦТК. Глутаминовая кислота после некоторых реакций может циклизоваться в пролин. Некоторые аминокислоты относят к условно заменимым, т.е. тем, синтез которых зависит строго от конкретных соединений:
Тирозин – продукт гидроксилирования только фенилаланина, аргинин является метаболитом орнитинового цикла синтеза мочевины, цистеин получается из метионина.
Особенности обмена отдельных аминокислот.
Общим для большинства аминокислот является использование их в генезе белков, поэтому такие представители называют протеиногенными. Но в клетках регистрируются их аналоги, которые не обнаруживаются в полипептидных цепях. Например, орнитин, цитруллин – метаболиты только орнитинового цикла синтеза мочевины, ГАМК – медиатор, гомоцистеин – продукт метаболизма метионина, β–аланин – компонент HSKoA и т.д.
Протеиногенные аминокислоты также, кроме своей вышеназванной основной роли и преобразования в свои аналоги, выполняют специфические, характерные только для них функции. Самый простейший представитель – глицин – служит субстратом в синтезе гема – простетической группы гемопротеидов (гемоглобина, миоглобина, каталазы, пероксидазы, цитохромов), пуриновых оснований (аденина, гуанина – главных компонентов нуклеотидов), включается в состав парных жёлчных кислот (гликохолевой, гликодезоксихолевой кислот), участник генеза креатина, который в мышцах в виде креатинфосфата является макроэргом.