Файл: белорусский государственный технологический университет.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 11.12.2023
Просмотров: 1125
Скачиваний: 1
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
БГТУ)
Одним из широко распространенных загрязнителей промышлен- ных сточных вод являются тяжелые металлы. Они хорошо сорбиру- ются клетками активного ила (АИ) и не позволяют использовать его в качестве удобрений.
Для детоксикации иловых осадков и удаления из них тяжелых ме- таллов могут быть использованы комплексоны, хорошо связывающие тяжелые металлы [1]. Одним из них является этилендиаминтетрауксус- ная кислота (ЭДТА).
Цель работы – анализ детоксикации активного ила и ее влияние на редуктазную активность микроорганизмов.
Объектом исследования служил АИ влажностью 99,9%, отобран- ный из иловой камеры МОС-1. Адсорбционные свойства иловых осад- ков до и после обработки ЭДТА определяли стационарным методом, строя изотермы мономолекулярной сорбции (а) при Т = 20оС от концен- трации ионов железа [2]. Величину адсорбции аопределяли как
 а= (C0 – Ср) V,
а= (C0 – Ср) V,
m
где Со, Ср – текущая и равновесная концентрации ионов Fe3+ в надоса- дочной жидкости; m – масса адсорбента в пересчете на абсолютно су- хое вещество, г.
Максимальную удельную емкость (а∞) определяли в соответст- вии с уравнением Ленгмюра, преобразуя его в обратных координатах
1/а = 1/а∞ + (1/а∞ ∙ К)∙ 1/Ср
Обработку ила ЭДТА проводили 1 ч при их соотношении 20:1. Осадок промывали водой при центрифугировании 6000 об/мин, 5 мин.
Далее анализировали способность обработанного осадка связывать ионы железа, как описано выше, а также определяли редуктазную ак- тивность клеток. Для этого использовали метод оптико–редуктазной пробы с метиленовым синим (МС) [3], регистрируя кинетику измене- ния Д660 красителя в анаэробных условиях на спектрофотометре Specord UV-VIS.
На рисунке 1 приведены результаты анализа максимальной ад- сорбционной емкости активного ила до и после его обработки ЭДТА, а также изменения его редуктазной активности (рисунок 2).
А∞, мг/г
 Рисунок 1 – Адсорбционная емкость активного ила до (1) и после (2) обработки ЭДТА
Рисунок 1 – Адсорбционная емкость активного ила до (1) и после (2) обработки ЭДТА
Как видно из рисунка 1, ЭДТА-обработка удаляет связанные тя- желые металлы и снижает токсичность иловых осадков, а также увели- чивает его сорбционную емкость в 4,5 раза. Это позволяет использо- вать ЭДТА для детоксикации ила. Отработанный АИ обладает доста- точно высокой редуктазной активностью (рисунок 2, 1).
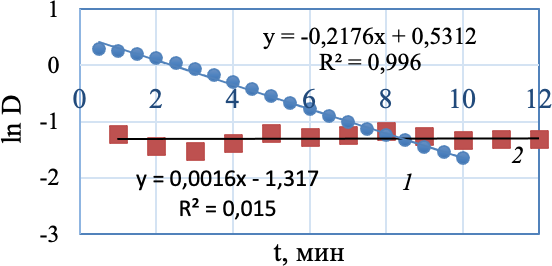
Рисунок 2 – Кинетика изменения (D/Do)660 при восстановлении метиленового синего микроорганизмами активного ила
до (1) и после (2) ЭДТА обработки и полулогарифмических координатах
Обработка АИ ЭДТА приводит к снижению редуктазной активно- сти клеток на два порядка (рисунок 2, 2). Таким образом, ЭДТА обра- ботка позволяет детоксицировать иловые осадки и снизить их токсич- ность в 4,5 раза, при этом нарушается жизнеспособность клеток
АИ
ЛИТЕРАТУРА
УДК 577.151+577.152.18
Студ. И.Ф. Тумилович
Науч. рук. доц. А.В. Игнатенко (кафедра биотехнологии, БГТУ)
Одной из устойчивых тенденций развития мирового молочного рынка является получение безлактозного молока и молочных продуктов в виду непереносимости лактозы у 50–90% населения стран Азии, Аф- рики, Южной Америки. Для получения безлактозной продукции необ- ходимы ферменты β–галактозидазы, которые в РБ не производятся [1]. Для получения β–галактозидаз могут использоваться различные лакто- зоутилизирующие микроорганизмы, прежде всего грибы, в виду выра- ботки ими экзоферментов, что облегчает их выделение. Однако актив- ность данных ферментов невысока и для ее увеличения требуется нара- щивание большой биомасссы клеток [2].
Цель работы – выбор способов получения β–галактозидаз из Гр+ и Гр– бактерий и сравнение их активности.
Объектом исследования служила творожная молочная сыво- ротка. В качестве продуцентов фермента β–галактозидазы использо- вали Гр+ бактерии B. subtilis и Гр– бактерии E. coli из коллекции ка- федры БТ БГТУ. Клетки культивировали на подготовленной молочной сыворотке. Для этого проводили осаждение белков 4% CaCl2, центри- фугирование при 6000 об/мин, 5 мин, пастеризацию сыворотки при 70оС 30 мин. В качестве критериев выбора продуцентов служили 3 по- казателя: 1) максимальная удельная скорость роста, 2) максимальная получаемая биомасса клеток, 3) максимальная активность β–галактози- даз. Биомассу клеток определяли по оптической плотности (D) свето- рассеивания клеток при 600 нм. Удельную скорость роста клеток нахо- дили по формуле:
µ = d(lnD)/dt
Для контроля активности β–галактозидаз использовали рефрак-
ДЕТОКСИКАЦИЯ АКТИВНОГО ИЛА И ЕЕ ВЛИЯНИЕ НА РЕДУКТАЗНУЮ АКТИВНОСТЬ МИКРООРГАНИЗМОВ
Одним из широко распространенных загрязнителей промышлен- ных сточных вод являются тяжелые металлы. Они хорошо сорбиру- ются клетками активного ила (АИ) и не позволяют использовать его в качестве удобрений.
Для детоксикации иловых осадков и удаления из них тяжелых ме- таллов могут быть использованы комплексоны, хорошо связывающие тяжелые металлы [1]. Одним из них является этилендиаминтетрауксус- ная кислота (ЭДТА).
Цель работы – анализ детоксикации активного ила и ее влияние на редуктазную активность микроорганизмов.
Объектом исследования служил АИ влажностью 99,9%, отобран- ный из иловой камеры МОС-1. Адсорбционные свойства иловых осад- ков до и после обработки ЭДТА определяли стационарным методом, строя изотермы мономолекулярной сорбции (а) при Т = 20оС от концен- трации ионов железа [2]. Величину адсорбции аопределяли как
 а= (C0 – Ср) V,
а= (C0 – Ср) V,m
где Со, Ср – текущая и равновесная концентрации ионов Fe3+ в надоса- дочной жидкости; m – масса адсорбента в пересчете на абсолютно су- хое вещество, г.
Максимальную удельную емкость (а∞) определяли в соответст- вии с уравнением Ленгмюра, преобразуя его в обратных координатах
1/а = 1/а∞ + (1/а∞ ∙ К)∙ 1/Ср
Обработку ила ЭДТА проводили 1 ч при их соотношении 20:1. Осадок промывали водой при центрифугировании 6000 об/мин, 5 мин.
Далее анализировали способность обработанного осадка связывать ионы железа, как описано выше, а также определяли редуктазную ак- тивность клеток. Для этого использовали метод оптико–редуктазной пробы с метиленовым синим (МС) [3], регистрируя кинетику измене- ния Д660 красителя в анаэробных условиях на спектрофотометре Specord UV-VIS.
На рисунке 1 приведены результаты анализа максимальной ад- сорбционной емкости активного ила до и после его обработки ЭДТА, а также изменения его редуктазной активности (рисунок 2).
А∞, мг/г
 Рисунок 1 – Адсорбционная емкость активного ила до (1) и после (2) обработки ЭДТА
Рисунок 1 – Адсорбционная емкость активного ила до (1) и после (2) обработки ЭДТА Как видно из рисунка 1, ЭДТА-обработка удаляет связанные тя- желые металлы и снижает токсичность иловых осадков, а также увели- чивает его сорбционную емкость в 4,5 раза. Это позволяет использо- вать ЭДТА для детоксикации ила. Отработанный АИ обладает доста- точно высокой редуктазной активностью (рисунок 2, 1).

Рисунок 2 – Кинетика изменения (D/Do)660 при восстановлении метиленового синего микроорганизмами активного ила
до (1) и после (2) ЭДТА обработки и полулогарифмических координатах
Обработка АИ ЭДТА приводит к снижению редуктазной активно- сти клеток на два порядка (рисунок 2, 2). Таким образом, ЭДТА обра- ботка позволяет детоксицировать иловые осадки и снизить их токсич- ность в 4,5 раза, при этом нарушается жизнеспособность клеток
АИ
ЛИТЕРАТУРА
-
Климов Е. С., Бузаева М. В. Природные сорбенты и комплек- соны в очистке сточных вод. Ульяновск: УлГТУ, 2011. -
ПНД Ф 14.1:2:4.50-96. Методика измерений массовой концен- трации железа в питьевых, поверхностных и сточных водах фотомет- рическим методом с сульфосалициловой кислотой. М.: ФБУ ФЦАО, 2011. -
Игнатенко, А. В. Биотестирование токсичности водных сред методом редуктазной пробы / А. В. Игнатенко // Труды БГТУ. Сер. 2, Химические технологии, биотехнологии, геоэкология. – Минск: БГТУ, 2018. – № 2 (211). – С. 155–160.
УДК 577.151+577.152.18
Студ. И.Ф. Тумилович
Науч. рук. доц. А.В. Игнатенко (кафедра биотехнологии, БГТУ)
ХАРАКТЕРИСТИКА β–ГАЛАКТОЗИДАЗНОЙ АКТИВНОСТИ ГР+ И ГР- БАКТЕРИЙ
Одной из устойчивых тенденций развития мирового молочного рынка является получение безлактозного молока и молочных продуктов в виду непереносимости лактозы у 50–90% населения стран Азии, Аф- рики, Южной Америки. Для получения безлактозной продукции необ- ходимы ферменты β–галактозидазы, которые в РБ не производятся [1]. Для получения β–галактозидаз могут использоваться различные лакто- зоутилизирующие микроорганизмы, прежде всего грибы, в виду выра- ботки ими экзоферментов, что облегчает их выделение. Однако актив- ность данных ферментов невысока и для ее увеличения требуется нара- щивание большой биомасссы клеток [2].
Цель работы – выбор способов получения β–галактозидаз из Гр+ и Гр– бактерий и сравнение их активности.
Объектом исследования служила творожная молочная сыво- ротка. В качестве продуцентов фермента β–галактозидазы использо- вали Гр+ бактерии B. subtilis и Гр– бактерии E. coli из коллекции ка- федры БТ БГТУ. Клетки культивировали на подготовленной молочной сыворотке. Для этого проводили осаждение белков 4% CaCl2, центри- фугирование при 6000 об/мин, 5 мин, пастеризацию сыворотки при 70оС 30 мин. В качестве критериев выбора продуцентов служили 3 по- казателя: 1) максимальная удельная скорость роста, 2) максимальная получаемая биомасса клеток, 3) максимальная активность β–галактози- даз. Биомассу клеток определяли по оптической плотности (D) свето- рассеивания клеток при 600 нм. Удельную скорость роста клеток нахо- дили по формуле:
µ = d(lnD)/dt
Для контроля активности β–галактозидаз использовали рефрак-