Файл: Конспект лекций для студентов специальности 1 48 01 02 Химическая технология органических веществ, материалов и изделий.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 12.01.2024
Просмотров: 1249
Скачиваний: 1
СОДЕРЖАНИЕ
Основные понятия и определения
Направленность ковалентной связи. Гибридизация орбиталей
Насыщаемость ковалентной связи
5 Общие свойства растворов. Идеальные растворы. Законы Рауля
Если в раствор добавить, например гидроксид натрия
Влияние pH на растворимость электролитов
Преимущественное направление ионно-молекулярных реакций
Получение заданного вещества реакцией обмена
Восстановители-металлы (простые вещества)
Составление материального баланса в полуреакциях
Комплексные соединения в окислительно-восстановительных реакциях
Электронный баланс в полуреакциях
Уравнение Нернста для металлического электрода
Электрохимический ряд металлов
Материальный баланс электрохимических реакций. Законы Фарадея
Таблица А.1 – Константы ионизации некоторых кислот и оснований
 – затраты ее на разрыв химических связей между атомами в решетке металла (Ереш);
– затраты ее на разрыв химических связей между атомами в решетке металла (Ереш);– расход энергии на ионизацию атомов с превращением их в катионы (характеризуется потенциалом ионизации, I);
– выделение энергии при связывании катионов металла с молекулами воды (энергия гидратации, Егидр.).
Чем меньше энергия металлической решетки и потенциал ионизации атомов металла и чем больше энергия гидратации (сольватации) катионов металла, тем более энергетически выгодным будет переход ионов металла в раствор, тем большим по абсолютной величине будет электродный потенциал. Если учесть, что на величину потенциала влияют также пространственное распределение ионов металла в растворе, изменение структуры растворителя и т. д., то станет ясно, что рассчитать абсолютную величину электродного потенциала не представляется возможным.
С другой стороны, экспериментальное определение абсолютной величины электродного потенциала также невозможно вследствие того, что хотя двойной электрический слой и представляет собой своеобразный «конденсатор», подключить к нему измерительную систему не удастся, т.к. одна из «обкладок» такого конденсатора – это катионы металла в растворе.
Вследствие изложенных выше причин остается только один вариант – определять не абсолютную, а относительную величину электродного потенциала или разность электродных потенциалов двух систем (полуэлементов), соединенных электрической цепью.
На приведенном ниже рисунке 12.1 показан вариант такой системы, включающей цинковый и медный полуэлементы.
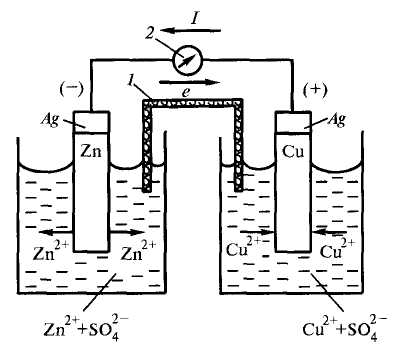 Рисунок 12.1 – Схема медно-цинкового гальванического элемента | Такие системы называют гальваническими элементами, в которых полуэлементы соединены внутренней цепью – электролитическим мостиком (1) и внешней цепью (2). Внешняя цепь выполняет функцию транспортировки электронов с электрода, поляризованного более отрицательно (его называют анодом) на электрод, поляризованный менее отрицательно (его называют катодом). Внутренняя цепь служит для транспортировки ионов (анионов) электролита в направлении, обратном движению электронов. |
Вследствие того, что металлический цинк окисляется легче, чем медь, его потенциал – более отрицательный, чем для меди. В таком случае цинк «поляризован анодно», а медь «поляризована катодно». Следовательно, на рисунке 12.1 цинковый электрод – это анод, а медный – катод.
Условия, необходимые для работы гальванического элемента
Если в схеме, приведенной выше, единственным электролитом является вода, то такой гальванический элемент работать не будет и разность электродных потенциалов измерить не удастся. Для работы гальванического элемента необходимо выполнение следующих условий:
– металлы полуэлементов должны быть погружены в растворы их солей;
– металлы полуэлементов должны иметь электрический контакт друг с другом (соединяться внешней цепью);
– должен быть электрический контакт растворов полуэлементов для обеспечения противотока ионов (наличие внутренней цепи).
При обеспечении этих условий элемент будет работать до выравнивания потенциалов полуэлементов.
Разность электродных потенциалов двух полуэлементов, например, цинкового и медного (Ер) – это разность потенциалов катодного и анодного процессов:
Eр = Екатода – Е анода = Е
Ер называют электродвижущей силой (ЭДС) гальванического элемента.
Вследствие того, что на практике используют не абсолютные, а относительные величины потенциалов, возникла необходимость определять их относительно одной и той же системы сравнения. В качестве электрода (полуэлемента) сравнения был выбран «водородный электрод». Устройство этого электрода показано на рисунке 12.2.
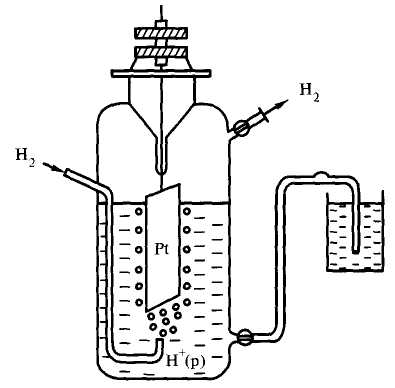
Рисунок 12.2 – Схема водородного электрода
Основной элемент водородного электрода – это платиновая пластина, покрытая платиновой чернью и погруженная в раствор серной или хлорной кислоты.
При пропускании через раствор молекулярного водорода он сорбируется на платиновом электроде, при этом активная платиновая чернь способствует его атомизации. В результате между водородом на пластине и в растворе устанавливается равновесие H+ + e H(г) и возникает скачок потенциала Е
Факторы, влияющие на величину электродного потенциала; уравнение Нернста; стандартный электродный потенциал
Стандартный электродный потенциал (Е0) окислительно-восстановительной системы – это потенциал, измеренный в стандартных условиях: при T = 298 K и молярности (активности) веществ, участвующих в превращении, равной 1 моль/л. Электродный потенциал измеряется в Вольтах (В).
Для водородного электрода стандартный потенциал условно приняли за «ноль».
Если условия нестандартные, то величину электродного потенциала рассчитывают по уравнению Нернста. Уравнение Нернста показывает зависимость электродного потенциала от природы веществ, участвующих в равновесии (через Е0), их концентрации и температуры
Е = Е0 +
 , (12.1)
, (12.1)где R – универсальная газовая постоянная (8,31 Дж/моль·К);
T – температура в градусах Кельвина;
F – число Фарадея (заряд электронов количеством 1 моль, 96500 Кл/моль);
n – число электронов, участвующих в элементарной реакции;
С(Ox) и С(Red) – молярные концентрации окисленной (oxidation) и восстановленной (redaction) форм веществ, составляющий полуэлемент;
x, y– соответствующие им стехиометрические коэффициенты в уравнении реакции.
При подстановке в уравнение (12.1) Т = 298 К, F = 96500 Кл/моль, R = 8,31 Дж/моль·К и замене ln lg для гомогенной окислительно-восстановительной системы
х Ox + ne y Red
получим следующее уравнение:
| Е = Е0 +  | (12.2) |
Если в равновесии участвуют газообразные вещества, то молярные их концентрации можно заменить на парциальные давления. Твердые вещества (например, металлы) в уравнение Нернста не включают.
Величина электродного потенциала – это количественная характеристика окислительно-восстановительных свойств веществ:
Чем больше алгебраическая величина электродного потенциала, тем большими окислительными свойствами обладает окисленная форма и тем меньшими восстановительными – восстановленная форма вещества.
Уравнение Нернста для водородного электрода

При нормальном давлении (p = 1 атм) это уравнение преобразуется в следующее:
Учитывая, что стандартный потенциал водородного электрода
приняли равным нулю, а также то, что –lgC(H+) = pH, получим зависимость водородного электрода от pH
| | (12.3) |
При pH = 7:
Уравнение Нернста для металлического электрода
На границе металл/раствор его солиустанавливается равновесие
Men+(раствор) + ne Me(электрод), для которого уравнение Нернста в общем виде, с учетом, что система гетерогенная, записывают следующим образом:
| | (12.4) |
При подстановке в это уравнение Т = 298 К, F = 96500 Кл/моль и замене натурального логарифма на десятичный получим следующее уравнение:
Электрохимический ряд металлов
В соответствии с увеличением окислительных свойств катионов металлов (окисленная форма) и уменьшением восстановительных свойств металлов – простых веществ (восстановленная форма) построен известный электрохимический ряд металлов:
Li K Na Mg Al Ti Mn Zn Fe Pb H Bi Cu Ag Pt Au
В электрохимическом ряду левее водорода расположены металлы, стандартные электродные потенциалы которых отрицательнее, чем у водородного электрода; правее водорода расположены металлы, стандартные электродные потенциалы которых положительные.
Для того, чтобы экспериментально определить стандартный электродный потенциал какого-нибудь металла, например цинка, необходимо в стандартных условиях собрать гальванический элемент, в котором один электрод будет металлическим (цинковым), а другой – водородным, и измерить разность потенциалов такого элемента, Е0:
Zn ZnCl2 HCl H2 (Pt)
Для цинка стандартный электродный потенциал отрицательнее водородного на 0,77 В, т. е.