Файл: 1. Элементарлы талдау а талданатын заттаы жеке компоненттерді анытайтын сапалы жне санды талдау дістері.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 03.12.2023
Просмотров: 1479
Скачиваний: 1
СОДЕРЖАНИЕ
С) 10-3 - 10-6 г; 10-1 - 10-4 мл
С) 10-3 - 10-6 г; 10-1 - 10-4 мл
*С) 10-3 - 10-6 г; 10-1 - 10-4 мл
С) 10-3 - 10-6 г; 10-1 - 10-4 мл
С) 10-3 - 10-6 г; 10-1 - 10-4 мл
С) 10-3 - 10-6 г; 10-1 - 10-4 мл
С) 10-3 - 10-6 г; 10-1 - 10-4 мл
A) Сұйылтылған азот қышқылымен.
A) Сұйылтылған хлорсутек қышқылы.
A) Калийдің гексанитрокупраты(II).
B) Қорғасынның гексанитрокупраты(II).
C) Натрийдің гексанитрокупраты(II).
*D) Калий және қорғасынның гексанитрокупраты(II).
*A) Қаныққан натрий карбонаты ерітіндісімен өңдеу
A) Концентрлі аммиак ерітіндісі.
B) Қаныққан натрий карбонаты ерітіндісі.
A) Концентрлі аммиак ерітіндісі.
C) Ерігіштік максимум мәнге жетеді.
D) Ерігіштік минимум мәнге жетеді.
C) Ерігіштік максимум мәнге жетеді.
D) Ерігіштік минимум мәнге жетеді.
201. АmBn жүйесі үшін тұнбаның түзілу жағдайы ( ):
A) КS мәні температураға тәуелді емес.
B) Температура жоғарылаған сайын Кsмәні артады.
222. Комплекстүзу реакциясы арқылы ерітіндіге нашар өтетін тұнба:
*A) Оствальдтың сұйылту заңына.
*A) Оствальдтың сұйылту заңына.
D) Тұнбаға түсіру кезіндегі ортаның рН мәнімен.
А) Массаларының қатынасы 1:10.
В) Көлемдерінің қатынасы 1:10.
*Е) Эквивалент мөлшерлерінің қатынасы 1:1.
*C) Индикатормен де, индикаторсыз да.
*A) Жұтылу спектрі - жұтылған жарықтың толқын ұзындығы.
A) Электромагнитті сәулеленудің табиғатын білу үшін.
*A) Жұмысшы электроды потенциалы – титрант көлемі.
*A) Жартылай толқын потенциалдардың айырымын арттыру үшін
B) Оптикалық жұтылу мен жұтылу қабатындағы толқын ұзындығыарасындағы сызықтық байланыс.
C) Оптикалық жұтылу мен жарық жұтылуындағы толқын ұзындығы арасындағы сызықтық байланыс.
D) Молярлық жұтылу мен толқын ұзындығы арасындағы сызықтық байланыс.
A) Тұрақты ток күшіндегі кулонометрия.
*A) Ток күшінің уақытқа көбейтіндісі.
B) Кернеудің уақытқа көбейтіндісі.
1. Элементарлық талдау:
*А) Талданатын заттағы жеке компоненттерді анықтайтын сапалық және сандық талдау әдістері.
В) Талданатын заттағы функционалдық топтарды анықтайтын сапалық және сандық талдау әдістері.
С) Талданатын заттағы молекулалық массасы тұрақты жеке химиялық қосылыстарды анықтайтын сапалық және сандық талдау әдістері.
D) Бір-бірімен бөлу бетімен шектелген және қасиеттерімен, физикалық құрылысымен ажыратылатын көп компонентті қоспадағы жеке компоненттердің химиялық табиғатын анықтайтын әдістер тобы.
E) Сандық талдауда қолданылатын барлық әдістердің жинақталған тобы.
2. Молекулярлық талдау:
А) Талданатын заттағы жеке компоненттерді анықтайтын сапалық талдау әдісі.
В) Талданатын заттағы функционалдық топтарды анықтайтын сапалық талдау әдісі.
*С) Талданатын заттағы молекулалық массасы тұрақты жеке химиялық қосылыстарды анықтайтын сапалық және сандық талдау әдістері.
D) Бір-бірімен бөлу бетімен шектелген және қасиеттерімен, физикалық құрылысымен ажыратылатын көп компонентті қоспадағы жеке компоненттердің химиялық табиғатын анықтайтын әдістер тобы.
E) Сандық талдауда қолданылатын барлық әдістердің жинақталған тобы.
3. Функционалдық талдау:
А) Талданатын заттағы жеке компоненттерді анықтайтын сапалық және сандық талдау әдістері.
*В) Талданатын заттағы функционалдық топтарды анықтайтын сапалық және сандық талдау әдістері.
С) Талданатын заттағы молекулалық массасы тұрақты жеке химиялық қосылыстарды анықтайтын сапалық және сандық талдау әдістері.
D) Бір-бірімен бөлу бетімен шектелген және қасиеттерімен, физикалық құрылысымен ажыратылатын көп компонентті қоспадағы жеке компоненттердің химиялық табиғатын анықтайтын әдістер тобы.
E) Сандық талдауда қолданылатын барлық әдістердің жинақталған тобы.
4. Фазалық талдау:
А) Талданатын заттағы жеке компоненттерді анықтайтын сапалық және сандық талдау әдістері.
В) Талданатын заттағы функционалдық топтарды анықтайтын сапалық және сандық талдау әдістері.
С) Талданатын заттағы молекулалық массасы тұрақты жеке химиялық қосылыстарды анықтайтын сапалық және сандық талдау әдістері.
*D) Бір-бірімен бөлу бетімен шектелген және қасиеттерімен, физикалық құрылысымен ажыратылатын көп компонентті қоспадағы жеке компоненттердің химиялық табиғатын анықтайтын әдістер тобы.
E) Сандық талдауда қолданылатын барлық әдістердің жинақталған тобы.
5. Химиялық талдаудағы заттың аналитикалық қасиетіне тән емес:
А) Иісі.
В) Түсі.
*С) ИҚ- спектрде жұтылу жолағының болуы.
D) Жалын түсінің боялуы.
E) Кристалдардың пішіні мен түсі.
6. Жартылай микроталдау әдісі:
А) Грамм - әдісі, зерттелетін заттың мөлшері 1 - 10 г.
*В) Сантиграмм - әдісі, зерттелетін заттың мөлшері 0,05 - 0,5 г.
С) Миллиграмм - әдісі, зерттелетін заттың мөлшері 10-3 - 10-6 г.
D) Микрограмм - әдісі, зерттелетін заттың мөлшері 10-6 - 10-9 г.
Е) Нанограмм - әдісі, зерттелетін заттың мөлшері 10-9 - 10-12 г.
7. Макроталдауда қолданылатын заттың массасы мен көлемі:
*А) 1 - 10 г; 10 - 100 мл
В) 0,05 - 0,5 г; 1 - 10 мл
С) 10-3 - 10-6 г; 10-1 - 10-4 мл
D) 10-6 - 10-9 г; 10-4 - 10-6 мл
E) 10-9 - 10-12 г; 10-7 - 10-10 мл
8. Микроталдауда қолданылатын заттың массасы мен көлемі:
А) 1 - 10 г; 10 - 100 мл
В) 0,05 - 0,5 г; 1 - 10 мл
*С) 10-3 - 10-6 г; 10-1 - 10-4 мл
D) 10-6 - 10-9 г; 10-4 - 10-6 мл
E) 10-9 - 10-12 г; 10-7 - 10-10 мл
9. Жартылай микроталдауда қолданылатын заттың массасы мен көлемі:
А) 1 - 10 г; 10 - 100 мл
*В) 0,05 - 0,5 г; 1 - 10 мл
С) 10-3 - 10-6 г; 10-1 - 10-4 мл
D) 10-6 - 10-9 г; 10-4 - 10-6 мл
E) 10-9 - 10-12 г; 10-7 - 10-10 мл
10. Грамм - әдісінде қолданылатын заттың массасы мен көлемі:
*А) 1 - 10 г; 10 - 100 мл
В) 0,05 - 0,5 г; 1 - 10 мл
С) 10-3 - 10-6 г; 10-1 - 10-4 мл
D) 10-6 - 10-9 г; 10-4 - 10-6 мл
E) 10-9 - 10-12 г; 10-7 - 10-10 мл
11. Ультрамикроталдауда қолданылатын заттың массасы мен көлемі:
А) 1 - 10 г; 10 - 100 мл
В) 0,05 - 0,5 г; 1 - 10 мл
С) 10-3 - 10-6 г; 10-1 - 10-4 мл
*D) 10-6 - 10-9 г; 10-4 - 10-6 мл
E) 10-9 - 10-12 г; 10-7 - 10-10 мл
12. Миллиграмм - әдісінде қолданылатын заттың массасы мен көлемі:
А) 1 - 10 г; 10 - 100 мл
В) 0,05 - 0,5 г; 1 - 10 мл
*С) 10-3 - 10-6 г; 10-1 - 10-4 мл
D) 10-6 - 10-9 г; 10-4 - 10-6 мл
E) 10-9 - 10-12 г; 10-7 - 10-10 мл
13. Нанограмм-әдісінде қолданылатын заттың массасы мен көлемі:
А) 1 - 10 г; 10 - 100 мл
В) 0,05 - 0,5 г; 1 - 10 мл
С) 10-3 - 10-6 г; 10-1 - 10-4 мл
D) 10-6 - 10-9 г; 10-4 - 10-6 мл
*E) 10-9 - 10-12 г; 10-7 - 10-10 мл
14. Микрограмм - әдісінде қолданылатын заттың массасы мен көлемі:
А) 1 - 10 г; 10 - 100 мл
В) 0,05 - 0,5 г; 1 - 10 мл
С) 10-3 - 10-6 г; 10-1 - 10-4 мл
*D) 10-6 - 10-9 г; 10-4 - 10-6 мл
E) 10-9 - 10-12 г; 10-7 - 10-10 мл
15. Сантиграмм - әдісінде қолданылатын заттың массасы мен көлемі:
А) 1 - 10 г; 10 - 100 мл
*В) 0,05 - 0,5 г; 1 - 10 мл
С) 10-3 - 10-6 г; 10-1 - 10-4 мл
D) 10-6 - 10-9 г; 10-4 - 10-6 мл
E) 10-9 - 10-12 г; 10-7 - 10-10 мл
16. Субмикроталдауда қолданылатын заттың массасы мен көлемі:
А) 1 - 10 г; 10 - 100 мл
В) 0,05 - 0,5 г; 1 - 10 мл
С) 10-3 - 10-6 г; 10-1 - 10-4 мл
D) 10-6 - 10-9 г; 10-4 - 10-6 мл
*E) 10-9 - 10-12 г; 10-7 - 10-10 мл
17. Бір ионды басқа иондардың қатысында анықтауға болатын аналитикалық реакция:
A) Селективті.
*B) Спецификалық.
C) Талғамды.
D) Топ реагентінің әсері.
E) Бөлу реакциясы.
18. Зерттелетін иондарды топқа бөліп, топты құрайтын иондарды белгілі бір ретпен анықтауға негізделген талдау:
A) Бөлшектік.
*B) Жүйелік.
C) Топ реагентінің әсері.
D) Бөлу реакциясы.
E) Тұнбаға толық түскенін тексеру әдісі.
19. Зерттелетін ерітіндінің бір бөлігінен, басқа иондардың қатысында спецификалық реакцияның көмегімен бір ионды анықтауға негізделген талдау:
*A) Бөлшектік.
B) Жүйелік.
C) Топ реагентінің әсері.
D) Бөлу реакциясы.
E) Тұнбаға толық түскенін тексеру әдісі.
20. Спецификалық реактив:
*A) Басқа иондардың қатысында бір ғана ионмен реакцияға түседі.
B) Зерттелетін заттардың өзіне тән қасиеттерімен ерекшеленетін жаңа қосылыстарға айналуына көмектеседі.
C) Түрлі топтарға жататын жекеленген иондардың шектеулі санымен әрекеттеседі.
D) Топтың барлық иондармен әрекеттеседі.
E) Спецификалық реактивтер болмайды
21. Селективті реактив:
A) Басқа иондардың қатысында бір ғана ионмен реакцияға түседі.
B) Зерттелетін заттардың өзіне тән қасиеттерімен ерекшеленетін жаңа қосылыстарға айналуына көмектеседі.
*C) Түрлі топтарға жататын жекеленген иондардың шектеулі санымен әрекеттеседі.
D) Топтың барлық иондармен әрекеттеседі.
E) Селективті реактивтер болмайды.
22. “Бөлшектік” талдау кезінде қолданылатын реакция:
А) Каталитикалық.
В) Гомогенді.
С) Гетерогенді.
D) Селективті.
*Е) Спецификалық.
23. “Сулы” жолмен жүргізілетін талдау:
А) Элементарлық.
В) Молекулярлық.
*С) Иондық.
D) Фазалық.
E) Құрылыстық.
24. Жүйелік талдауда топтарға бөлу үшін қолданылады:
А) Спецификалық реакция.
В) Селективті реагент.
*С) Топтық реагент.
D) Гомогенді реакция.
Е) Гетерогенді реакция.
25. Анықтауға болатын заттың немесе ионның ең аз мөлшері:
-
Реакцияның сезімталдылығы. -
Реакцияның спецификалығы. -
*Ашу шегі. -
Шекті сұйылту. -
Минималды концентрация.
26. Ерітіндідегі ионның ашу шегін есептейтін формула:
А) 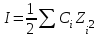
В)
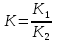
С)
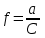
D)
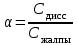
*Е)
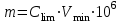
27. Ашу шегінің өлшем бірлігі:
A) моль/л
B) моль
C) тонна
*D) мкг
E) кг
28. Көлемі 0,02 мл ерітіндідегі алюминий ионының ашу шегі 1,2 мкг болатын ерітіндідегі Al3+ ионының шекті концентрациясы мен эквивалентінің молярлық концентрациясы:
A) *6,0·10-5; 6,7·10-3
B) 1,0·10-5; 2,0·10-4
C) 6,6·10-5; 0,1
D) 1,0·10-5; 0,5
E) 6,6·10-5; 2,0·10-4
29. Шекті концентрациясы 1,2·10-3 г/мл тең болатын К+ ионын анықтауға қажет KCl ерітіндісінің минималды концентрациясы CM (моль/л):
A) 3·10-1
B) 2,3·10-1
*C) 3·10-2
D) 1,6·10-5
E) 1,6·10-1
30. Шекті сұйылтылған 1:10000 ерітіндінің 0,1 мл көлеміндегі реакцияның ашу шегі:
A) 10-5 г
B) *10-6 г
C) 105 мкг
D) 106 мкг
E) 10-4 г
31. 1 гAg+ионын 25000 г еріткіштен анықтауға болатын реакцияның шекті сұйылту мәні:
-
0,02 мл -
4·10-5 г -
0,8 мкг -
25000:1 -
* 1:25000
32. Аналитикалық реакцияның сезгіштігі сипатталады:
A) Ерігіштік көбейтіндісімен – Ks.
B) Молярлық ерігіштікпен – S.
*C) Ашу шегімен – m.
D) Заттың массалық концентрациясымен - Cm.
E) Заттың массалық үлесімен – w.
33. Аналитикалық реакцияның сезгіштігі жоғары болады, егер:
А) Аз мөлшерде шекті сұйылту болғанда.
*B) Ашу шегі аз болғанда.
C) Ерітіндінің үлкен концентрациясында.
D) Ерітіндінің рН < 0 болғанда.
E) Ерітіндінің рН > 0 болғанда.
34. Катиондарды топқа бөлудегі аналитикалық жіктеу олардың электрондық конфигурациясымен тығыз байланыстылығын көрсететін шама:
А)
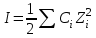
В)
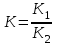
*С)
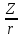
D)

Е)
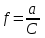
35. Қышқылдық-негіздік жіктелу бойынша Ag+,
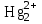 , Pb2+ иондары:
, Pb2+ иондары: *A) II топ
B) IV топ
C) IIIтоп
D) Vтоп
E) VI топ
36. Қышқылдық-негіздік жіктелу бойынша Mn2+, Mg2+, Bi3+, Fe2+, Fe3+, Sb3+, Sb5+ иондары:
A) II топ
B) IV топ
C) IIIтоп
*D) Vтоп
E) VI топ
37. Қышқылдық-негіздік жіктелу бойынша Ni2+, Hg2+, Co2+, Cd2+, Cu2+ иондары:
A) II топ
B) IV топ
C) IIIтоп
D) Vтоп
*E) VI топ
38. Қышқылдық-негіздік жіктелу бойынша Ba2+, Ca2+, Sr2+ иондары:
A) II топ
B) IV топ
*C) IIIтоп
D) Vтоп
E) VI топ
39. Күкіртсутекті жіктелу бойынша Ba2+, Sr2+, Ca2+ катиондар тобының топ реагенті:
A) HCl
B) H2SO4
C) Na2HPO4
D) Na2SO4
*E) (NH4)2CO3
40. VI аналитикалық топ катиондарын V аналитикалық топ катиондарынан бөлу үшін ерітіндіге қосылатын реагент:
A) HCl
B) H2SO4
C) NaOH
D) NaOH + H2O2
*E) NH4OH
41.Тұнбалары концентрлі аммиактың әсерінен ерітіндіге көшетін аналитикалық топ:
A) 2
*B) 6
C) 3
D) 5
E) 1
42. NaOH ерітіндісін қосқан кезде түзілген тұнбалар реактивтің артық мөлшерінен еріп ерітіндіге өтсе, зерттелетін ерітіндіде болуы мүмкін:
-
2 топ катиондары. -
3 топ катиондары. -
*4 топ катиондары. -
5 топ катиондары. -
6 топ катиондары.
43. NH4OHерітіндісін қосқан кезде түзілген тұнбалар реактивтің артық мөлшерінен еріп ерітіндіге өтсе, зерттелетін ерітіндіде болуы мүмкін:
-
2 топ катиондары. -
3 топ катиондары. -
1топ катиондары. -
5 топ катиондары. -
*6 топ катиондары.
44. Топ реактиві жоқ анион:
А)
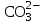
В)