Файл: 1. Элементарлы талдау а талданатын заттаы жеке компоненттерді анытайтын сапалы жне санды талдау дістері.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 03.12.2023
Просмотров: 1474
Скачиваний: 1
СОДЕРЖАНИЕ
С) 10-3 - 10-6 г; 10-1 - 10-4 мл
С) 10-3 - 10-6 г; 10-1 - 10-4 мл
*С) 10-3 - 10-6 г; 10-1 - 10-4 мл
С) 10-3 - 10-6 г; 10-1 - 10-4 мл
С) 10-3 - 10-6 г; 10-1 - 10-4 мл
С) 10-3 - 10-6 г; 10-1 - 10-4 мл
С) 10-3 - 10-6 г; 10-1 - 10-4 мл
A) Сұйылтылған азот қышқылымен.
A) Сұйылтылған хлорсутек қышқылы.
A) Калийдің гексанитрокупраты(II).
B) Қорғасынның гексанитрокупраты(II).
C) Натрийдің гексанитрокупраты(II).
*D) Калий және қорғасынның гексанитрокупраты(II).
*A) Қаныққан натрий карбонаты ерітіндісімен өңдеу
A) Концентрлі аммиак ерітіндісі.
B) Қаныққан натрий карбонаты ерітіндісі.
A) Концентрлі аммиак ерітіндісі.
C) Ерігіштік максимум мәнге жетеді.
D) Ерігіштік минимум мәнге жетеді.
C) Ерігіштік максимум мәнге жетеді.
D) Ерігіштік минимум мәнге жетеді.
201. АmBn жүйесі үшін тұнбаның түзілу жағдайы ( ):
A) КS мәні температураға тәуелді емес.
B) Температура жоғарылаған сайын Кsмәні артады.
222. Комплекстүзу реакциясы арқылы ерітіндіге нашар өтетін тұнба:
*A) Оствальдтың сұйылту заңына.
*A) Оствальдтың сұйылту заңына.
D) Тұнбаға түсіру кезіндегі ортаның рН мәнімен.
А) Массаларының қатынасы 1:10.
В) Көлемдерінің қатынасы 1:10.
*Е) Эквивалент мөлшерлерінің қатынасы 1:1.
*C) Индикатормен де, индикаторсыз да.
*A) Жұтылу спектрі - жұтылған жарықтың толқын ұзындығы.
A) Электромагнитті сәулеленудің табиғатын білу үшін.
*A) Жұмысшы электроды потенциалы – титрант көлемі.
*A) Жартылай толқын потенциалдардың айырымын арттыру үшін
B) Оптикалық жұтылу мен жұтылу қабатындағы толқын ұзындығыарасындағы сызықтық байланыс.
C) Оптикалық жұтылу мен жарық жұтылуындағы толқын ұзындығы арасындағы сызықтық байланыс.
D) Молярлық жұтылу мен толқын ұзындығы арасындағы сызықтық байланыс.
A) Тұрақты ток күшіндегі кулонометрия.
*A) Ток күшінің уақытқа көбейтіндісі.
B) Кернеудің уақытқа көбейтіндісі.
А) 1·10-14
В) 1·10-7
С) 7
*D) 14
Е) 1·10+14
255. Сутектік көрсеткіш:
A) Ерітіндінің жалпы концентрациясы.
B) Гидроксил ионы концентрациясының теріс таңбамен алынған ондық логарифмі.
*C) Сутегі ионы концентрациясының теріс таңбамен алынған ондық логарифмі.
D) Сутегі ионы концентрациясының теріс таңбамен алынған натурал логарифмі.
E) Қышқыл молекуласының диссоциацияланбаған “артық” қоры.
256. Сілті ерітінділерінің рН мәнін есептейтін формула:
A)
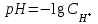
B)
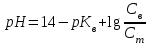
C)
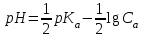
D)
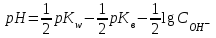
*E)
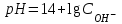
257. Концентрациясы 0,01 моль/л NaOH ерітіндісінің рН:
-
2 -
5 -
7 -
9 -
*12
258. 0,01 н HCl ерітіндісінің рОН:
-
2 -
5 -
7 -
9 -
*12
259. Ерітінді рН=3 болған кездегі
 иондарының концентрациясы:
иондарының концентрациясы: -
3 -
*10-3 -
3·10-3 -
11 -
10-9
260. Ерітінді рН=6 болған кездегі
 иондарының концентрациясы:
иондарының концентрациясы:-
8 -
10-4 -
6 -
*10-8 -
10-10
261. Концентрациясы 10-3 моль/л NaOH ерітіндісінің рН:
A) 2
B) 5
C) 7
D) 9
*E) 11
262. Концентрациясы 0,01 моль/л КОН ерітіндісінің рН:
A) 10-2
B) 10-12
C) 2
*D) 12
E) 1
263. 10-3 н HCl ерітіндісінің рOН:
A) 2
B) 5
C) 7
D) 9
*E) 11
264. 0,001М азот қышқылы ерітіндісі үшін рН-тың теңдеуі:
A) ln10-3
B) -ln10-3
C) 10-3
*D) -lg10-3
E) -ln103
265. Эквивалентінің молярлық концентрациясы 0,1 моль/л кальций гидроксиді ерітіндісі үшін рН-тың теңдеуі:
A) 14- ln10-1
B) 14- lg10-1
C) 14 + ln10-1
*D) 14 + lg10-1
E) 10-14
266. Сутектік көрсеткіші 5 тең, ерітіндінің сутегі ионының концентрациясы
 :
:A) 10-1
B) 10-3
*C) 10-5
D) 10-7
E) 10-9
267. Сутектік көрсеткіші 4 тең, ерітіндінің гидроксил ионының концентрациясы
 :
:A) 10-2
B) 10-4
C) 10-6
D) 10-8
*E) 10-10
268. Сутегі ионының концентрациясы [H+] = 4,5·10-9 моль/л ерітіндідегі гидроксил ионының концентрациясы
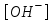 :
:A) 2,2·10-4
B) 2,2·10-5
*C) 2,2·10-6
D) 2,2·10-7
E) 2,2·10-8
269. Эквивалентінің молярлық концентрациясы 0,01 моль/л күкірт қышқылы ерітіндісінің pH:
А) 1
*В) 2
С) 3
D) 4
Е) 5
270. Гидроксилдік көрсеткішті pOH анықтайтын формула:
А)
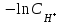
*В)
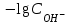
С)
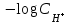
D)
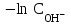
Е)
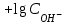
271.
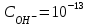 болғанда, ерітінді ортасы:
болғанда, ерітінді ортасы:А) Сілтілік.
В) Әлсіз сілтілік.
С) Бейтарап.
D) Әлсіз қышқылдық.
*Е) Күшті қышқылдық.
272. HCl ерітіндісін 100 есе сумен сұйылтқанда рН мәні:
-
2 есе артады. -
*2-ге артады. -
Өзгермейді. -
2 есе кемиді. -
2-ге кемиді.
273.[H+]=4,5·10-9моль/л, OH- ионының концентрациясы:
A) 2,2·10-4
B) 2,2·10-5
C) *2,2·10-6
D) 2,2·10-7
E) 2,2·10-8
274. 0,01 моль/л HClO қышқылы ерітіндісінің рН (Ка = 10-8):
A) 4
B) 3
C) 7
D) 6
E) *5
275. CH
A) HCl
B) NaCl
C) NaOH
D) KNO3
E) *H3PO4
276. KOH ерітіндісін 100 есе сумен сұйылтқанда рН мәні:
-
2 есе артады. -
2-ге артады. -
Өзгермейді. -
*2-ге кемиді. -
2 есе кемиді.
277. Концентрациясы 10-5моль/л HClерітіндісіне 1 л0,001 моль NaOH ерітіндісін қосқан кезде ерітіндінің рН мәні :
-
*6-ғаартады. -
3-кеартады. -
Өзгермейді. -
2-гекемиді. -
5-кекемиді.
278. Концентрациясы 10-5моль/л HClерітіндісіне 1 л0,001 моль HCl ерітіндісін қосқан кезде ерітіндінің рН мәні:
-
6-ғаартады. -
3-кеартады. -
Өзгермейді. -
*2-гекемиді. -
5-кекемиді.
279. Күшті электролиттер арасындағы бейтараптану реакциясын сипаттайтын теңдеу:
A) NH3 + H2O ↔ NH4+ + OH-
B) H2O+ H2O ↔ H3O+ + OH-
C) NH3 + CH3COOH ↔ NH4+ + CH3COO-
D) CH3COOH + H2O ↔ CH3COO-+ H3O+
E) *H3O+ + OH- ↔ 2H2O
280. Әлсіз электролиттер арасындағы бейтараптану реакциясын сипаттайтын теңдеу:
A) NH3 + H2O ↔ NH4+ + OH-
B) H2O+ H2O ↔ H3O+ + OH-
C) *NH3 + CH3COOH ↔ NH4+ + CH3COO-
D) CH3COOH + CH3COOH ↔ CH3COO- + CH3COOH2+
E) HCl + NaOH ↔ NaCl + H2O
281. Қышқыл күшінің көрсеткіші:
А) pH
В) pKW
*С) pKa
D) pKв
Е)
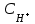
282. Күшті қышқыл:
А) K(CH3COOH) = 1,74·10-5
В) K1(H2CO3) = 4,5·10-7
С) K2(H2CO3) = 4,8·10-11
*D) K(HNO2) = 5,1·10-4
Е) K(H3AsO3) = 5,1·10-10
283.
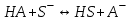 реакциясы үшін қышқылдың шынайы константасы:
реакциясы үшін қышқылдың шынайы константасы:A)
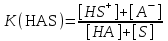
B)
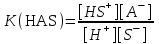
*C)
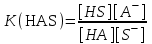
D)
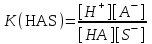
E)
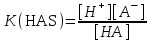
284.
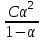 сәйкес келеді:
сәйкес келеді:*A) Оствальдтың сұйылту заңына.
B) Аррениус теңдеуіне.
C) Нернст теңдеуіне.
D) Илькович теңдеуіне.
E) Вант-Гофф теңдеуіне.
285.
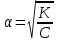 сәйкес келеді:
сәйкес келеді:*A) Оствальдтың сұйылту заңына.
B) Аррениус теңдеуіне.
C) Нернст теңдеуіне.
D) Илькович теңдеуіне.
E) Вант-Гофф теңдеуіне.
286. Оствальдтың сұйылту заңына сәйкес келетін теңдеу:
*A)
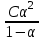
B)
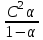
C)
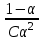
D)
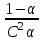
E)
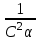
287. Диссоциациялану дәрежесінің мәндерін салыстыра қарағанда ең күшті қышқыл:
А) *α = 1
B) α = 0,87
C) α = 0,5
D) α = 0,3
E) α = 0,013
288. Диссоциациялану константасының мәндерін салыстыра қарағанда ең күшті қышқыл:
-
K(HNO2)= 5,1 . 10-4 -
K(HBrO)= 2,5 . 10-9 -
*K(HІO3)= 1,6 . 10-1 -
K(HІO)= 2,3 . 10-11 -
K(HF)= 6,8 . 10-4
289. Диссоциациялану константасының мәндерін салыстыра қарағанда ең әлсіз қышқыл:
-
K(HNO2) = 5,1 . 10-4 -
K(HBrO) = 2,5 . 10-9 -
K(HІO3)= 1,6 . 10-1 -
*K(HІO)= 2,3 . 10-11 -
K(HF)= 6,8 . 10-4
290. Диссоциациялану константасының мәндерін салыстыра қарағанда ең күшті негіз:
-
Аммоний гидроксиді;Kв= 1,76 . 10-5 -
Гидразин;Kв= 9,8 . 10-7 -
Гидроксиламин; Kв= 9,6 . 10-9 -
Дифениламин; Kв= 7,1 . 10-14 -
*Күміс гидроксиді;Kв= 5,0 . 10-3
291. Диссоциациялану константасының мәндерін салыстыра қарағанда ең әлсіз негіз:
-
Аммоний гидроксиді;Kв= 1,76 . 10-5 -
Гидразин;Kв= 9,8 . 10-7 -
Гидроксиламин; Kв= 9,6 . 10-9 -
*Дифениламин; Kв= 7,1 . 10-14 -
Күміс гидроксиді;Kв= 5,0 . 10-3
292. 0,1 н NH4OHерітіндісіндегі
 иондарының концентрациясы (K(NH4OH) = 10-5):
иондарының концентрациясы (K(NH4OH) = 10-5):-
10-1 -
10-2 -
*10-3 -
10-4 -
10-5
293. K(NH4OH) = 10-5
тең, 0,1 н NH4OHерітіндісінің диссоциациялану дәрежесі:
-
10-1 -
*10-2 -
10-3 -
10-4 -
10-5
294. K(CH3COOH) = 10-5тең, 0,1 н CH3COOH ерітіндісінің рН:
-
1 -
2 -
*3 -
4 -
5
295. K(CH3COOH) = 10-5тең, 0,1 н CH3COOHерітіндісінің диссоциациялану дәрежесі:
-
10-1 -
* 10-2 -
10-3 -
10-4 -
10-5
296. Иондану дәрежесі 4,2 %, концентрациясы 0,01 М аммиак ерітіндісінің тепе-теңдік концентрациясы:
A) 4,2·10-1моль/л
B) 4,2·10-2моль/л
C) 4,2·10-3моль/л
*D) 4,2·10-4моль/л
E) 4,2·10-5моль/л
297. 0,01 М әлсіз бірқышқылды негіз ерітіндісінің рН = 10. Негіздің диссоциациялану константасы:
A) 1·10-20
B) 1·10-18
C) 1·10-10
D) 1·10-8
*E) 1·10-6
298. 0,1 М әлсіз бірнегізді қышқыл ерітіндісіндегі сутегі ионының концентрациясы 10-5 моль/л. Қышқылдың диссоциациялану константасы:
A) 1·10-1
B) 1·10-5
C) 1·10-6
D) 1·10-10
*E) 1·10-9
299. K(NH4OH) = 10-5 тең, 0,001 н NH4OH ерітіндісінің рОН:
A) 1
B) 2
C) 3
*D) 4
E) 5
300. K(CH3COOH) = 10-5 тең, 0,001 н CH3COOH ерітіндісінің рН:
A) 1
B) 2
C) 3
*D) 4
E) 5
301. Эквивалентінің молярлық концентрациясы 0,1 моль/л, α = 0,01 тең болатын сірке қышқылы ерітіндісінің рН:
A) 1
B) 0,5
*C) 3
D) 2
E) 2,5
302. Әлсіз қышқыл ерітінділеріндегі сутегі ионының концентрациясы:
A)
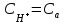
*B)
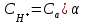
C)
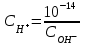
D)
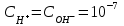
E)
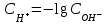
303. Әлсіз қышқылдар үшін сутек иондарының концентрациясын есептейтін формула:
А)
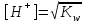
В)
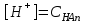
*С)
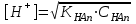
D)
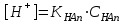
Е)
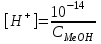
304. Әлсіз қышқыл ерітінділерінің рН мәнін есептейтін формула:
A)

B)
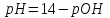
C)

*D)

E)

305. Әлсіз негіздердің рН мәнін есептейтін формула:
*A)
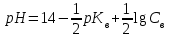
B)

C)

D)

E)

306. Әлсіз негіз MeOH сипаттайтын теңдеу:
A)
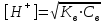
B)
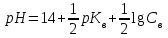
C)
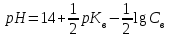
D)
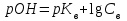
*E)
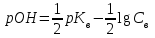
307. HNO2 ерітіндісінің сутегі ионы концентрациясын есептейтін теңдеу (К(HNO2) = 5,1·10-4):
A)
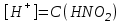
*B)

C)
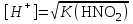
D)
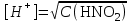
E)
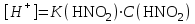
308. NH4OH ерітіндісінің сутегі ионы концентрациясын есептейтін теңдеу (К(NH4OH) = 1,8·10-5):
*A)
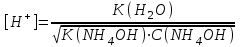
B)
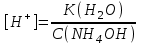
C)
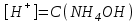
D)
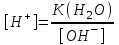
E)
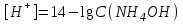
309. Эквивалентінің молярлық концентрациясы 0,006 моль/л, Ка = 1,8·10-4 тең болатын құмырсқа қышқылы ерітіндісінің рН:
A) 1,15
B) 2,20
C) 6,50
D) 4,50
*E) 3,00
310. Эквивалентінің молярлық концентрациясы 0,03 моль/л, Ка