Файл: 1. Элементарлы талдау а талданатын заттаы жеке компоненттерді анытайтын сапалы жне санды талдау дістері.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 03.12.2023
Просмотров: 1489
Скачиваний: 1
СОДЕРЖАНИЕ
С) 10-3 - 10-6 г; 10-1 - 10-4 мл
С) 10-3 - 10-6 г; 10-1 - 10-4 мл
*С) 10-3 - 10-6 г; 10-1 - 10-4 мл
С) 10-3 - 10-6 г; 10-1 - 10-4 мл
С) 10-3 - 10-6 г; 10-1 - 10-4 мл
С) 10-3 - 10-6 г; 10-1 - 10-4 мл
С) 10-3 - 10-6 г; 10-1 - 10-4 мл
A) Сұйылтылған азот қышқылымен.
A) Сұйылтылған хлорсутек қышқылы.
A) Калийдің гексанитрокупраты(II).
B) Қорғасынның гексанитрокупраты(II).
C) Натрийдің гексанитрокупраты(II).
*D) Калий және қорғасынның гексанитрокупраты(II).
*A) Қаныққан натрий карбонаты ерітіндісімен өңдеу
A) Концентрлі аммиак ерітіндісі.
B) Қаныққан натрий карбонаты ерітіндісі.
A) Концентрлі аммиак ерітіндісі.
C) Ерігіштік максимум мәнге жетеді.
D) Ерігіштік минимум мәнге жетеді.
C) Ерігіштік максимум мәнге жетеді.
D) Ерігіштік минимум мәнге жетеді.
201. АmBn жүйесі үшін тұнбаның түзілу жағдайы ( ):
A) КS мәні температураға тәуелді емес.
B) Температура жоғарылаған сайын Кsмәні артады.
222. Комплекстүзу реакциясы арқылы ерітіндіге нашар өтетін тұнба:
*A) Оствальдтың сұйылту заңына.
*A) Оствальдтың сұйылту заңына.
D) Тұнбаға түсіру кезіндегі ортаның рН мәнімен.
А) Массаларының қатынасы 1:10.
В) Көлемдерінің қатынасы 1:10.
*Е) Эквивалент мөлшерлерінің қатынасы 1:1.
*C) Индикатормен де, индикаторсыз да.
*A) Жұтылу спектрі - жұтылған жарықтың толқын ұзындығы.
A) Электромагнитті сәулеленудің табиғатын білу үшін.
*A) Жұмысшы электроды потенциалы – титрант көлемі.
*A) Жартылай толқын потенциалдардың айырымын арттыру үшін
B) Оптикалық жұтылу мен жұтылу қабатындағы толқын ұзындығыарасындағы сызықтық байланыс.
C) Оптикалық жұтылу мен жарық жұтылуындағы толқын ұзындығы арасындағы сызықтық байланыс.
D) Молярлық жұтылу мен толқын ұзындығы арасындағы сызықтық байланыс.
A) Тұрақты ток күшіндегі кулонометрия.
*A) Ток күшінің уақытқа көбейтіндісі.
B) Кернеудің уақытқа көбейтіндісі.
A) KCN
*B) K4[Fe(CN)6]
C) K3[Fe(CN)6]
D) CH3COONa
E) NH4OH
103.
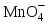 ионын түссіздендіреді:
ионын түссіздендіреді:A) Силикат ионы.
*B) Оксалат ионы.
C) Нитрат ионы.
D) Фосфат ионы.
E) Карбонат ионы.
104. Гидролиз сапалық реакциясы болып табылатын катион:
A) Магний.
*B) Сурьма(III).
C) Марганец.
D) Темір(III).
E) Темір(II).
105. Хром(ІІІ) ионын анықтауға спецификалық реакция:
A) Хром(ІІІ) гидроксидінің түзілуі.
B) Хромиттің түзілуі.
C) Фосфаттың түзілуі.
*D) Сілтілік ортада бром суымен реакциясы.
E) Натрий гидрофосфатымен реакциясы.
106. Гидроксиді амфотерлік қасиет көрсетпейтін катион:
A) Қалайы(II, IV).
B) Хром(III).
*C) Магний(II).
D) Мырыш.
E) Сурьма(ІІІ, V).
107. Cu2+ ионын анықтауға спецификалық реакция:
A) Мыс(ІІ) гидроксидінің түзілуі.
B) Мыс(ІІ) негіздік карбонатының түзілуі.
C) Мыс фосфатының түзілуі.
*D) Мыс гексацианоферраты(ІІ) түзілуі.
E) Мыстың металдармен ығыстырылуы.
108. Марганец(IV) гидроксиді тұнбасының түсі:
A) Ақ.
B) Көк.
C) Алқызыл.
*D) Күрең-қызыл.
E) Сұр-жасыл.
109. Сынап(ІІ) ионын анықтауға спецификалықреакция:
A) Сынап(II) сульфидінің түзілуі.
B) Сынап(II) фосфатының түзілуі.
*C) Қалайы(II) тұзымен тотығу-тотықсыздану реакциясы.
D) Сынап хроматының түзілуі.
E) Тетраамминсынап(II) комплексті ионының түзілуі.
110. Алюминий ионын анықтайтын реактив:
A) α-нитрозо-β-нафтол.
B) Диметилглиоксим.
C) Купрон.
D) Дитизон.
*E) Ализарин.
111. Кобальтионын анықтайтын реактив:
*A) α-нитрозо-β-нафтол.
B) Диметилглиоксим.
C) Купрон.
D) Дитизон.
E) Ализарин.
112. Гидроксиді амфотерлік қасиет көрсететін катион:
A) Темір(II).
B) Темір(III).
C) Марганец(II).
*D) Сурьма(III).
E) Кадмий(ІІ).
113.
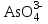 ионымен нашар еритін қосылыс түзетін реактив:
ионымен нашар еритін қосылыс түзетін реактив:A) Сұйылтылған хлорсутек қышқылы.
B) Диметилглиоксим.
*C) Аммоний молибдаты HNO3 қатысында.
D) Натрий гидрофосфаты аммоний тұздары мен аммиак қатысында.
E) Калийдің гексацианоферраты(II).
114. Күміс хроматы тұнбасының түсі:
A) Жасыл.
B) Күлгін.
C) Сары.
D) Алқызыл.
*E) Қызыл-қоңыр.
115. Ca(NO3)2 және Ba(NO3)2 қоспаларын бөледі:
A) Сұйылтылған азот қышқылымен.
B) Сұйылтылған хлорсутек қышқылымен.
C) Аммоний оксалатымен.
D) Натрий карбонатымен.
*E) Калий дихроматымен.
116. BaSO4, CaSO4, SrSO4, PbSO4 сульфаттарын концентрлі аммоний ацетаты ерітіндісімен өңдегенде ерітіндіге көшетін ион:
A) Ba2+
B) Sr2+
C) Ca2+
*D) Pb2+
E) Ba2+, Pb2+
117. Қорғасын сульфатымен суда жақсы еритін қосылыс түзеді:
A) Сұйылтылған хлорсутек қышқылы.
*B) Концентрлі аммоний ацетаты ерітіндісі.
C) Артық мөлшердегі калий иодиді.
D) Концентрлі аммиак ерітіндісі.
E) Сұйылтылған күкірт қышқылы.
118. Барий ионына спецификалық реакция:
A) Барий сульфатының түзілуі.
B) Барий карбонатының түзілуі.
*C) Барий хроматының түзілуі.
D) Жалынның боялуы.
E) Барий оксалатының түзілуі.
119. Калий-натрий гексанитрокобальтаты(III) тұнбасының түзілуіне қажетті жағдай:
A) Қыздыру.
*B) Бейтарап орта.
C) Күшті қышқылды орта.
D) Әлсіз қышқылды орта.
E) Сілтілік орта.
120. BiJ3 тұнбасының түсі:
A) Сары.
*B) Қара.
C) Қызыл.
D) Ақ.
E) Алқызыл.
121. Калий ионына тән микрокристаллоскопиялық реакция нәтижесінде түзілетін қосылыс:
A) Калийдің гексанитрокупраты(II).
B) Қорғасынның гексанитрокупраты(II).
C) Натрийдің гексанитрокупраты(II).
*D) Калий және қорғасынның гексанитрокупраты(II).
E) Натрий және қорғасынның гексанитрокупраты(II).
122. Hg2+ ионын Hg22+ және Hg0 дейін тотықсыздандыратын қосылыс:
A) Sn(OH)2
B) [SnCl6]4-
C) Sn0
D) *SnCl2
E) [SnCl4]2-
123. Mn2+ ионы(NH4)2S әрекетекенде түзіледі:
A) MnO(OH)2
B) MnO4-
C)* MnS
D) Mn(OH)2
E) MnSO4
124. K2Pb[Cu(NO2)6] тұнбасының түсі:
A) Сары.
*B) Қара.
C) Қызыл.
D) Ақ.
E) Алқызыл.
125. III топ катиондары сульфаттарын карбонаттарға айналдыру үшін қажетті жағдай:
*A) Қаныққан натрий карбонаты ерітіндісімен өңдеу
B) Қыздыру.
C) Араластыру.
D) Салқындату.
E) Натрий ацетатын қосу.
126. Стронций ұшқыш тұздарынан жалын түсі боялады:
A) Сарыға.
B) Сары-жасылға.
*C) Ашық қызылға.
D) Көгілдірке.
E) Жасылға.
127. Кальций ионын K4[Fe(CN)6] реактивімен анықтау үшін қажетті жағдай:
A) Суыту.
B) Араластыру.
C) Аммоний ацетатын қосу.
*D) Аммоний хлоридін қосу.
E) Қыздыру.
128. Ca(NH4)2[Fe(CN)6] комплексті қосылысының түсі:
A) Қызыл.
*B) Ақ.
C) Сары.
D) Қара.
E) Жасыл.
129. Сынап иодидімен суда жақсы еритін қосылыс түзетін реагент:
A) Концентрлі аммиак ерітіндісі.
B) Қаныққан натрий карбонаты ерітіндісі.
*C) Артық мөлшердегі калий иодиді.
D) Сұйылтылған хлорсутек қышқылы.
E) Сұйылтылған күкірт қышқылы.
130. Жүйелік талдауда стронций ионын кальций ионы қатысында анықтауға болатын реактив:
A) Калий хроматы.
*B) Гипс суы.
C) Натрий карбонаты.
D) Сұйылтылған күкірт қышқылы.
E) Аммоний оксалаты.
131. Мышьяк(V) ионын мышьяк(ІІІ) ионынан бөлу үшін қолданылатын реактив:
A) AgNO3
B) NH4OH
C) HCl + H2S
D) * MgCl2 + NH4OH + NH4Cl
E) KJ
132. AgCl тұнбасынНg2Cl2тұнбасынанбөугеқолданылатынреагент:
A) KCl, K2CO3
B) HNO3 конц.
C) *NH4ОН конц.
D) HCl конц.
E) Na2S2O3
133. Сынап(ІІ) ионын ерітіндіден мыс(ІІ) ионы қатысында ашуға болатын реагент:
A) H2SO4
B) HCl
C) *SnCl2
D) Na2S2O3
E) Na2S
134. Висмут ионы қатысында қорғасын ионын анықтауға болатын реагент:
A) NH4OH
B) (NH4)2CO3
C) Na2S2O3
D) Na2HPO4
E) *H2SO4
135. Ag2S тұнбасы еритін реактив:
A) HCl
B) Na2S
C) NaOH
D) *KCN
E) H2SO4
136. Каломель тұнбасын ерітетін қосылыс:
A) Концентрлі аммиак ерітіндісі.
B) Концентрлі аммоний ацетаты ерітіндісі.
*C) Патша сұйығы.
D) Сұйылтылған сірке қышқылы.
E) Сұйылтылған күкірт қышқылы.
137. Стронций ионын анықтайтын реактив:
A) Na3[Co(NO2)6]
*B) H2SO4сұй.
C) HCl сұй.
D) K3[Sb(OH)6]
E) Na2Pb[Cu(NO2)6]
138. Күміс иодиді тұнбасының түсі:
*A) Сары.
B) Ақ.
C) Қызғылт-сары.
D) Қара.
E) Жасыл.
139. Жүйелік талдауда күміс ионын анықтау үшін спецификалық реакция:
A) Күміс фосфатының түзілуі.
B) Күміс тиосульфатының түзілуі.
*C) Күміс хлоридінің түзілуі.
D) Күміс оксидінің түзілуі.
E) Күміс сульфатының түзілуі.
140. Барий карбонаты тұнбасын ерітетін қосылыс:
A) Аммоний гидроксиді.
B) Натрий гидроксиді.
C) Аммоний ацетаты.
D) Аммоний хлориді.
*E) Сірке қышқылы.
141. Қорғасын ионын анықтайтын спецификалық реакция:
A) NaOH
B) SnCl2
*C) KJ
D) Na3[Co(NO2)6]
E) СН3СООН
142. Жүйелік талдауда гидролиз реакциясын қолдану арқылы анықталатын иондар тобы:
A) Fe2+, Fe3+
B) Cr3+, Mn2+
*C) Sb3+, Bi3+
D) Ni2+, Co2+
E) As3+, As5+
143. Қорғасын мен барий сульфаттарын бөлу үшін қолданылатын реактив:
-
HCl -
NH4Cl -
*CH3COONH4 -
NH4OH -
NaOH
144. Sr2+- ионын Ca2+- ионынан бөлу үшін қолданылатын реактив:
А) H2SO4
В) NH3
С) NaOH
*D) (NH4)2SO4
Е) CH3COONH4
145. Қышқылдық-негіздік жіктелу бойынша Zn2+ ионын
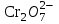 ,
, 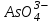 иондарынан бөлу үшін қолданылатын реагент:
иондарынан бөлу үшін қолданылатын реагент:A) NH4OHконц.
B) NaOH
C) H2SO4
*D) Na2CO3
E) HNO3 сұй., t0
146. Cu2S, HgS тұнбаларын VІ аналитикалық топтың басқа катиондарынан бөлу үшін ерітіндіге қосады:
A) (NH4)2S
B) H2S
C) *H2SO4 + Na2S2O3
D) Na2S2O3
E) (NH4)2S2
147. CH3COO-, CO32-, SO42-, S2O32-, PO43- иондар қоспасынан сульфат ионын жеке бөліп алуға қолданады:
A) Барий тұзын.
B) Стронций тұзын.
C) *Барий тұзымен тұндырып, содан соң HCl өңдеу арқылы.
D) Қышқылдық ортада мырышпен SO2 тотықсыздандыруды.
E) Кальций тұзымен.
148. Zn2+, Sn2+, Cd2+ иондары тұздарының ерітіндісіне KOH артық мөлшерін қосқанда түзілетін тұнба:
A) Zn(OH)2, Sn(OH)2, Cd(OH)2
B) Sn(OH)2, Cd(OH)2
C) Sn(OH)2
D) *Cd(OH)2
E) Тұнба түзілмейді.
149. Al3+, Zn2+, Cu2+ иондары тұздарының ерітіндісіне аммиак ерітіндісінің артық мөлшерін қосқан кезде түзілетін тұнба: