Файл: 1. Элементарлы талдау а талданатын заттаы жеке компоненттерді анытайтын сапалы жне санды талдау дістері.docx
ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 03.12.2023
Просмотров: 1523
Скачиваний: 1
СОДЕРЖАНИЕ
С) 10-3 - 10-6 г; 10-1 - 10-4 мл
С) 10-3 - 10-6 г; 10-1 - 10-4 мл
*С) 10-3 - 10-6 г; 10-1 - 10-4 мл
С) 10-3 - 10-6 г; 10-1 - 10-4 мл
С) 10-3 - 10-6 г; 10-1 - 10-4 мл
С) 10-3 - 10-6 г; 10-1 - 10-4 мл
С) 10-3 - 10-6 г; 10-1 - 10-4 мл
A) Сұйылтылған азот қышқылымен.
A) Сұйылтылған хлорсутек қышқылы.
A) Калийдің гексанитрокупраты(II).
B) Қорғасынның гексанитрокупраты(II).
C) Натрийдің гексанитрокупраты(II).
*D) Калий және қорғасынның гексанитрокупраты(II).
*A) Қаныққан натрий карбонаты ерітіндісімен өңдеу
A) Концентрлі аммиак ерітіндісі.
B) Қаныққан натрий карбонаты ерітіндісі.
A) Концентрлі аммиак ерітіндісі.
C) Ерігіштік максимум мәнге жетеді.
D) Ерігіштік минимум мәнге жетеді.
C) Ерігіштік максимум мәнге жетеді.
D) Ерігіштік минимум мәнге жетеді.
201. АmBn жүйесі үшін тұнбаның түзілу жағдайы ( ):
A) КS мәні температураға тәуелді емес.
B) Температура жоғарылаған сайын Кsмәні артады.
222. Комплекстүзу реакциясы арқылы ерітіндіге нашар өтетін тұнба:
*A) Оствальдтың сұйылту заңына.
*A) Оствальдтың сұйылту заңына.
D) Тұнбаға түсіру кезіндегі ортаның рН мәнімен.
А) Массаларының қатынасы 1:10.
В) Көлемдерінің қатынасы 1:10.
*Е) Эквивалент мөлшерлерінің қатынасы 1:1.
*C) Индикатормен де, индикаторсыз да.
*A) Жұтылу спектрі - жұтылған жарықтың толқын ұзындығы.
A) Электромагнитті сәулеленудің табиғатын білу үшін.
*A) Жұмысшы электроды потенциалы – титрант көлемі.
*A) Жартылай толқын потенциалдардың айырымын арттыру үшін
B) Оптикалық жұтылу мен жұтылу қабатындағы толқын ұзындығыарасындағы сызықтық байланыс.
C) Оптикалық жұтылу мен жарық жұтылуындағы толқын ұзындығы арасындағы сызықтық байланыс.
D) Молярлық жұтылу мен толқын ұзындығы арасындағы сызықтық байланыс.
A) Тұрақты ток күшіндегі кулонометрия.
*A) Ток күшінің уақытқа көбейтіндісі.
B) Кернеудің уақытқа көбейтіндісі.
А) Оттегінің бір атомына.
В) Сутегінің бір ионына.
С) Оттегінің бір молекулалық массасына.
*D) Бір электронға.
Е) Оттегінің бір молекуласына.
479. Калий перманганатының қышқылдық ортадағы эквивалентінің молярлық массасы (E°(MnO4-/Mn2+) = 1,52 B; M(KMnO4) = 158 г/моль):
А) 158 г/моль
*В) 31,6 г/моль
С) 1,58 г/моль
D) 52,6 г/моль
Е) 5,26 г/моль
480. Сілтілік ортада
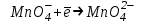 жүретін жартылай реакциядағы калий перманганатының эквивалентінің молярлық массасы (M(KMnO4) = 158 г/моль):
жүретін жартылай реакциядағы калий перманганатының эквивалентінің молярлық массасы (M(KMnO4) = 158 г/моль):*А) 158 г/моль
В) 15,8 г/моль
С) 31,6 г/моль
D) 3,16 г/моль
Е) 52,6 г/моль
481. Перманганатометриялық титрлеуде қолданылатын индикатор:
А) Тұндыру.
В) Адсорбциялық.
С) Металлохромдық.
*D) Индикаторсыз.
Е) Қышқылдық-негіздік.
482. Иодометрия әдісіндегі титрант:
А) NaCl
В) (NH4)2C2O4
С) KMnO4
*D) Na2S2O3·5H2OЕ) Na2SO3
483. Перманганатометриялық титрлеу әдісімен Fe (II) ионын анықтауда қолданылатын Циммерман-Рейнгард қоспасы:
А) MnSO4, NaCl, H2SO4
В) MnSO4, H2SO4, CaCl2
*С) MnSO4, H3PO4, H2SO4
D) MnSO4, H2SO4, ZnCl2
Е) MnSO4, H3PO4, HCl
484. 2S2O32- + J3- → S4O62-+ 3J- жартылай реакциясындағы натрий тиосульфатының эквивалентінің молярлық массасы (M(Na2S2O3·5H2O) = 248,19 г/моль):
А) 124,09 г/моль
*В) 248,19 г/моль
С) 24,82 г/моль
D) 12,409 г/моль
Е) 24,82 г/моль
485.
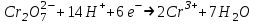 жартылай редокс реакциясындағы калий дихроматының эквивалентінің молярлық массасы (M(K
жартылай редокс реакциясындағы калий дихроматының эквивалентінің молярлық массасы (M(K
2Cr2O7) = 294,22 г/моль):
А) 38,09 г/моль
В) 294,22 г/моль
*С) 49,03 г/моль
D) 29,42 г/моль
Е) 98,06 г/моль
486. Эквивалентінің молярлық концентрациясы 0,02 моль/л 100 мл ерітінді дайындауға қажет калий дихроматының массасы (M(K2Cr2O7) = 294,22 г/моль):
А) 98,06 г
В) 9,806 г
С) 0,9806 г
*D) 0,09806 г
Е) 0,009806 г
487. Натрий тиосульфаты ерітіндісін калий бихроматы ерітіндісі бойынша тура титрлеу арқылы стандартауға болмайды, себебі:
A) Реакция баяу жүреді.
B) Эквиваленттік нүктені анықтау мүмкін емес.
C) K2Cr2O7 дәл массасын өлшеу мүмкін емес.
*D) Реакцияның бір теңдеумен өрнектелуі мүмкін емес.
E) Реакция қайтымды.
488. Титриметриялық талдауда қолданылатын иод ерітіндісін даярлау тәсілі:
A) Калий иодиді мен әктас қоспасын айдау арқылы тазаланған иод ерітіндісінің дәл сынамасын қолдану.
B) Сатып алынған иод ерітіндісінің дәл сынамасын қолдану.
C) Йодты суда еріту.
*D) Йодты калий иодидінде еріту.
E) Йодты сұйылтылған спиртте еріту.
489. Иодометриялық титрлеуде қолданылатын индикатор:
A) Метил қызыл-сарысы.
B) Фенолфталеин.
C) Әмбебап индикаторы.
*D) Крахмал.
E) Калий хроматы.
490. Жартылай реакциядағы
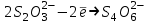 натрий тиосульфатының эквивалентінің молярлық массасы (М(Na2S2O3·5H2O) = 248,19 г/моль):
натрий тиосульфатының эквивалентінің молярлық массасы (М(Na2S2O3·5H2O) = 248,19 г/моль):A) 49,04
B) 31,61
*C) 248,19
D) 127,11
E) 63,04
491. Иодометрия әдісінде қолданылатын титрант:
A) Натрий хлориді.
B) Аммоний оксалаты.
C) Калий перманганаты.
*D) Натрий тиосульфаты.
E) Натрий сульфиті.
492. Салицил қышқылын анықтайтын әдіс:
A) Йодометриялық.
*B) Броматометриялық.
C) Перманганатометриялық.
D) Цериметриялық.
E) Ванадатометриялық.
493. Fe(II) ионын калий бихроматымен титрлеу кезінде эквиваленттік нүктені анықтау үшін қолданылатын индикатор (Е0(Fe3+/Fe2+) = 0,77 B; Е0(Cr2O72-, 14H+/2Cr3+) = 1,33 B):
A) Дифениламин (Е0 = +0,76 B).
*B) Фенилантронил қышқылы (Е0 = +0,88 B).
C) Дифениламиназосульфон қышқылы (Е0 = +0,04 B).
D) Бейтарап қызыл (Е0 = +0,24 B).
E) Метил көгі (Е0 = +0,53 B).
494. Бихроматометриялық әдіспен анықтайды:
А) Mg2+
В) Cr3+
С) Cl-
*D) Fe2+
Е) MnO4-
495. Тұндыру әдісінде эквиваленттік нүкте анықталады:
A) Негізбен.
B) Тұнба түзілумен.
C) *Индикаторсыз да, индикатормен де.
D) Буфермен.
E) Қышқылмен.
496. Титрлеу секірмесінің ауданы жоғары болатын тұнба:
*A) Ks(AgJ) = 8,3·10-17
B) Ks(AgBr) = 5,3·10-13
C) Ks(AgCl) = 1,78·10-10
D) Ks(AgJO3) = 3,0·10-8
E) Ks(Ag2CrO4) = 1,1·10-12
497. Мор әдісі бойынша анықталатын иондар тобы:
*A) Cl-, Br-, CN-
B) Cl-, CN-, I-
C) CN-, Br-, SCN-
D) I-, SCN-, CN-
E) S-, I-, SCN-
498. Фольгард әдісінің титранты:
A) NaCl
B) AgNO3
*C) KSCN
D) J2
E) Na2S2O3
499. Меркурометриялық титрлеуде қолданылатын реакция:
*A)
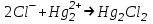
B)
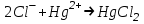
C)
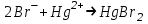
D)
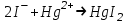
E)
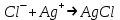
500. Фольгард әдісінің индикаторы:
A) (NH4)2Fe(SO4)2·6H2O
*B) NH4Fe(SO4)2·12H2O
C) FeSO4
D) K4[Fe(CN)6]
E) Fe2O3
501. Тұндыру титрлеу әдісінде эквиваленттік нүкте анықталады:
A) Индикатормен.
B) Индикаторсыз.
*C) Индикатормен де, индикаторсыз да.
D) Крахмалмен.
E) Метил қызыл-сарысы қолданылады.
502. Тұндыру титрлеу әдісіндегі титрант:
А) NaOH
В) HNO3
*С) AgNO3
D) Ca(NO3)2
Е) NH4NO3
503. Мор әдісінің индикаторы:
А) Флуоресцеин.
*В) Калий хроматы.
С) Темір (ІІІ) тұзы.
D) Метил қызыл-сарысы.
Е) Индикаторсыз титрленеді.
504. Аргентометриялық титрлеу әдісімен хлорид ионын анықтауға болмайды, егер ерітіндіде:
А) Na+ ионы болса.
В) K+ ионы болса.
С)  ионы болса.
ионы болса.
D) CH3COO- ионы болса. *Е)
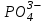 ионы болса.
ионы болса.505. Тұндыру титрлеу әдісінде қолданылатын темір (ІІІ) ионы индикаторы:
*А) Металлохромды.
В) Редокс.
С) Адсорбциялық.
D) Тұндыру.
Е) Қышқылдық-негіздік.
506. Флюоресцеин индикаторы:
А) Қышқылдық-негіздік.
В) Редокс.
С) Тұндыру.
D) Металлохромды.
*Е) Адсорбциялық.
507. Комплексон - І формуласы:
A)
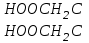 >
>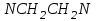 <
<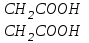
B)
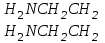 >
>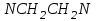 <
<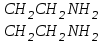
C)
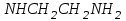
D)
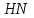 <
<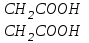
*E)
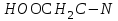 <
<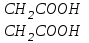
508. Комплексон - ІІІ ерітіндісін стандарттайтын бастапқы зат:
A) Na2CO3
B) K2Cr2O7
C) J2
*D) MgSO4·7H2O
E) CaSO4
509. Металлохромды индикатор:
*A) Мурексид.
B) Метил қызыл-сарысы.
C) Фенолфталеин.
D) Дифениламин.
E) Әмбебап индикаторы.
510. Комплексонометриялық титрлеу әдісімен магнийді эриохром-қара индикаторы қатысында анықтағанда ерітінді түсінің ауысуы:
*A) Шарап қызылдан - көкке.
B) Қарадан - көкке.
C) Сары қызылдан – күлгінге.
D) Шарап қызылдан – қараға.