ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 04.12.2023
Просмотров: 127
Скачиваний: 3
ВНИМАНИЕ! Если данный файл нарушает Ваши авторские права, то обязательно сообщите нам.
Распад нуклеотидов в тканях и ЖКТ
Любая животная или растительная пища включает нуклеопротеиды (см. Приложение, таблица 2); продукты, попадая в ротовую полость, подвергаются механической переработке, в желудке сложные белки начинает разрушать соляная кислота (схема). Ее подобное свойство обусловлено тем, что изначально образование данных протеинов связано с особенностями строения входящих в их состав компонентов. Нуклеотиды за счет наличия в них фосфатов являются анионами, а в белках преобладают основные аминокислоты (лизин, арг) - что обеспечивает их щелочной характер (поликатионы). Объединение этих структур и происходит с помощью ионных связей. Соляная кислота, являясь сильным электролитом, легко их разрывает, и отделившиеся друг от друга вышеназванные соединения в других отделах ЖКТ подвергаются действию различных ферментов.
Полипептиды разрушаются с помощью протеаз (см выше), а cреди гидролаз, ответственных за распад нуклеотидов, можно выделить следующие их варианты: а) рибо- и дезоксирибонуклеазы - в зависимости от того, что служит субстратом: РНК или ДНК; б) экзо - и эндонуклеазы, разрушающие фосфодиэфирные связи у концов или в середине молекулы (схема).
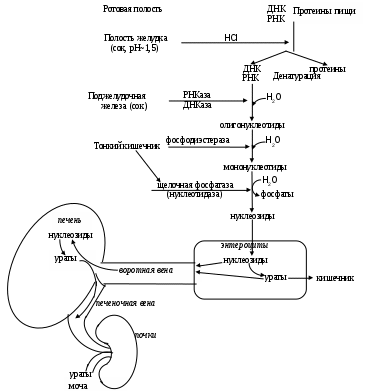
Схема катаболизма полинуклеотидов пищи
Последовательное уменьшение длины молекулы полинуклеотида приводит к образованию мононуклеотида, который подвергается дефосфорилированию под действием щелочной фосфатазы. Продукт данной реакции - нуклеозид - легко всасывается, попадая в энтероцит, часть подобных гликозидов, в первую очередь, включающих пуриновые основания, преобразуются (дезаминируются, гидроксилируются) в мочевую кислоту. Соли последней - ураты экскретируются в просвет тонкого кишечника. Основная доля усвоившихся нуклеозидов по системе воротной вены попадает в печень. В гепатоцитах они разрушаются до конечных продуктов (пурины до уратов, пиримидины до мочевины, воды, СО2).
Схема гидролиза тканевых нуклеопротеидов во многом сходна с вышеописанными реакциями. Отличается только механизмом дефосфолирования. В клетках рН не имеет такого основного характера, как в полости тонкого кишечника, поэтому это действие производит не щелочная фосфатаза (она в этих условиях не активна), а 5’ - нуклеотидаза. Заканчивается разрушение эндогенных нуклеозидов в печени.
Специфические пути преобразования нуклеотидов
Конденсированные ароматические азотные основания (пурины: аденин, гуанин) вследствие наличия солидного обобществленного пи-электроного облака (сопряженности) очень прочны, в клетках отсутствуют ферменты, способные разрушить их неполярные связи. В отличие от них кольца пиримидинов распадаются за счет повреждения сопряженности путем гидрирования одной из связей.
Конечный продукт модификации пуринов - мочевая кислота
Как замечено выше, распада циклов пуринов не происходит. Просто, чтобы обеспечить их выведение из организма природа стремится увеличить их растворимость в воде, вводя в молекулу полярные гидроксильные группировки. (Рис.). Начальные стадии изменений аденозина и гуанозина несколько отличаются друг от друга из-за низкой растворимости первого, рост данного свойства обеспечивается заменой аминогруппы более полярной гидроксильной (реакция гидролитического дезаминирования) и только после этого с помощью нуклеозидфосфорилазы рвется нуклеозидная связь. Образующийся гипоксантин с участием ксантин-ДГ дважды гидроксилируется. Активность данного фермента усиливается в присутствии катионов Мо2+. Конечным продуктом данного процесса и служит мочевая кислота. Одна из ее гидроксильных групп способна к диссоциации, что и придает ей кислые свойства.
Гуанин за счет наличия двух полярных группировок (-ОН, -NН2) лучше растворяется в воде, поэтому его нуклеотид вначале подвергается фосфоролизу под влиянием нуклеозидфосфорилазы, а только потом гидролитическому дезаминированию. Результатом чего является ксантин, преобразования которого также заканчиваются мочевой кислотой.
Из гепатоцитов ее соли попадают в общий кровоток, доставляется в почки, и выводятся в составе мочи; а часть их вновь реабсорбируется.
В норме содержания уратов в плазме крови не превышает 0,5 ммоль/л, причем у мужчин регистрируются более высокие цифры, чем у женщин.
Схема разрушений пиримидиновых колец
Распад разных пиримидиновых нуклеотидов протекает по сходной схеме (рис. 3.3.2.1.2.) одним из важнейших превращений, в которой служит гидрирование ароматического кольца, что повреждает целостность Пи-электронного облака и поэтому снижает его прочность. Первой реакцией цитидина является гидролитическое дезаминирование, как и в случае с аденином. В результате получается
уридин, который реже подвергается фосфоролизу под действием нуклеозидфосфорилазы. Освободившийся пиримидин - урацил, используя восстановленный НАД и дигидроурацил-ДГ, становится дигидроурацилом. Из-за нарушения ароматичности он довольно легко гидролизуется с разрывом кольца (работает соответствующая гидролаза дигидропиримидиназа). Продукт реакции обычно считают производным пропионовой кислоты, β – углеродный атом которой связан с остатком мочевины (β–уреидпропионат). Дальнейшие гидролитические преобразования совершаются отделением аммиака и углекислого газа, которые после определенных модификаций (в соли аммония, глутамин и гидрокарбонаты) используются в синтезе мочевины. Из углеродного скелета получается β-аланин. Часть его молекулы включается в дипептиды - карнозин, ансерин - важные АО, а также в динуклеотид - HSKоА. Другая половина переаминируется, итогом этого процесса служит формилацетат, который, вступая в реакции, сходные с окислительным декарбоксилированием α-кетокислот, становится ацетилКоА, судьба которого завершается в ЦТК.
Тимидин является гомологом дезоксиуридина, поэтому этапы его распада фактически повторяют вышеописанные реакции, только метаболиты отличаются на гомологическую разницу (СН2-). Вместо β-уреидпропионата образуется β-аминоизобутират, из которого после переаминирования и окислительного декарбоксилирования получается метилмалонил-КоА. Это соединение под влиянием метилмалонил-КоА-мутазы изомеризуется в сукцинил-КоА, который легко вступает в ЦТК, в клетках эритроидного ряда и гепатоцитах большая часть его молекул используется в синтезе гема.
Пути синтеза мононуклеотидов
В настоящее время считают, что азотистые основания мононуклеотидов имеют эндогенное происхождение, а их пищевые аналоги разрушаются в энтеро- и гепатоцитах. Что касается пентоз, то они могут оказаться в общем кровотоке после всасывания из кишечника, затем, подвергнувшись облегчённой диффузии фосфорилироваться в клетке, как гексозы и глицерин:
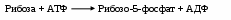
Подобный фосфорный эфир рибозы является также метаболитом ПФП. Однако, чтобы ее первый атом сумел образовать N–гликозидную связь с пурином или пиримидином, необходимо его активировать:
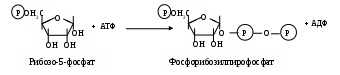
Ароматические гетероциклы для своего синтеза используют аминокислоты (глн, асп, а пурин - еще и глицин), но сам процесс их генеза отличается тем, что пиримидины вначале образуется в свободном виде и только потом взаимодействует с фосфорибозилпирофосфатом, а пуриновые основания строят свои циклы, связывая отдельные атомы с активной рибозой.
Синтез пуриновых нуклеотидов
На рисунке. показано, какие соединения участвуют в синтезе пуриновых нуклеотидов, родоначальником которых является инозин-монофосфат (ИМФ): источниками атомов азота служат аспарагин, две молекулы глутамина, а глицин используется полностью. С помощью тетрагидрофолиевой кислоты, которая способна принимать от одних соединений С1-фрагменты и передавать их другим, появляются в кольцах два атома углерода; также гидрокарбонат включается в образование пуринового кольца.
Сам процесс синтеза многостадийный, в нем участвует 10 ферментов, используются четыре молекулы АТФ. Синтез начинается с того, что ФРПФ под влиянием амидинферазы взаимодействует с глутамином, при этом происходит еще и конверсия (α-пентоза преобразуется в β-форму, получившейся 5–фосфорибозиламин реагирует с глицином и продолжается до тех пор, пока не возникает ИМФ, из которого путем переаминирования не образуются АМФ и ГМФ.
Подобный путь синтеза получил название – denovo (заново). Но клетки некоторых тканей (эмбриональных, регенирирующих, опухолевых) способны использовать азотистые основания или гликозиды, высвободившиеся при распаде полинуклеотидов, для включения их в новые нуклеиновые структуры (путь спасения). Ключевыми ферментами этого процесса являются гипоксантингуанин - фосфорибозилтрансфераза (ГГФРТ), аденинфосфорибозилтрансфераза.
Образование пиримидиновых колец
Как отмечено выше, для пиримидинов характерны их гены в свободном виде, точнее синтезируется оротовая кислота, которая позднее взаимодействует с ФРПФ. В этом процессе участвуют атомы аспартата, глутамина и гидрокарбонат. Первая реакция протекает также, как начало синтеза мочевины с образованием карбамоилфосфата (рис.) с затратой энергии двух молекул АТФ. На второй стадии при участии аспартаткарбамоилтрансферазы получается карбамоиласпартат, затем происходит замыкание кольца с высвобождением молекулы воды (т.е. реакция, обратная гидролизу, при действии того же фермента
дигидропиримидиназы). Ее продукт - дигидрооротовая кислота (дигидрооротат) подвергается дегидрированию, что обеспечивает возникновение сопряженной системы в цикле. Интересная деталь: восстановленный НАД+ при благоприятных условиях может запустить ЭТЦ, и окислительное фосфорилирование, что закончится образованием 3 АТФ (итог - самообеспечение энергией синтеза пиримидинов). Возникший оротат взаимодействует с ФРПФ, что фактически завершает процесс генеза, остается лишь произвести декарбоксилирование оротидинмонофосфата (ОМФ), приводящее к получению уридинмонофосфата (УМФ), а после переаминирования части его молекул - к ЦМФ.
Подготовка мононуклеотидов к полимеризации
Образовавшиеся нуклеозидмонофосфаты, как отмечено выше, для выполнения своих функций с помощью соответствующих киназ подвергаются постадийному фосфорилированию:
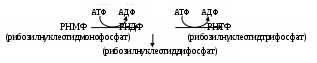
Получившиеся продукты являются макроэргами и могут использоваться в самых разных реакциях: УТФ в синтезе полисахаридов, ЦТФ в генезе фосфолипидов, ГТФ при транслокации иРНК на рибосоме и т.д. В таком же виде эти мононуклеотиды необходимы при транскрипции. В репликации (образовании ДНК) требуются их дезоксипроизводные; для этих целей используется следующая схема:
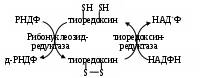
Участвующие в ней нуклеозиддифосфаты фосфорилируются, затем в дАТФ, дГТФ, дЦТФ; а от дУДФ, наоборот, отнимается фосфат. В дальнейшем с ним идут следующие преобразования:
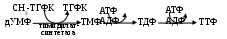
Замечено, что нуклеозид тимидин может легко фосфорилироваться до ТМФ под действием тимидинкиназы, т.е. возможен ресинтез (а не de novo) этого соединения.
Патология обмена мононуклеотидов
Гиппократ более 2500 лет назад описал болезнь подагру, которую считал патологией полководцев, аристократов, монахов, а в наше время ее называют болезнью королей и королем болезней. Ею страдали Колумб, Ньютон, Дарвин, Стендаль, Томас Мор, Рубенс, Бетховен, Рембрант, Тургенев и другие. В основе этого заболевания лежит развитие хронической гиперурикемии - повышенное содержание уратов в плазме крови. Причины этого симптома имеют многочисленный характер (схема), поэтому различают: