ВУЗ: Не указан
Категория: Не указан
Дисциплина: Не указана
Добавлен: 15.08.2024
Просмотров: 500
Скачиваний: 0
СОДЕРЖАНИЕ
1.1. Естественные и гуманитарные науки
1. Наука – это способ познания мира, отрасль культуры и определенная система организованности.
2.1. Структурные уровни организации материи
2.3. Пространство, время, теория относительности
2.4. Мегамир. Космология и космогония
2.5. Положения и принципы квантовой механики
3. Порядок и беспорядок в природе
4.1. Этапы развития химического знания. Основные понятия
Современный вариант длинной формы периодической системы химических элементов
4.2. Реакционная способность веществ
5. Биологический уровень организации материи
5.1. Иерархия структурных уровней живой материи
Оценки потерь биологического разнообразия за последние четыре века
5.2. Молекулярный уровень организации живого
Примеры кодирования аминокислот кодонами днк
Важнейшие химические элементы клетки
Сравнение клеток растений и животных
Некоторые доминантные и рецессивные признаки человека
5.5. Теория эволюции органического мира
5.6. Происхождение и сущность жизни
6.4. Физиология человека, здоровье, творчество, эмоции
3. Самым распространённым неорганическим веществом в живых организмах является вода. Свободная вода находится в межклеточных пространствах, сосудах, вакуолях, полостях органов. Её функцией является перенос веществ из окружающей среды в клетки и обратно. Связанная вода входит в состав некоторых клеточных структур, находясь между молекулами белка, мембранами, или соединяется с некоторыми белками.
4. Уникальные свойства воды связаны со структурой её молекулы, обладающей полярностью и способностью образовывать водородные связи:
– вода легко растворяет газы, ионные и некоторые неионные, но полярные соединения (гидрофильные вещества), что повышает их реакционную способность;
– слабая растворимость в воде жиров, нуклеиновых кислот и некоторых белков приводит к тому, что тонких слой этих гидрофобных веществ позволяет ограничить переход воды между клеткой и окружающей её средой, а также между различными участками клетки;
– вода обладает высокой теплопроводностью, что обеспечивает равномерное распределение тепла по всему организму;
– вода обладает высокой теплоёмкостью, что защищает ткани организма от резких изменений температуры, а также обеспечивает возможность его охлаждения испарением воды (транспирация у растений и потоотделение у животных);
– практическая несжимаемость воды определяет объём и упругость клеток и тканей, а также поддерживает форму у круглых червей, медуз и других организмов;
– оптимальное для биологических систем значение силы поверхностного натяжения обеспечивает капиллярный ток крови или токи растворов в растениях.
5. Минеральные вещества клетки в основном представлены солями, диссоциированными на ионы, или находящимися в твёрдом состоянии. Кристаллические включения в цитоплазму (соли кальция и фосфора) образуют опорные структуры клетки и организма (минеральное вещество костной ткани, раковины моллюсков, хитин и др.). Различная концентрация неорганических ионов (K+, Na+, Ca2+, Mg2+, NH3+, Cl–, HPO42–, H2PO4–, HCO3–, NO3–, PO43–, CO32– ) создаёт разность потенциалов между содержимым клетки и окружающей средой, что обеспечивает раздражимость и передачу возбуждения по нервам и мышцам. Кроме того, ионы являются компонентами буферных систем, поддерживающих требуемый уровень кислотности. Соединения азота, фосфора, кальция и других неорганических веществ используются для синтеза органических молекул (аминокислот, белков, нуклеиновых кислот и др.). Ионы многих металлов (Mg, Ca, Fe, Zn, Cu, Mn, Mo, Br, Co) являются компонентами многих ферментов, гормонов и витаминов. Например, ион железа входит в состав гемоглобина, а ион цинка – в гормон инсулина.
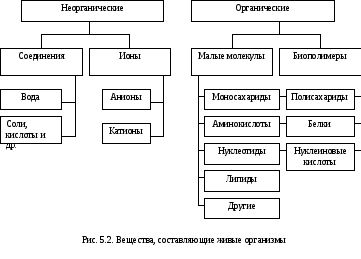
6. Биополимерами являются белки, нуклеиновые кислоты, полисахариды.
7. Углеводами, или сахаридами, называются органические соединения, в состав которых входят углерод, водород и кислород. Название этих веществ связано с тем, что в большинстве углеводов атомов водорода содержится вдвое больше, чем атомов кислорода, аналогично молекуле воды. Углеводы делят на три класса: моносахариды, олигосахариды и полисахариды.
8 .Моносахаридами.
называются простые углеводы – бесцветные
вещества, хорошо растворимые в воде и
обладающие приятным сладким вкусом. К
распространённым моносахаридам относятся
гексозы (глюкоза, галактоза и др.), пентозы
и триозы. Латинские числительные в
названии показывают число атомов
углерода в молекуле моносахарида, другие
слова могут быть связаны со свойствами
(глюкоза – сладкий вкус), или с
происхождением вещества (термин
«галактоза» указывает на содержание
этого моносахарида в молоке). Например,
молекула глюкозы (одного из гексозов),
содержит 6 атомов углерода, (рис. 5.3).
Глюкоза является мономером полисахаридов
(крахмала, гликогена, целлюлозы) и
присутствует в клетках всех организмов.
.Моносахаридами.
называются простые углеводы – бесцветные
вещества, хорошо растворимые в воде и
обладающие приятным сладким вкусом. К
распространённым моносахаридам относятся
гексозы (глюкоза, галактоза и др.), пентозы
и триозы. Латинские числительные в
названии показывают число атомов
углерода в молекуле моносахарида, другие
слова могут быть связаны со свойствами
(глюкоза – сладкий вкус), или с
происхождением вещества (термин
«галактоза» указывает на содержание
этого моносахарида в молоке). Например,
молекула глюкозы (одного из гексозов),
содержит 6 атомов углерода, (рис. 5.3).
Глюкоза является мономером полисахаридов
(крахмала, гликогена, целлюлозы) и
присутствует в клетках всех организмов.
Наибольшее значения для живых организмов имеют рибоза, дезоксирибоза, глюкоза, фруктоза, галактоза, (рис. 5.4).
9. Олигосахариды образованы двумя (дисахариды) или несколькими моносахаридами. Наиболее распространены следующие дисахариды: сахароза, мальтоза, лактоза.
10. Полисахариды представляют собой полимеры из остатков моносахаридов, соединённых ковалентными связями (крахмал, гликолен, целлюлоза, хитин и др.).
11. Основными функциями углеводов являются следующие:
– энергетическая: при их расщеплении и окислении углеводов выделяется энергия, обеспечивающая жизнедеятельность организмов;
– запасающая:
при избытке углеводов они накапливаются
в клетке и используются при необходимости
в качестве источника энергии;
запасающая:
при избытке углеводов они накапливаются
в клетке и используются при необходимости
в качестве источника энергии;
– структурная, или строительная: от 20 до 40 % материала клеточных стенок составляет прочная, нерастворимая в воде целлюлоза; в состав клеточных стенок некоторых простейших и грибов входит хитин, он же является компонентом наружного скелета у отдельных групп животных;
– защитная: твёрдые клеточные стенки одноклеточных, хитиновые покровы членистоногих, а также камеди (смолы, производные моносахаридов) препятствуют проникновению в раны болезнетворных микроорганизмов.
1 2.Липиды
– жироподобные вещества, выполняющие
следующие функции:
2.Липиды
– жироподобные вещества, выполняющие
следующие функции:
– энергетическую: накопление энергии, освобождающейся при расщеплении;
– запасающую: липиды накапливаются в клетке и используются при необходимости в качестве источника энергии, а также воды, что ценно для пустынных животных;
– структурную: входят в состав клеточных мембран;
– защитную: отделяют содержимое клетки от окружающей среды и обеспечивают её теплоизоляцию благодаря низкой теплопроводности, а также сохранение воды из-за водоотталкивающих свойств (гидрофобности);
– регуляторную: многие производные липидов участвуют в обменных процессах (гормоны коры надпочечников, половых желез, витамины А, D, E), а также влияют на мембранные процессы, в том числе на транспорт ионов, активность ферментов и др.
13. Универсальным субстратом жизни, характеризующимся структурным и функциональным разнообразием, являются белки и нуклеиновые кислоты.
14. Белки представляют собой высокомолекулярные природные полимеры, построенные из остатков аминокислот, которые соединяются друг с другом пептидной связью. В составе белков обнаружено 20 различных аминокислот, являющихся мономерами белков.
15. Молекула каждой аминокислоты состоит из двух частей. Одна часть у всех аминокислот одинакова, в неё входят углерода (С), основная аминогруппа (NH2) и кислотная карбоксильная группа (COOH), (рис. 5.5). Другая часть называется радикалом (R), (рис. 5.5 а), она у всех аминокислот разная. Примерами могут служить следующие аминокислоты: валин (рис. 5.5 б) и цистеин (рис. 5.5 в).

16. Для образования белкового полимера аминокислоты связываются путём взаимодействия основной аминогруппы и кислотной карбоксильной группы (рис. 5.6). От аминогруппы отщепляется атом водорода H, а от карбоксила – группа OH. За счет освободившихся валентных связей молекулы аминокислот соединяются, а отщепившиеся атомы образуют молекулу воды. Такая связь называется пептидной, а образовавшееся соединение – пептидом. Дипептид (димер) представляет собой соединение двух аминокислот, трипептид (тример) – трёх, а полипептид (или полимер) является соединением многих аминокислот. Именно полипептиды были возможными предшественниками белков в процессе биохимической эволюции.
Природный белок также представляет собой полипептид, содержащий десятки или сотни аминокислотных звеньев. Белки различаются не только по составу аминокислот и их числу, но и по порядку их расположения в цепи. По этой причине число различных белков, содержащихся в клетках животных и растений очень велико.
17. Классификация белков. Протеины состоят только из белков, протеиды содержат небелковую часть, например, гемоглобин. Белки, состоящие только из аминокислот, называются простыми. В состав сложных белков могут входить углеводы, жиры, нуклеиновые кислоты и др.
18. Первичная структура белка представляет собой линейную последовательность, или цепь аминокислотных звеньев, соединённых прочными пептидными (ковалентными) связями.
Вторичной структурой белка является пространственная спираль: молекула белка закручивается по винтовой линии за счёт образования водородных связей между пептидными группами, то есть между NH и CO (рис. 5.7). Водородные связи значительно слабее ковалентных, но из-за их многократного повторения получается также устойчивая структура.
Третичная структура представляет собой специфическую для каждого белка конфигурацию, имеющую вид клубка (глобулу). Такая укладка пространственной спирали обусловлена ионными, водородными и дисульфидными связями между остатками цистеина, а также гидрофобным взаимодействием. Последнее представляют собой силы сцепления между неполярными молекулами или неполярными радикалами, встречающимися у ряда аминокислот. Эти силы ещё слабее водородных, но благодаря их многочисленности также обеспечивают не только достаточную устойчивость белковой молекулы, но и её высокую подвижность.
Ч етвертичная
структура характерна не для всех белков.
Она возникает в результате соединения
нескольких глобул в сложный комплекс
из белковых макромолекул. Это полимерные
образования, в которых в роли мономеров
выступают макромолекулы белка. Они
соединяются также слабыми связями
(водородными, гидрофобными). Примером
может служить гемоглобин – комплекс
из четырёх молекул этого белка, способный
лишь в такой конфигурации осуществлять
необходимые функции: присоединять и
транспортировать молекулы кислорода.
етвертичная
структура характерна не для всех белков.
Она возникает в результате соединения
нескольких глобул в сложный комплекс
из белковых макромолекул. Это полимерные
образования, в которых в роли мономеров
выступают макромолекулы белка. Они
соединяются также слабыми связями
(водородными, гидрофобными). Примером
может служить гемоглобин – комплекс
из четырёх молекул этого белка, способный
лишь в такой конфигурации осуществлять
необходимые функции: присоединять и
транспортировать молекулы кислорода.
19. Утрата белковой молекулой своей природной структуры называется денатурацией, которая может возникать под воздействием температуры, химических веществ, обезвоживания, облучения и других факторов. При восстановлении нормальных условий белок может восстановить свою структуру, если не нарушена первичная цепь аминокислот.
20. Функции белков:
– строительная (или структурная) функция означает, что белки являются основой всех биологических мембран и всех органоидов клетки (коллаген – компонент перьев, волос, рогов; эластин – эластичный компонент связок, стенок, кровеносных сосудов);
– ферментативная (каталитическая) функция заключается в том, что белковые молекулы ферментов способны ускорять течение биохимических реакций в клетке в сотни миллионов раз;
– транспортная функция белков реализуется в процессе переноса белками различных веществ через клеточные мембраны, а также от одних органов к другим;
– защитную функцию выполняют специфические белки, предохраняющие организм от вторжения чужеродных организмов и от повреждения (антитела, блокирующие чужеродные белки; интерфероны – универсальные противовирусные белки; фибриноген, тромбин и другие, предохраняющие организм от потери крови образованием тромба);
– регуляторная функция присуща белкам-гормонам, которые регулируют различные физиологические процессы, например, инсулин, регулирующий содержание глюкозы в крови;
– энергетическая функция может выполняться белками в процессе их распада с выделением энергии, но реализуется очень редко;
– двигательная функция заключается в том, что все виды движений, к которым способны клетки и организмы (сокращение мышц у высших животных, мерцание ресничек у простейших, движение жгутиков, двигательные реакции у растений и др.), выполняются особыми, сократительными белками;
– информационная роль выполняется рецепторными белками, которые расположены на наружной стороне мембраны для получения информации о состоянии внешней среды и восприятия различных регуляторных сигналов, в том числе и гормональных.
21. Нуклеиновые кислоты – это биополимеры, осуществляющие хранение и передачу наследственной информации во всех организмах, а также участвующие в биосинтезе белков. Существует два типа нуклеиновых кислот: дезоксирибонуклеиновая (ДНК) и рибонуклеиновая (РНК). Наиболее высокое содержание нуклеиновых кислот обнаружено в ядрах клеток, именно оттуда эти кислоты получили своё название от латинского слова «нуклеус» – ядро. Впоследствии выяснилось, что нуклеиновые кислоты имеются в цитоплазме, а также в митохондриях и пластидах.
Первичной нуклеиновой кислотой на Земле была РНК.
22. Самую большую молекулярную массу имеет ДНК, содержащая 100 млн. нуклеотидов. Она состоит из двух цепей, спирально закрученных одна вокруг другой и соединённых друг с другом по всей длине водородными связями, (рис. 5.8). Такую конструкцию называют двутяжевой цепью.